Преждевременная недостаточность яичников (ПНЯ) – мультифакториальное заболевание со значительным вкладом генетической детерминированности, одной из ведущих, социально значимых жалоб при котором является стойкое бесплодие, с выраженной резистентностью к стандартным методам лечения. ПНЯ определяется как гипогонадизм в возрасте до 40 лет у женщин, ранее имевших нормальный менструальный цикл. Данный диагноз может быть установлен при получении минимум двух результатов повышенного ФСГ (>25 МЕ/л) с интервалом в 4 недели [1]. Частота данной нозологии колеблется от 1 до 13% [2].
Метод активации фолликулярного роста, впервые описанный K. Kawamura, A. Hsueh и соавт., эффективность которого подтверждена клинически, а также данными молекулярно-генетических исследований, сегодня нашел применение в различных модификациях более чем в 6 странах мира [3, 4]. Одним из фундаментальных обоснований механизма хирургического воздействия в рамках описанной методики является влияние фрагментации ткани яичников на полимеризацию актина, прекращению передачи сигнала по пути Hippo, повышению концентрации факторов роста CCN и ингибиторов апоптоза BIRС 1,7 [5]. Изначально методика японских исследователей предполагала проведение односторонней овариэктомии с последующим этапом демедулляции под гистологическим контролем, криоконсервации коркового слоя яичниковой ткани, его фрагментации и двухдневной активации in vitro (добавление в среду ингибитора PTEN и активатора PI3K-сигнальных путей). Далее производилась ипсилатеральная трансплантация фрагментированной размороженной ткани под серозную оболочку маточной трубы лапароскопическим доступом [4].
Дальнейшее изучение фундаментальных механизмов хирургической активации яичниковой ткани позволило оптимизировать методику до одноэтапного метода. В России первая операция, в основу которой легла хирургическая активация функции яичников, была произведена академиком Л.В. Адамян 06.03.2019 г. [6]. При этом были разработаны собственные подходы к тактике ведения, включающей критерии отбора пациентов, клинико-лабораторное обследование, предоперационную подготовку, оперативное лечение и послеоперационное ведение.
Клиническое наблюдение
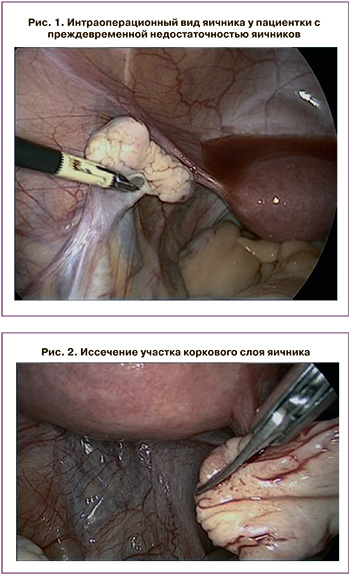 Больная А., 32 лет, с верифицированным диагнозом ПНЯ обратилась в ФГБУ «НМИЦ АГП им. В.И. Кулакова» для решения вопроса о возможности реализации репродуктивной функции с использованием собственных ооцитов. Из анамнеза: родилась путем самопроизвольных срочных родов от матери 27 лет, второй ребенок в семье, имеет старшую сестру. Возраст менопаузы у матери 52 года.
Больная А., 32 лет, с верифицированным диагнозом ПНЯ обратилась в ФГБУ «НМИЦ АГП им. В.И. Кулакова» для решения вопроса о возможности реализации репродуктивной функции с использованием собственных ооцитов. Из анамнеза: родилась путем самопроизвольных срочных родов от матери 27 лет, второй ребенок в семье, имеет старшую сестру. Возраст менопаузы у матери 52 года.
Менархе с 14 лет, менструации установились сразу, регулярные, по 4–5 дней, через 28 дней, умеренные, безболезненные. В течение последних 2 лет отмечает изменение ритма менструаций – укорочение межменструального интервала до 24–25 дней, уменьшение объема менструальной кровопотери. При гормональном обследовании отмечалось периодическое увеличение сывороточного уровня фолликулостимулирующего гормона (ФСГ) до 33 МЕ/л, ассоциированное с эпизодами олигоменореи, в связи с чем обоснован прием заместительной гормональной терапии (эстрадиола валерат 2 мг + дидрогестерон 10 мг) в течение 2 менструальных циклов до операции для повышения эффективности хирургического этапа лечения. Пациентка была обследована, и в связи с критическим снижением овариального резерва и нецелесообразностью стимуляции функции яичников была рекомендована донация ооцитов как единственно возможный вариант достижения беременности.
На дооперационном этапе было проведено полное клинико-лабораторное исследование. Базальные уровни гонадотропинов: ФСГ – 33 МЕ/л, лютеинизирующий гормон (ЛГ) – 9,7 МЕ/л, эстрадиол – 73,4 пмоль/л, антимюллеров гормон (АМГ) < 0,13 нг/мл. По данным осмотра, клинико-лабораторного обследования, в том числе ультразвукового исследования в режиме 3D-сканирования, установлен диагноз: Бесплодие. Сниженный овариальный резерв.
Учитывая наличие бесплодия в течение 2 лет, отсутствие эффекта от проведенного ранее лечения, выраженное снижение овариального резерва, а также настойчивое желание пациентки реализовать репродуктивную функцию с использованием собственных ооцитов, с целью оптимизации комплексного лечения бесплодия было принято решение о проведении оперативного вмешательства – одноэтапного хирургического метода активации функции яичников: лапароскопии, ревизии органов брюшной полости и малого таза, хромогидротубации, биопсии коркового слоя обоих яичников с последующей его фрагментацией и одноэтапной реимплантацией, гистероскопии, биопсии эндометрия (рис. 1–6) [6]. После получения информированного добровольного согласия больной проведено оперативное вмешательство в планируемом на предоперационном этапе объеме. Интраоперационно было выявлено: яичники уменьшены в размерах (27×18×22 мм), белесовато-желтого цвета, с глубокими бороздами на поверхности, плотной консистенции, без стигм функциональной активности (без видимых фолликулов, желтых и белых тел) (рис. 1), при разрезе – с признаками минимальной васкуляризации, утолщенной белочной оболочкой. При гистероскопии: эндометрий равномерной толщины, сосудистый рисунок не усилен, железистый рисунок сохранен. Органы брюшной полости без видимых патологических изменений. Аппендикс оперативно удален ранее.
Биоптат эндометрия и 10% объема каждого фрагмента яичниковой ткани были отправлены на гистологическое исследование. При проведении гистологического исследования установлено: ткань яичников с фиброзом стромы коркового слоя без визуализации фолликулярного аппарата. Эндометрий стадии ранней пролиферации.

Операция длительностью 1 ч 5 минут прошла без осложнений, кровопотеря составила 10 мл. Послеоперационный период протекал без особенностей. Выписана на 3-е сутки после операции.

На 3-й день после оперативного вмешательства проведено повторное гормональное исследование с определением уровня гонадотропинов и эстрадиола. Уровень эстрадиола составил 335 пмоль/л, что в 4,5 раза превышает дооперационную концентрацию. Существенной динамики в уровнях гонадотропинов выявлено не было.
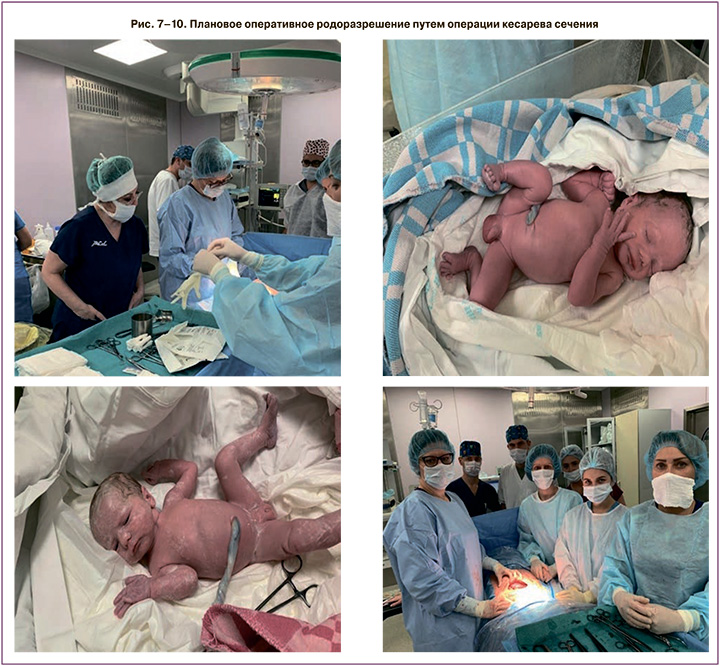
Спустя 1,5 месяца после операции в связи с задержкой менструации был определен сывороточный уровень бета-субъединицы хорионического гонадотропина (В-ХГЧ), равный 800 мМЕ/мл. При ультразвуковом исследовании установлено наличие многоплодной беременности – дихориальной диамниотической двойни. Беременность протекала без осложнений в течение всего периода гестации. По данным скрининговых исследований отклонений выявлено не было. 1 октября 2020 г. было выполнено плановое оперативное родоразрешение путем операции кесарева сечения при сроке беременности 37 недель 4 дня (хирург: Николаева А.В.). Операция продолжительностью 33 минуты прошла без осложнений, на 2-й минуте за паховые сгибы извлечена живая доношенная девочка массой 2620 г, длиной 49 см, оценка состояния по шкале Апгар 8/9 баллов. На 3-й минуте за подмышечные впадины извлечен живой доношенный мальчик массой 2332 г, длиной 47 см, оценка состояния по шкале Апгар 8/8 баллов (рис. 7–10).
Послеродовый период проходит без осложнений. В дальнейшем планируется динамическое наблюдение за состоянием пациентки с проведением полного клинико-лабораторного обследования.
Заключение
В результате разработанной нами тактики ведения, включающей клинико-лабораторное и инструментальное обследование, гормональную подготовку, а также хирургический этап – одноэтапный хирургический метод активации функции яичников, отмечено улучшение общего самочувствия, психоэмоционального фона у ряда пациентов, изменение показателей овариального резерва, а именно положительная динамика гормонального статуса, сопряженная с активацией фолликулярного роста по данным ультразвукового исследования, ответом на стимуляцию функции яичников в циклах ЭКО с получением собственного клеточного материала и достижением беременности у ряда пациенток.
Приведенный клинический случай, демонстрирующий самопроизвольное наступление беременности и родоразрешение у пациентки с ПНЯ позволяет считать данную операцию целесообразной к выполнению у пациенток с выраженным снижением овариального резерва, как альтернативу донации ооцитов.



