Хронический эндометрит (ХЭ) до сих пор остается недостаточно изученной патологией, которая сопряжена с неблагоприятными репродуктивными последствиями, такими как несостоявшаяся имплантация и повторный выкидыш [1]. Изменение представления об этиологическом факторе ХЭ за последние десятилетия, подтверждающем немаловажную роль диссоциаций факультативно- и облигатно-анаэробных микроорганизмов и вирусов, зачастую приводит к развитию клинически стертых и атипичных форм заболевания, которые безусловно затрудняют диагностику ХЭ и значительно снижают эффективность классических схем его лечения [2–4].
Латентное течение ХЭ увеличивает длительность персистенции повреждающего фактора и приводит к тому, что воспалительный процесс нарушает баланс про- и антиангиогенных факторов, возникают гипоксия и ишемия ткани, что в итоге вызывает нарушение кровоснабжения не только эндометрия, но и матки в целом [5–7]. Анатомо-патологические изменения проявляются высокой плотностью сосудов с пролиферацией эндотелия и отеком, связанным с гиалиновым утолщением стенки, окклюзией просвета, тромбозом мелких сосудов и сегментарной фибриноидной дегенерацией [8].
В связи с тем, что воспалительный процесс слизистой оболочки полости матки вызывает расстройства кровоснабжения, выявление нарушений сосудистого русла позволит повысить неинвазивную диагностику ХЭ. По рекомендации консенсуса IETA (International Endometrial Tumor Analysis) для оценки васкуляризации срединных отделов матки предложен метод визуализации сосудов по 4-балльной градации от 1 (аваскуляризация) до 4 (гиперваскуляризация), который можно использовать при заболеваниях эндометрия, в том числе ХЭ [9]. Недостатком этой методики является субъективизм, зависящий от опыта врача, настроек и технического уровня сканера.
Ультразвуковая спектральная допплерография применяется для исследования сосудистого русла в эндометрии и миометрии. Однако спектральная допплерография позволяет оценить показатели только в одном выбранном сосуде. А это может неправильно отражать изменения кровообращения во всем органе [10].
Трехмерная (3D) ультразвуковая допплерография позволяет оценить васкуляризацию во всем объеме органа или его части, например в матке или эндометрии, и является хорошим инструментом для оценки физиологических и патологических изменений кровообращения.
Терапия ХЭ начинается с антибактериальных и/или антивирусных препаратов с последующим назначением лечения, направленного на восстановление гомеостаза, в том числе адекватного кровоснабжения эндометрия. Второй этап включает гормональную, метаболическую и иммуномодулирующую терапию, физиотерапию [11].
В последние годы появились научные исследования применения локальной цитокинотерапии, являющейся комплексом натуральных противомикробных пептидов, цитокинов и универсальным стимулятором иммунной системы, обладающей антибактериальной, противовирусной и антиоксидантной активностью, снижающей проявления воспалительного процесса с последующим восстановлением и эпителизацией поврежденных поверхностей, в которых оценивалась эффективность таких препаратов [12–18]. В научных работах были доказаны уменьшение проявлений воспаления, снижение его аутоиммунного компонента, нормализация концентраций про- и противовоспалительных цитокинов, иммуноглобулинов в эндометрии. Авторы отмечали более быстрое и стойкое нивелирование признаков заболевания, что позволило повысить чувствительность к антибактериальной терапии, а также сократить сроки излечивания пациенток.
Являясь естественными передатчиками сигналов между иммунными клетками, цитокины участвуют в регуляции иммунного ответа [19]. Если активность клеток недостаточна, дополнительная доза экзогенных цитокинов способствует усилению их функциональной активности, а в случае избыточной активности подавляет ее, способствуя нормализации их функционирования. Это положение подтверждается Тапильской Н.И. и соавт. (2022), в исследовании которых выявлено снижение количества Т-лимфоцитов (CD8+) и В-лимфоцитов (CD20+) в стромальном компоненте эндометрия и, наоборот, увеличение количества Т-хелперов (СD4+), что приводило к снижению признаков ХЭ и наблюдалось у значительно большего числа пациенток, получавших антибактериальную и цитокинотерапию, по сравнению со стандартным курсом лечения [20].
Таким образом, локальная цитокинотерапия является одним из эффективных альтернативных способов лечения персистирующего воспаления в эндометрии, и назначение этих препаратов представляет перспективное дополнение к комплексному лечению ХЭ. В отечественной и зарубежной литературе не обнаружено работ, посвященных ультразвуковому исследованию кровотока в матке, в том числе в эндометрии, при включении в схему лечения препаратов цитокинов.
Цель исследования: оценить влияние лечения ХЭ, в том числе с применением цитокинотерапии, на маточно-эндометриальный кровоток.
Материалы и методы
Проведено ретроспективное когортное исследования 298 женщин репродуктивного возраста с клинико-морфологически верифицированным диагнозом ХЭ.
Основную группу составили 140 пациенток, которые получили противовоспалительную терапию, включающую такие комбинации антибиотиков, как макролиды последнего поколения+нитроимидазол; макролиды+цефалоспорины III поколения; защищенные пенициллины+макролиды. Терапия была дополнена противогрибковыми, противовирусными и иммуномодулирующими препаратами. По мере выявления сопутствующей флоры были назначены антипротозойные, противомикробные средства, антисептики. Дополнительно в этой группе применялась цитокинотерапия в виде однократного курса препарата «Суперлимф» 25 ЕД в 1 свече вагинально на ночь длительностью 20 дней.
Группу сравнения составили 158 женщин, получавших противовоспалительное лечение по той же схеме без применения экзогенных цитокинов. Клиницисты при назначении терапии руководствовались стандартами оказания медицинской помощи, препаратами, зарегистрированными в Российской Федерации, и действующими инструкциями по медицинскому применению, опубликованными в Реестре лекарственных средств (https://www.rlsnet.ru/).
В исследование не были включены женщины с сопутствующей патологией, включающей эндометриоз, миому матки, с патологией труб и/или яичников.
Перед исследованием было получено одобрение Этического комитета факультета непрерывного медицинского образования РУДН.
Всеми пациентками подписаны добровольные информированные согласия на публикацию своих данных.
Возраст пациенток основной группы соответствовал 34,7 (6,6) года, группы сравнения – 33,5 (5,4) года. Клиническая диагностика ХЭ проводилась на основании анамнестических данных, предъявляемых жалоб, двуручного исследования. Морфологическая диагностика основывалась на результатах цитологических и гистологических исследований эндометрия после гистероскопии, морфологического и иммуногистохимического анализа эндометрия, полученного при пайпель-биопсии, обнаружении плазматических клеток (CD138) и/или моноклональных антител к антигенам иммунных клеток (CD4, CD8, CD20).
Ультразвуковое обследование органов малого таза проводилось на аппарате Affiniti70 (Philips, Нидерланды) трансвагинальным доступом с применением объемного внутриполостного датчика, с последующей реконструкцией изображения в 3D-режиме в раннюю пролиферативную фазу менструального цикла. Контрольное исследование осуществляли спустя месяц после окончания лечения также в раннюю пролиферативную фазу.
Для количественной оценки степени васкуляризации матки и эндометрия использовалась прикладная программа QLab, работающая в ангиорежиме при 3D-реконструкции с получением индекса васкуляризации (VI); потокового индекса (FI) и васкуляризационно-потокового индекса (VFI).
При импульсно-волновой допплерографии маточных артерий (МА) исследовали такие показатели, как максимальная скорость кровотока (Vmax), конечно-диастолическая скорость (Vmin), средняя скорость (Vmean), пульсационный индекс (PI) и индекс резистентности (RI), а также измеряли диаметр МА.
В дальнейшем определяли индекс артериальной перфузии (ИАП), который отражает перфузию 1 см3 тела матки кровью, поступающей по обеим МА, выраженный в процентах. Для этого вычисляли объемный кровоток (см3 за один сердечный цикл) в каждой из МА по следующей формуле:
Vvol = Vmean×S,
где S – площадь маточной артерии (см2).
ИАП вычисляется по формуле:
ИАП (%)=(VvolМАправая+VvolМАлевая)/Vматки×100,
где VvolМАправая – объемный кровоток по правой МА (см3); VvolМАлевая – объемный кровоток по левой МА (см3); Vматки – объем матки (см3).
Статистический анализ
Для статистического анализа использовалось программное обеспечение SPSS 27.0 (IBM, США). Нормальность распределения проверялась с помощью теста Шапиро–Уилка. Учитывая, что большинство данных не подчинялись нормальному распределению, все результаты представлены как медиана (Me) и интерквартильный размах (Q1; Q3).
Сравнение между двумя независимыми группами (основная группа и группа сравнения) проводили с помощью непараметрического критерия Манна–Уитни. Сравнение между двумя связными группами (показатели правой и левой МА до и после лечения в каждой из групп) проводилось с помощью непараметрического критерия Уилкоксона. Динамика значений переменных оценивалась как разность значений до и после лечения, для полученных величин также проводился тест на нормальность распределения. Для описания разностей использовались Me (Q1; Q3) и применялись непараметрические критерии. Дискретные признаки представлены в виде абсолютного числа (n) и относительной величины (%). Гипотезу о равенстве средних для групп с бинарными признаками проверяли с помощью критерия Мак-Немара с поправкой Йейтса.
С целью выявления и оценки тесноты связи между двумя рядами сопоставляемых количественных показателей использовали коэффициент ранговой корреляции Спирмена с интерпретацией по шкале Чеддока. За пороговый уровень статистической значимости принято p<0,05.
Результаты
Возраст пациенток основной группы соответствовал 34 (29; 44) годам, группы сравнения – 33 (26; 42) годам (p>0,05). Длительность бесплодия в основной группе колебалась от 2 до 12 лет, в группе контроля – от 1 до 13 лет. Репродуктивный анамнез статистически значимых отличий между группами не имел (табл. 1).
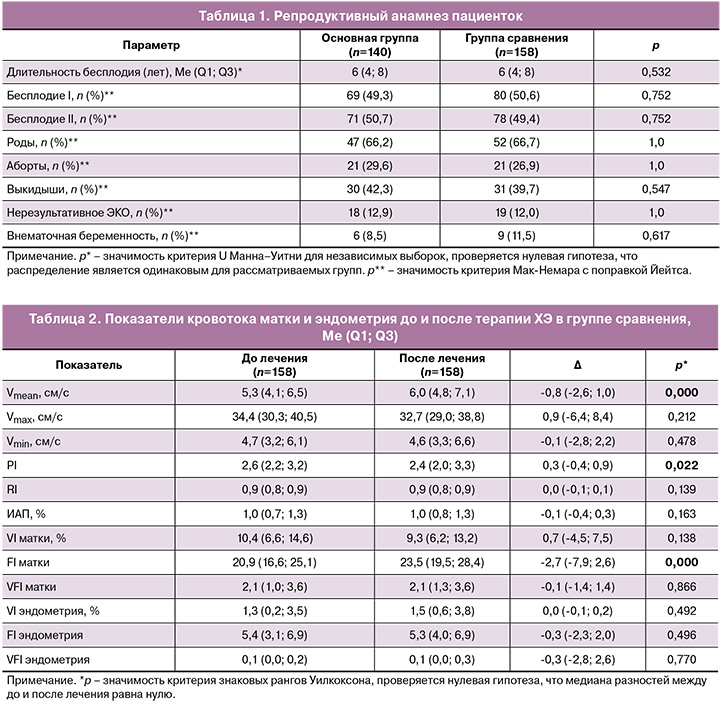
Анализ показателей кровотока правой и левой МА не выявил асимметрии цифровых значений (р>0,05).
Проведенное противовоспалительное лечение ХЭ в обеих группах привело к изменениям гемодинамики матки и кровоснабжения эндометрия. Так, в группе сравнения стандартный комплекс лечения продемонстрировал статистически значимое повышение Vmean, снижение PI МА и повышение FI матки. В основной группе применение цитокинотерапии отразилось на васкуляризации матки и эндометрия, что проявилось снижением значений VI и VFI матки, а также VI, FI и VFI эндометрия (p<0,05), в то время как отсутствовало влияние на скоростные показатели и уголнезависимые индексы (табл. 2–4).
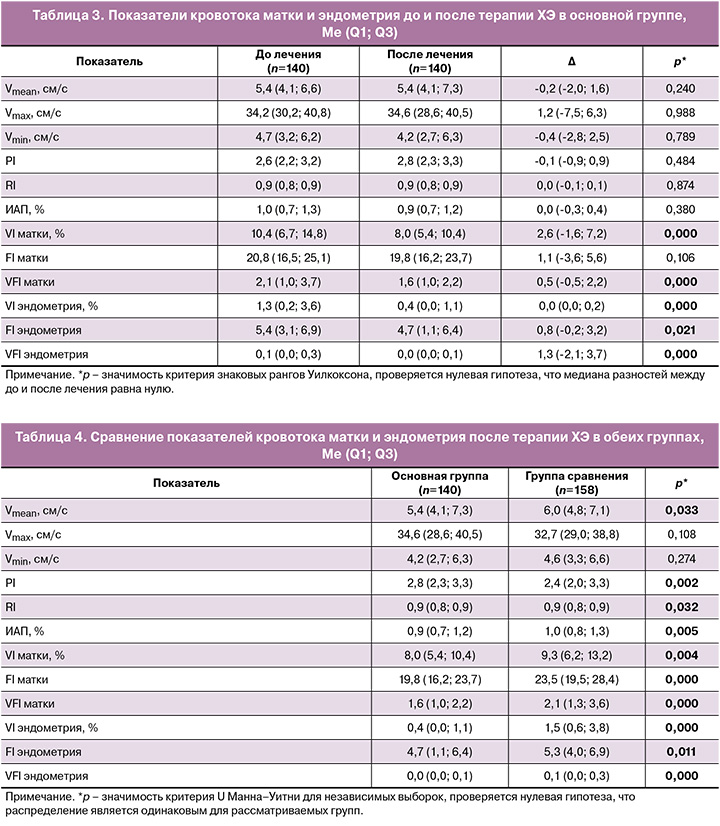
Влияние цитокинотерапии существенно потенцировало эффект противовоспалительной терапии, что привело к выраженному снижению васкуляризации как матки в целом, так и эндометрия; в то время как не оказывало значимого влияния на кровоток, регистрируемый в МА (табл. 5).
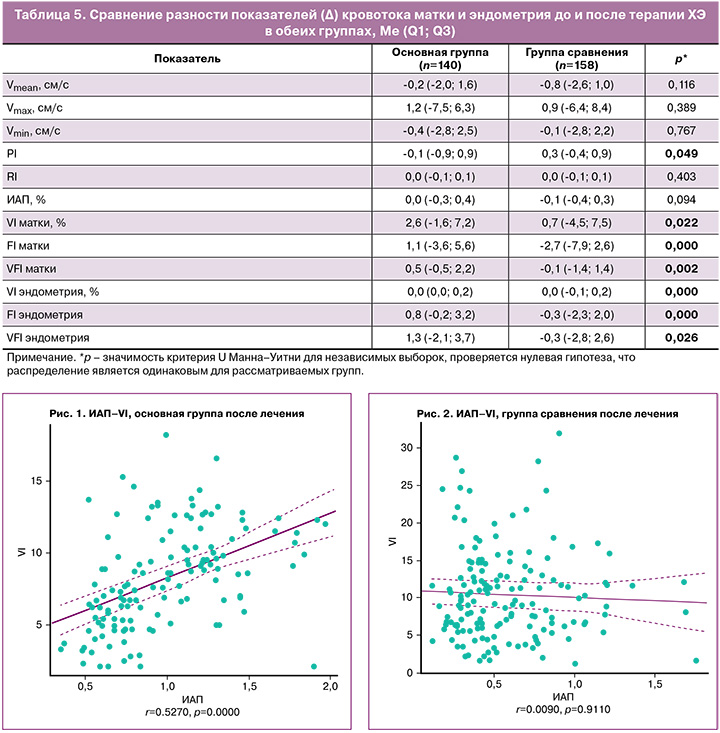
До лечения теснота связи между ИАП и VI матки составила r=-0,116, а между ИАП и VI эндометрия – r=0,038. После лечения в основной группе эти показатели имели значения r= 0,527 (рис. 1) и r=0,261, а в группе сравнения – r=-0,009 (рис. 2) и r= -0,014 соответственно.
Обсуждение
Одним из звеньев в цепи патофизиологических процессов при воспалении является расстройство микроциркуляции в очаге поражения, проявляющееся расширением сосудов, застоем крово- и лимфообращения, что в результате приводит к экссудации плазмы и миграции лейкоцитов [5], которые оказывают влияние на степень васкуляризации как эндометрия, так и матки, что было доказано ранее [21, 22].
Несмотря на широкое применение цветового картирования в рутинной диагностической практике, его возможности весьма ограничены для определения степени васкуляризации в тканях, где необходимо оценить микроциркуляторную сосудистую сеть, в частности, в срединных отделах матки, в том числе в эндометрии. Ограничение метода заключается в интерпретации показателей кровотока в отдельно взятых сосудах при строгом соблюдении определенного угла инсонации, что не всегда возможно, учитывая выраженно непрямолинейный ход спиральных и базальных артериол и вен, а также малый их просвет. На отсутствие связи между показателями кровотока в МА и кровотоком в эндометрии указывали многие авторы [23–26]. Как считают Мотовилова Т.М. и соавт. (2013), допплерометрия сосудов матки имеет особое значение при динамическом наблюдении с целью оценки эффективности лечения ХЭ [27]. Авторы указывают, что нарушение кровотока в маточных сосудах с преобладанием повреждений преимущественно на уровне базальных и спиральных артерий, а также сложности визуализации концевых артерий свидетельствуют о существенном нарушении перфузии ткани на фоне хронического воспалительного процесса в эндометрии. Применение лазерной терапии, по данным допплерометрии эндометрия, привело к выраженной положительной динамике в 78,2% случаев.
С помощью 3D-допплерографии и прикладных программ (VOCAL, Qlab) появилась возможность объективной оценки степени васкуляризации с получением VI, FI и VFI.
По результатам исследования показатель, который соответствует степени васкуляризации матки (VI), в основной группе значимо снизился после лечения, в том числе он оказался ниже, чем в группе сравнения (p<0,05). У пациенток, которым была добавлена цитокинотерапия, VI эндометрия также снизился, но в группе сравнения такого эффекта не произошло. Для интерпретации данного феномена было интересно сопоставить VI матки и эндометрия, которые отражают артерио-венозную «насыщенность» и ИАП, свидетельствующий об артериальном кровоснабжении матки. Выяснилось, что до лечения теснота связи как в матке, так и в эндометрии практически отсутствовала. После лечения в основной группе сила связи между артерио-венозным и артериальным кровотоком в матке была заметной (r=0,527), а в эндометрии осталась слабой (r=0,261); в группе сравнения теснота связи в матке и в эндометрии была слабой. Данный анализ свидетельствует о том, что степень васкуляризации зависит не только от притекающей артериальной крови, но и от адекватного венозного оттока, который нарушен при ХЭ. На фоне лечения происходит не столько изменение артериальной гемодинамики матки, сколько восстановление оттока венозной крови, более выраженное в матке. В эндометрии вследствие применения цитокинотерапии нарушение венозного оттока успешно купировалось, в то время как при стандартной схеме лечения аналогичного эффекта не наблюдалось. Такой результат демонстрирует нарушение гемодинамики матки за счет венозного звена и незначительные изменения артериального кровотока, которые лучше восстанавливаются при применении цитокинотерапии, а также ставит под сомнение целесообразность оценки скоростных показателей и уголнезависимых индексов МА для оценки эффекта лечения ХЭ.
Интенсивность тока крови в матке оценивается по FI. Данный индекс, несмотря на статистически значимое отличие между группами после лечения, при добавлении в курс лечения цитокинотерапии снизился (р>0,05), а в группе, получающей стандартную терапию, повысился (р<0,05). Возможно, это обусловлено особенностью микроциркуляторного русла, расположенного в толще миометрия, преимущественно за счет среднего кругового слоя, представленного гладкомышечными волокнами с большим количеством сосудов, среди которых много венозных. Контрактильная активность субэндометриального слоя миометрия путем механического воздействия на сосудистую стенку способствует улучшению венозно-лимфатического дренажа [27]. По-видимому, по этой причине значимая разница FI матки была отмечена между основной группой и группой сравнения.
В работе Селезневой Т.А. и соавт. (2016) исследовалось влияние препарата, стимулирующего продукцию эндогенных интерферонов и обладающего противовоспалительным и иммуномодулирующим действиями, на кровоток в радиальных и базальных ветвях МА у женщин с ХЭ [28]. Авторами было доказано, что комплексное лечение приводит к снижению RI в терминальных ветвях МА, однако влияние на кровоток в спиральных артериях оценено не было.
В работе Озерской И.А. и соавт. (2018) отмечено повышение конечно-диастолической скорости в ранней пролиферативной фазе менструального цикла у пациенток с эндометритом, что привело к повышению средней скорости кровотока, которая также была выше, чем у здоровых женщин, но практически не изменило ИАП [29]. Соответственно, достоверное снижение Vmean в основной группе отразилось на снижении ИАП в сравнении с группой, принимающей антибактериальную терапию, с разницей 5,1% (р<0,05), но по сравнению с показателями до лечения статистически значимых отклонений не выявлено.
Анализ полученных данных подтверждает тот факт, что в случае дополнения противовоспалительной терапии ХЭ цитокинами происходит перераспределение артериально-венозного русла, восстановление сбалансированной регуляции и функционирования микроциркуляторного кровотока таким образом, что объем крови в приносящих (артериальных) сосудах соответствует объему крови в выносящем (венозном) звене; об этом свидетельствуют снижение VI, FI и VFI матки и эндометрия при достаточно монотонных значениях ИАП, что приводит к уменьшению экссудации и выбросу провоспалительных цитокинов, способствуя угасанию воспалительного процесса. Также можно предположить, что гиперваскуляризация матки и эндометрия при воспалительном процессе обусловлены не увеличением артериального притока, а снижением (затруднением) венозного оттока и лимфооттока, которые сопровождают воспаление. Следует учитывать, что расширение аркуатного сплетения также может приводить к гиперваскуляризации миометрия на основании высоких показателей VI матки, но диагностически значимым является сочетание с гиперваскуляризацией эндометрия.
Проведенное исследование ультразвуковой оценки эффективности лечения на основании изменений маточно-эндометриального кровотока можно отнести к одному из первых в этом направлении. Не вызывает сомнений необходимость дальнейших исследований, направленных на выяснение особенностей кровоснабжения эндометрия при различных морфотипах ХЭ, а также схем и продолжительности лечения.
Заключение
Эффективность противовоспалительной терапии ХЭ, дополненной экзогенными цитокинами, влияет на гемодинамику матки и эндометрия за счет восстановления венозного оттока, что приводит к нормализации кровоснабжения эндометрия и доказывает целесообразность применения препарата «Суперлимф» в комплексном лечении.



