Согласно современным представлениям (2020 г.), хронический эндометрит (ХЭ) характеризуется как состояние воспалительных изменений эндометрия, сопровождающихся избыточной плотностью стромальных клеток и отеком, диссоциированным созреванием клеток эпителия и фибробластов на фоне плазматической инфильтрации стромы [1, 2]. Множественные вторичные морфофункциональные изменения, которые появляются как следствие персистенции повреждающего действия инфекционного агента с инфильтрацией стромы плазмоцитами, приводят к нарушению циклической транcформации эндометрия. Малосимптомная или в большинстве случаев бессимптомная клиническая картина, важность выполнения биопсии эндометрия для подтверждения диагноза приводят к тому, что данные о распространенности ХЭ весьма вариабельны – от 8 до 72% [3, 4]. Следует учесть, что до сих пор нет общепризнанных критериев диагностики ХЭ; по этой причине данные о реальной распространенности заболевания неизвестны и могут сильно разниться [5].
В настоящее время ХЭ как причина репродуктивных потерь остается актуальной проблемой, так как максимальная его частота приходится именно на возрастной период, который является наиболее важным в реализации репродуктивной функции женщин, и он продолжает занимать лидирующее положение в структуре внутриматочной патологии у пациенток с бесплодием, достигнув 65,2% [3].
Главной причиной ХЭ считают результат взаимодействия между бактериальным агентом и эндометриальным иммунитетом. Наиболее частыми инфекционными агентами являются распространенные бактерии, встречающиеся в урогенитальной области. По данным Краснопольского и соавт., наиболее часто встречаются ассоциации микроорганизмов, среди которых большую роль играют хламидии, уреаплазмы, микоплазмы, вирусы. Эти возбудители подготавливают среду для колонизации анаэробов, которые обнаруживаются в 70–80% случаев в мазках из маточных труб [6]. В результате исследований, направленных на изучение заболеваний шейки матки и эндометрия, выясняется, что вирусная инфекция также поражает женский репродуктивный тракт, приводя к нарушениям адекватного иммунного ответа на инфекцию, что, безусловно, ведет к созданию благоприятной среды для хронической персистенции вирусов и бактерий в полости матки [7]. По данным Espinoza J. et al., эндометрий также постоянно подвергается воздействию бактерий из половых путей, что свидетельствует о взаимодействии инфекционного агента с микроокружением эндометрия [8].
В настоящее время гистологически верифицированный диагноз основывается на данных результатов биоптатов слизистой полости у женщин с различными гинекологическими проблемами и у инфертильных женщин во время обследований по поводу бесплодия [9].
На сегодняшний день не существует общепринятых стандартизированных определений, диагностических рекомендаций для ХЭ, хотя многие эксперты сходятся во мнении, что наличие стромальных плазмоцитов является наиболее специфичным и чувствительным признаком при этой патологии, а к самому надежному критерию относят инфильтрацию слизистой CD138 (синдикан-1)-положительными плазматическими клетками [1, 10].
Гистероскопия также позволяет выявить признаки, заставляющие с большей долей вероятности предположить наличие ХЭ при обнаружении таких маркеров, как гиперемия слизистой, стромальный отек, микрополипы, при наличии которых показания к прицельной биопсии эндометрия являются обоснованными [11].
Для оценки эндометрия с успехом применяется ультразвуковая диагностика, преимуществами которой являются неинвазивность, отсутствие лучевой нагрузки, возможность многократных исследований в определенные дни менструального цикла, доступность и информативность. Наиболее предпочтительным является трансвагинальное исследование в сочетании с трехмерной реконструкцией на 5–7-й день менструального цикла [3]. Однако есть мнение, что эхография недостаточно эффективна для выявления внутриматочных поражений в связи с вариабельностью эхографических изменений эндометрия при циклической трансформации в течение менструального цикла [12].
Воздействие ХЭ на бесплодие все еще не до конца изучено. Несмотря на это, терапия хронически воспаленного эндометрия способна оказывать положительное влияние на женскую фертильность [9, 13, 14]. Диапазон эмпирических методов лечения, направленных на улучшение рецептивности эндометрия, в большинстве случаев основан на двух постулатах. Первый, что повышение маточного кровотока улучшает функциональное состояние эндометрия. Второй, что ХЭ является следствием измененной реакции иммунной системы женщины [3].
Стандартом начала терапии ХЭ является проведение антибактериального лечения с целью элиминации инфекционного агента. Следующий этап лечения направлен на восстановление гомеостаза и морфофункциональных характеристик эндометрия. Разными авторами предложено и рекомендовано использовать гормональную, метаболическую и иммуномодулирующую терапию, физиотерапию [9, 15, 16].
В последнее время научное сообщество старается найти возможность применения в качестве комплексной терапии ХЭ все более расширенный спектр средств. В частности, методом выбора может стать применение локальной цитокинотерапии, являющейся комплексом натуральных противомикробных пептидов, цитокинов и универсальным стимулятором иммунной системы, обладающей противовирусной и антиоксидантной активностью, снижающей проявления воспалительного процесса с последующим восстановлением и эпителизацией поврежденных поверхностей [1, 5, 14].
Эффективность таких препаратов оценивалась в ряде исследований. Например, в работах Дикке Г.Б. и Остроменского В.В. [16], а также Кореевой Н.В. и Доброхотовой Ю.Э. [17] было доказано уменьшение проявлений воспаления, снижение его аутоиммунного компонента, нормализация концентраций про- и противовоспалительных цитокинов, иммуноглобулинов в секрете эндометрия. Исследователи отметили также более быстрое и стойкое нивелирование эндометрита, что позволило повысить чувствительность к антибактериальной терапии, а также сократить сроки излечивания пациенток. В работе Доброхотовой Ю.Э. и соавт. отмечается, что после успешного применения экзогенной цитокинотерапии у 62,8% женщин диагноз ХЭ был снят, а у оставшихся пациенток он перешел в неактивную стадию [18]. Таким образом, цитокинотерапия является одним из новых эффективных альтернативных способов лечения персистирующего воспаления в эндометрии. Назначение локальных цитокинов является перспективным дополнением к комплексному подходу к лечению ХЭ [1, 5, 14].
Цель исследования: оценка динамики эхографических изменений эндометрия на фоне комплексного лечения ХЭ с применением цитокинотерапии.
Материалы и методы
Проведен ретроспективный анализ ультразвукового исследования 298 женщин репродуктивного возраста, которым диагностирован ХЭ. Основную группу составили 140 пациенток, которым было проведено комплексное лечение, включающее противовоспалительную терапию макролидами последнего поколения с нитроимидазолами; макролидами с цефалоспоринами III поколения; защищенными пенициллинами с макролидами в сочетании с антимикотиками, а также противовирусными и иммуномодулирующими препаратами (аномальные нуклеотиды, интерфероны, гипериммунные и полиспецифические иммуноглобулины). В зависимости от выявленной микрофлоры назначались антипротозойные, комбинированные противомикробные средства или антисептики. В данной группе дополнительно назначался 1 курс цитокинотерапии по 25 ЕД в 1 свече, вводимой во влагалище на ночь, длительностью 20 дней.
Группу сравнения составили 158 женщин, получавших аналогичное противовоспалительное лечение, но без применения экзогенных цитокинов. Все назначения были произведены лечащим врачом в соответствии со стандартами оказания медицинской помощи препаратами, зарегистрированными в Российской Федерации, и действующими инструкциями по медицинскому применению, опубликованными в Реестре лекарственных средств (https://www.rlsnet.ru/).
В исследование не входили пациентки с миомой матки, эндометриозом и патологией придатков.
Исследование было одобрено Этическим комитетом факультета непрерывного медицинского образования РУДН.
Все пациентки подписали информированное согласие на публикацию своих данных.
Возраст пациенток основной группы был 34,7±6,6 года, группы сравнения – 33,5±5,4 года. Клиническая диагностика ХЭ осуществлялась на основании предъявляемых жалоб, данных анамнеза, бимануального исследования, результатов цитологического и гистологического исследования эндометрия после гистероскопии, морфологического и иммуногистохимического исследований эндометрия, полученного при пайпель-биопсии, с типированием плазматических клеток (CD138); при необходимости применяли расширенную панель, включающую моноклональные антитела к антигенам иммунных клеток (CD4, CD8, CD20).
Обследование органов малого таза проводилось в ранней пролиферативной фазе менструального цикла на ультразвуковой системе Affiniti70 (Philips, Нидерланды) трансабдоминальным и трансвагинальным доступом, с последующей объемной реконструкцией в 3D-режиме. Для получения количественных показателей измеряли объем матки, толщину и объем эндометрия, с расчетом скорректированного объема, который является отношением объема эндометрия к объему тела матки, выраженному в процентах [19]. Качественные показатели включали оценку слизистой оболочки полости матки: структуру, эхогенность, характер линии смыкания или расхождения листков слизистой (зияние) полости матки, субэндометриальный контур, наличие различных акустических феноменов.
Статистический анализ
Полученные результаты обрабатывались стандартными статистическими методами с применением программного обеспечения MS Excel V10 и проекта R для статистических вычислений, версия R 4.3.2 (Eye Holes) [20]. Учитывая, что часть данных не подчинялась нормальному распределению, применялись методы непараметрической статистики: определялись медианы (Me) с интерквартильным размахом (Q1–Q3). Дискретные признаки представлены в виде абсолютного числа (n) и относительной величины (%). Гипотезу о равенстве средних проверяли с помощью непараметрического метода U-критерия Манна–Уитни для несвязанных совокупностей. При сравнении двух зависимых групп номинальных данных использовался критерий Мак-Немара с поправкой Йейтса. Различия между статистическими данными рассматривались на уровне значимости не ниже р<0,05.
Результаты
Показатели объема тела матки среди женщин обеих групп до и после лечения значимых различий не имели (р>0,05).
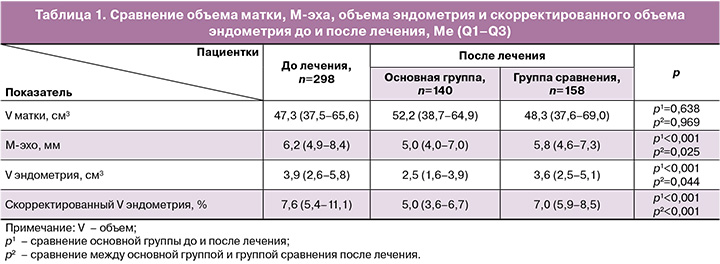
В основной группе на фоне лечения наблюдалось снижение значения толщины эндометрия, и при сопоставлении с группой сравнения уменьшение показателя толщины срединного комплекса оказалось значимым (p<0,05). Объем эндометрия и скорректированный объем как в случае применения цитокина, так и при сопоставлении с группой сравнения после лечения стали существенно меньше (p<0,05) (табл. 1) .
Со стороны эндометрия отмечались изменения как функционального, так и базального слоя. Неоднородная структура и повышенная эхогенность были самыми частыми признаками, типичными для ХЭ (62,8 и 69,1% соответственно). Визуализировались множественные разнокалиберные гипо-/гиперэхогенные включения малого размера правильной и неправильной формы, часть из которых были без акустических феноменов, так и с эффектом реверберации. Следует отметить, что существенных изменений частоты встречаемости неоднородной структуры в основной группе до и после лечения, а также при сопоставлении с группой сравнения не выявлено (p>0,05). Так, среди женщин, применяющих цитокинотерапию, данный признак зафиксирован в 55,0% случаев, а в группе сравнения – в 64,6% (табл. 2).
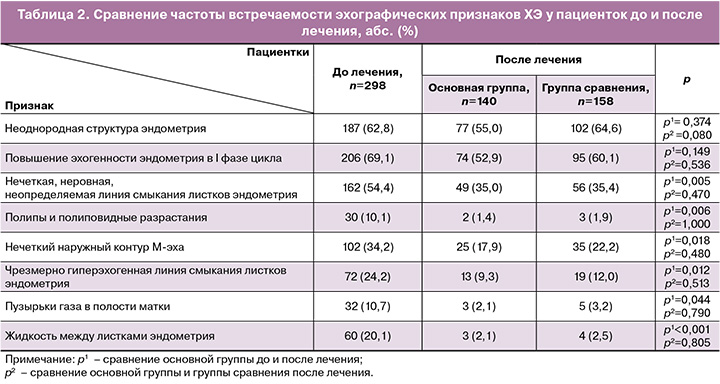
Повышение эхогенности эндометрия после лечения стало встречаться реже, однако статистически значимой разницы при добавлении в лечение цитокинов не получено (p>0,05).
Полиповидные разрастания и полипы, при наличии которых эндометрий становится неоднородным, отмечены до лечения у 10,0% пациенток, а после лечения в основной группе – у 1,4% (p<0,05). После проведенного антибактериального лечения без назначения цитокинов очаговые образования эндометрия, которые могли быть расценены как полипы, наблюдались у 1,9% женщин. Каких-либо закономерностей локализации патологических зон в эндометрии не выявлено. После проведенной терапии 7 пациенток с полипами были направлены на гистероскопию, во время которой произведено удаление очаговых образований с гистологическим диагнозом полипа в 5 (71,4%) случаях и в 2 (28,6%) – описание соответствовало ХЭ без идентификации полипа (табл. 2).
Изменения наружного контура эндометрия до лечения имелись у 34,2% пациенток: он был нечетким, неровным, вплоть до его отсутствия, когда невозможно корректно измерить толщину срединного комплекса матки. После лечения патологическая область проекции базального слоя осталась у половины из этих женщин (p<0,05); но при сопоставлении с группой сравнения статистически значимого улучшения выявлено не было (табл. 2).
Нечеткая, неровная или неопределяемая линия смыкания листков эндометрия до лечения отмечена у 54,4% женщин. После лечения частота встречаемости этого признака статистически значимо снизилась, вне зависимости от проводимой терапии, и составила 35,0% в основной группе (p<0,05). По сравнению с пациентками, получавшими противовоспалительную терапию без локальных цитокинов, изменение срединной линии отмечено в 35,4% случаев, что оказалось статистически незначимо (p>0,05). Аналогичная картина наблюдалась в отношении чрезмерно выраженной, гиперэхогенной срединной линии: до лечения она зафиксирована в 24,2% случаев, после лечения с применением цитокинотерапии – у 9,3% пациенток (p<0,05), без цитокинов – у 12,0%, p>0,05 (табл. 2).
В толще эндометрия, на линии смыкания листков слизистой или в содержимом полости матки у 10,7% больных встречались мелкие гиперэхогенные включения с акустическим феноменом реверберации, что характерно для пузырьков газа. После лечения достоверное улучшение выявлено как в основной группе (2,1%, p<0,05), так и в группе сравнения (3,2%). Влияния цитокинотерапии на исчезновение данного признака не выявило статистически значимого эффекта (p>0,05) (табл. 2).
Расширение полости матки за счет ангипоэхогенного содержимого до лечения наблюдалось у 20,1% пациенток. После терапии, включавшей локальные цитокины, лишь у 2,1% женщин сохранялся этот патологический признак (p<0,05), в группе сравнения – у 2,5%, p>0,05 (табл. 2).
Обсуждение
Особая значимость ХЭ, проявляющаяся его влиянием на женскую репродуктивную систему, сложность диагностики как до лечения, так и результата после лечения, обязывают к разработке новых критериев оценки состояния эндометрия, в том числе и ультразвуковым методом. Накопление научных знаний свидетельствует о том, что противомикробная терапия не всегда приводит к окончательному излечиванию ХЭ, так как после ее проведения с целью элиминации инфекционных агентов через некоторое время может происходить повторная контаминация восходящим и/или лимфогенным путем [21].
Одним из перспективных направлений лечения ХЭ, помимо антибактериальной, противовирусной и гормональной терапии, может стать местная цитокинотерапия, в отдельных исследованиях убедительно показавшая положительные результаты [1, 5, 14–18]. Бесспорным преимуществом использования местной цитокинотерапии являются более короткие сроки купирования персистирующего воспалительного процесса в эндометрии, стойкий эффект после лечения и наступление беременности [14, 15].
В проведенном исследовании была предпринята попытка изучения и сопоставления ультразвуковой картины состояния эндометрия с целью оценки эффективности комплексной противовоспалительной и цитокинотерапии.
ХЭ сопровождается отеком и лимфоидной инфильтрацией, приводя к увеличению толщины и объема эндометриальной ткани. На фоне проведенного лечения происходило более выраженное уменьшение толщины, объема эндометрия и его скорректированного объема при назначении цитокинотерапии, чем среди женщин, получающих стандартный противовоспалительный комплекс.
Характерная для ХЭ неоднородная структура эндометрия после лечения в основной группе стала регистрироваться на 9,7% реже, но статистически значимых изменений в зависимости от вида терапии выявлено не было.
Интересными оказались результаты в случаях диагностики полипов и полиповидных разрастаний. Так, данная патология после лечения обнаружена почти в 3,5 раза реже, чем до лечения. Снижение частоты их встречаемости свидетельствует о том, что не всегда полиповидные образования, определяемые при ультразвуковом исследовании, являются истинными полипами. В связи с этим представляется целесообразным проведение противовоспалительной терапии до назначения гистероскопии с целью полипэктомии, что будет способствовать снижению внутриматочных вмешательств, которые провоцируют ХЭ.
Демидов В.Н. и Гус А.И. описывают утолщенную и гиперэхогенную срединную линию как признак ХЭ, связывая данный феномен со скоплением мелких пузырьков газа в полости матки [22]. Кроме этого, авторы указывают на визуализацию отдельных мелких гиперэхогенных включений с акустическим эффектом реверберации, или «хвост кометы», что также характерно для газа. После проведенного лечения с применением цитокинотерапии частота выявления патологической срединной линии уменьшилась в 2,6 раза. Отдельно расположенные пузырьки газа как в эндометрии, так и в полости матки визуализировались еще реже, то есть в 3 раза, но влияния цитокинов при этом не отмечено.
Наличие жидкости в полости матки Демидов В.Н. и Гус А.И. расценивают как один из наиболее достоверных признаков ультразвуковой диагностики ХЭ [22]. Исчезновение жидкости оказалось наиболее выраженным эффектом вследствие проводимой терапии в основной группе (в 5,6 раза).
Таким образом, результаты исследования после проведенного курса цитокинотерапии свидетельствуют об улучшениях ультразвукового изображения слизистой оболочки полости матки, которые наблюдались почти по всем описанным критериям, характеризующим изменения эндометрия при ХЭ, за исключением неоднородности структуры и повышения эхогенности эндометрия. Кроме показателей толщины, объема эндометрия и его скорректированного объема, отсутствуют существенные различия между показателями в группе пациенток, которым наряду с противомикробными и противовирусными препаратами была добавлена цитокинотерапия, и группой, получавшей аналогичное противовоспалительное лечение без цитокинов. Вместе с тем отмечается тенденция к потенцированию положительного эффекта комплекса, включающего цитокины, на состояние слизистой оболочки полости матки. Вероятно, такой результат связан с недостаточной длительностью применения препарата (продолжительностью 20 дней) в виде разового курса, в то время как Радзинский В.Е. и соавт. [5] отмечают выраженный клинический эффект после 3-месячного лечения, начиная с 5-го дня менструального цикла, а Доброхотова Ю.Э. и соавт. доказали преимущество 40-дневной цитокинотерапии по сравнению с 20-дневной [23]. Второй причиной может быть отмеченное ранее отсутствие полного восстановления структуры эндометрия на фоне лечения ХЭ [9, 24].
Заключение
После одноразового 20-дневного курса применения цитокинотерапии в суппозиториях по 25 ЕД 1 раз в день с целью лечения ХЭ были отмечены улучшения результатов по количественным и качественным ультразвуковым критериям состояния эндометрия. Исчезновение жидкости и пузырьков газа из полости матки оказалось наиболее выраженным эффектом от проводимой терапии. Приближение ультразвуковых характеристик эндометрия к нормативным показателям свидетельствует о частичном восстановлении структуры эндометрия.



