Рецидивирующие неудачи имплантации при использовании вспомогательных репродуктивных технологий у пациенток с нарушением репродуктивной функции, связанным с хроническим эндометритом (ХЭ), наблюдаются в 7,7–67,5% случаев [1, 2]. Эффективность экстракорпорального оплодотворения (ЭКО) у пациенток с ХЭ не превышает 30% за цикл лечения и еще ниже у женщин старше 36 лет [3]. Диагностика ХЭ, его лечение и преодоление бесплодия методом ЭКО сопряжены с увеличением временного интервала до наступления ожидаемой беременности, неблагоприятным влиянием на психоэмоциональное состояние супружеской пары, высокими материальными затратами. Свести к минимуму эти издержки можно, имея информацию о предполагаемом успехе ЭКО перед его выполнением [4]. Однако уже разработанные инструменты для определения предикторов успеха пока не нашли широкого применения в рутинной клинической практике из-за их трудоемкости, низкой прогностической точности и сомнительной клинической полезности.
Так, в систематическом обзоре и метаанализе 22 исследований дана оценка клинического значения толщины эндометрия для исхода ЭКО, и авторы пришли к выводу об отсутствии способности этого показателя прогнозировать беременности и живорождения [5]. В более позднем систематическом обзоре 20 исследований сделан более мягкий вывод: результаты ЭКО у пациенток с нарушением рецептивности эндометрия зависят не только от толщины эндометрия, но и от ряда других факторов риска как в циклах переноса свежего эмбриона, так и криопереноса. Подчеркиваются важность персонализированного подхода с эффективными методами диагностики и лечения для улучшения рецептивности эндометрия, а также необходимость дальнейших исследований для оценки важности толщины эндометрия, протоколов лечения и других факторов [6].
В настоящее время для прогноза вероятности живорождения после 1–3 циклов ЭКО оценены модели, в которых использовались множественные клинические и лабораторные показатели (в одном из исследований – до 100 переменных), а также количество извлеченных ооцитов, которые давали ограниченную точность прогноза менее 60% – AUC от 0,51 до 0,60 [7–10]. Mc Lernon D.J. et al. (2016) дали индивидуальную оценку совокупных шансов пары на рождение ребенка в результате шести последовательных циклов ЭКО, использовав параметры, полученные как до лечения, так и после первого переноса свежих эмбрионов (индекс прогностической ценности для модели до ЭКО составлял 0,73, после первого цикла – 0,72); при этом все характеристики пациентов и лечения по отдельности имели статистически значимую одновариантную связь с живорождением, за исключением необъяснимого бесплодия [11]. Модели, разработанные Xu T. et al. (2022), ограничиваются прогнозированием беременности сразу после цикла ЭКО, но не живорождения, с точностью 68% [12]. Заслуживает внимания исследование, в котором авторы оценили возможность предсказать вероятность живорождения в первом цикле ЭКО до его выполнения, разработав три модели на основании независимого набора данных; при этом модель, включающая АМГ, достигла точности прогноза 71% [13]. Систематический обзор, выполненный в 2020 г., оценил качество 35 моделей прогнозирования ЭКО, отметив как наиболее качественную и информативную модель Маклернона [14].
Однако ориентация на ограниченный объем данных не позволяет использовать весь массив полученных биологических параметров, определить их ценность для прогноза; и поэтому в настоящее время активно внедряются в медицинскую практику модели прогнозирования, основанные на современных алгоритмах, таких как нейронные сети [15]. Несмотря на многообещающие данные, искусственный интеллект (ИИ) пока не получил статус «золотого стандарта», что послужило основанием для систематического обзора 18 исследований, целью которого явилась оценка прогностических возможностей моделей на основе ИИ [16]. Синтез данных этого анализа показал, что такие модели успешно точно предсказывают результат ЭКО в отношении клинической беременности с сердцебиением плода (72%) и живорождения (90%).
VerMilyea M. et al. (2022) применили глубокое машинное обучение (анализ медицинских изображений) для прогнозирования жизнеспособности эмбриона на основе микроскопии; при этом совокупная точность составила 64% как для жизнеспособных, так и для нежизнеспособных эмбрионов, что продемонстрировало надежность модели и ее обобщаемость, превосходящую на 42% результат по сравнению с оценкой эмбриологами [17]. Глубокое машинное обучение описано Mihara M. et al. (2023) для диагностики ХЭ по данным гистологических и иммуногистохимических картин; отмечен потенциал для улучшения диагностики, преодоления разобщенности гистологических и гистероскопических оценок, разработки стандартизированных диагностических критериев и единых клинических рекомендаций для этого заболевания [18].
Вместе с тем научный и практический интерес относительно прогноза беременности/живорождения в результате ЭКО у пациенток с маточной формой бесплодия, обусловленной ХЭ (дефект имплантации яйцеклетки, необъяснимое бесплодие), остается неудовлетворенным; исследования по поиску предикторов успеха этого вмешательства после лечения ХЭ не проводились, и, следовательно, этот вопрос является актуальным для современной репродуктивной медицины.
Цель исследования: разработать с помощью нейросетевой технологии прогностическую модель вероятности наступления клинической беременности и живорождения у женщин с маточной формой бесплодия, обусловленной ХЭ, на этапе отбора в программы ЭКО с криопереносом и оценить ее эффективность.
Материалы и методы
Дизайн – вторичный анализ результатов исследования «Течение и исходы беременности, наступившей в результате ЭКО, у пациенток с ХЭ, получавших комплексное лечение с использованием препарата “Суперлимф” на прегравидарном этапе (рандомизированное контролируемое испытание “ТЮЛЬПАН 2”)» [19].
Материал. Использовали электронную базу данных о 600 пациентках с диагнозом «женское бесплодие маточного происхождения, дефект имплантации яйцеклетки (N97.2), хроническая воспалительная болезнь матки (N71.1)», подтвержденным гистологически и иммуногистохимически, отвечавших критериям включения/исключения, прошедших лечение ХЭ и процедуру ЭКО (криоперенос) с сентября 2019 г. по июнь 2023 г. на базе женской консультации ГБУЗ ТО «Перинатальный центр» (Тюмень, Россия). Лечение ХЭ, проведенное на прегравидарном этапе, включало антибактериальную терапию; гестаген во вторую фазу цикла; комплекс природных антимикробных пептидов и цитокинов. В настоящий анализ из указанной базы отобраны 188 пациенток, имевших полный пакет данных клинического, функционального, лабораторного, гистологического, иммуногистохимического, иммуноферментного исследований и лазерного конверсионного тестирования (спектрометр «Фотон-Био») до и после проведенного лечения (лица с недостающими данными из анализа были исключены). Пациентки были распределены на 2 группы: I (n=102) – у которых в результате ЭКО наступила клиническая беременность; II (n=86) – у которых беременность не наступила.
Основные результаты. Предикторы и модель прогноза беременности/живорождения в результате планируемого ЭКО с криопереносом. Программа персонализированного прогнозирования (онлайн-калькулятор) для оценки индивидуальной вероятности беременности/живорождения у пациенток с ХЭ до выполнения ЭКО.
Статистический анализ
Статистический анализ данных выполняли, руководствуясь принципами Международного комитета редакторов медицинских журналов (ICMJE) и рекомендациями «Статистический анализ и методы в публикуемой литературе» (SAMPL). Статистическая обработка результатов исследования осуществлялась с помощью пакета программ IBM SPSS Statistics Version 25.0 (International Business Machines Corporation, США). Анализ нормальности распределения признаков проводился путем оценки критерия Колмогорова–Смирнова. Учитывая распределение количественных признаков, отличное от нормального в большинстве случаев, полученные данные представлены в виде медианы, первого и третьего квартилей – Me (Q1; Q3). Номинальные данные описывались с указанием абсолютных значений (n) и долей (%). Сравнение независимых показателей между группами проводилось с помощью критерия Манна–Уитни (U), при двухэтапном измерении (до и после лечения) количественных показателей – путем оценки рангового Т-критерия Уилкоксона, который в заключении SPSS автоматически преобразовывался в величину Z (z-score). Сравнение независимых номинальных данных проводилось при помощи критерия хи-квадрат (χ2) Пирсона, при этом в малых выборках применяли поправку на правдоподобие, при количестве наблюдений менее 10 – поправку Йейтса на непрерывность, менее 5 – точный критерий Фишера. Для сравнения двух зависимых групп номинальных данных использовался критерий χ2 Мак-Нимара. Во всех случаях р<0,05 считали статистически значимым при уровнях ошибки первого и второго рода α=5% и β=20% соответственно. Между исследуемыми параметрами корреляционные связи определяли, используя коэффициент Спирмена, силу связи – по шкале Чеддока.
Нейросетевой анализ. Для создания модели прогноза использовали процедуру многослойного персептрона (модуль Neural Networks программы IBM SPSS Statistics V. 25,0 (IBM Corporation, USA)). Статистически значимые параметры были включены в выборки, использованные для обучения (n=188) и тестирования (n=57). Тестовая выборка была сформирована методом Randomize. Диагностическая информативность модели прогноза определена путем ROC-анализа.
Результаты
Общие сведения о пациентках. Возраст пациенток варьировал от 18 до 45 лет, Ме (Q1; Q3)=36,0 (35,1; 36,1) и 36,0 (35,1; 36,1) года в I и II группах соответственно (р=0,89). Социальная и клиническая характеристика пациенток представлена в таблице 1, анализ которой показал отличие между группами по уровню образования, брачному статусу, профессиональным вредностям, методам контрацепции.
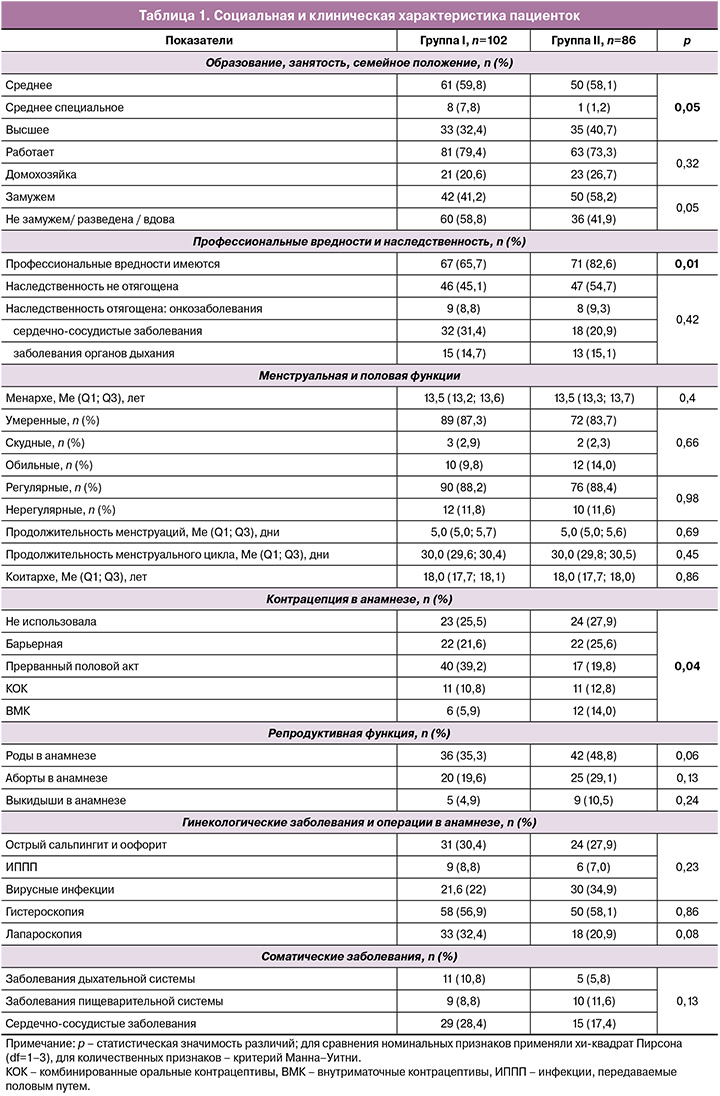
Продолжительность бесплодия до 5 лет была у 78,4% (80/102) и 73,3% (63/86) пациенток, 5 лет и более – у 21,6% (22/102) и 26,7% (23/86) соответственно, р=0,41, и в среднем составила 2,0 (2,0; 3,2) и 2,0 (2,0; 3,3) года соответственно, р=0,51.
Лечение, выполненное в прегравидарном периоде, не имело статистически значимых различий по составу медикаментозных средств – все пациентки получали антибактериальную терапию; гестаген во вторую фазу цикла – 51,0% (52/102) и 55,8% (48/86), р=0,51; комплекс природных антимикробных пептидов и цитокинов – 67,6% (69/102) и 55,8% (48/86), р=0,1 соответственно.
Результаты функциональных и лабораторных методов исследования. Динамика показателей ультразвукового исследования и лазерного конверсионного тестирования представлена в таблице 2.
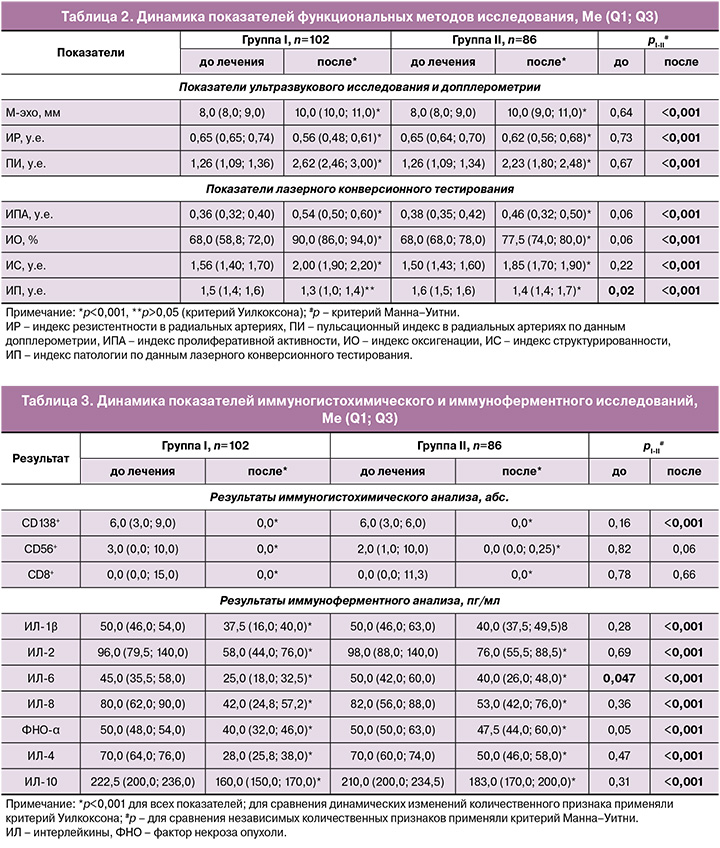
Показатели УЗИ и допплерометрии, равно как и лазерного конверсионного тестирования после лечения, значительно улучшились в обеих группах, но у пациенток I группы отличались статистически значимо в лучшую сторону по сравнению со II.
Аналогичное заключение можно сделать и в отношении результатов иммуногистохимического и иммуноферментного исследований (табл. 3).
Исходы ЭКО
Из числа наступивших беременностей у пациенток I группы живорождением завершились 88,2% (90/102), или от общего количества пролеченных пациенток – 47,9% (90/188). Продолжительность бесплодия у пациенток с благоприятным исходом составляла 1,0 (1,0; 2,7), с неблагоприятным исходом – 2,0 (2,0; 3,3) года (p=0,08). Завершение беременности у пациенток с благоприятным исходом произошло через 39,0 (37,4; 39,0) недели, с неблагоприятным – через 8,0 (7,6; 11,3) недели (p<0,001).
Отсутствие живорождения в I группе (n=12) было связано с самопроизвольным выкидышем до 12 недель в 83,4% (10/12) наблюдений, до 22 недель – в 8,3% (1/12), антенатальной гибелью плода – в 8,3% (1/12). Прочие осложнения беременности (преждевременные роды, преэклампсия, преждевременная отслойка нормально расположенной плаценты, гипоксия и задержка роста плода) встречались в среднем с частой 6,6 и 9,4% наблюдений в I и II группах соответственно, что было статистически сопоставимо (р=0,36).
Оценка состояния новорожденных по шкале Апгар в конце первой минуты у пациенток с благоприятным исходом составляла 8,0 (7,4; 8,0) балла, в конце пятой минуты – 8,0 (7,8; 8,0) балла, вес новорожденных составил 3300,0 (3116,2; 3291,0) г.
Предикторы и модель прогноза беременности/живорождения в результате ЭКО
Учитывая необходимость исключения мультиколлинеарности между коррелирующими параметрами используемых методов исследования, было решено при создании модели прогноза исхода ЭКО у пациенток с бесплодием после лечения ХЭ использовать только наиболее важные параметры (предикторы). Для этой цели была выбрана процедура многослойного персептрона. Число входных нейронов составило 11 единиц, в качестве которых выступали параметры исследования (наличие или отсутствие в структуре лечения комплекса антимикробных пептидов и цитокинов, количественные значения после лечения пульсационного индекса в радиальных артериях, индексов оксигенации, структурированности и пролиферативной активности по данным лазерного конверсионного тестирования, CD138 и цитокинов интерлейкина (ИЛ)-4, ИЛ-10, ИЛ-1β и фактора некроза опухоли (ФНО)-α), имеющие не только значимые различия при сравнении исследуемых групп, но и патогенетическое значение.
Учитывая число входных нейронов, в архитектуру многослойного персептрона было включено 2 скрытых слоя. Автоматический выбор архитектуры позволил вычислить оптимальное количество нейронов в указанных скрытых слоях, равное 8 и 6 соответственно и позволяющее при этом максимально эффективно прогнозировать интересующий исход. Архитектура разработанной нейронной сети представлена на рисунке 1.
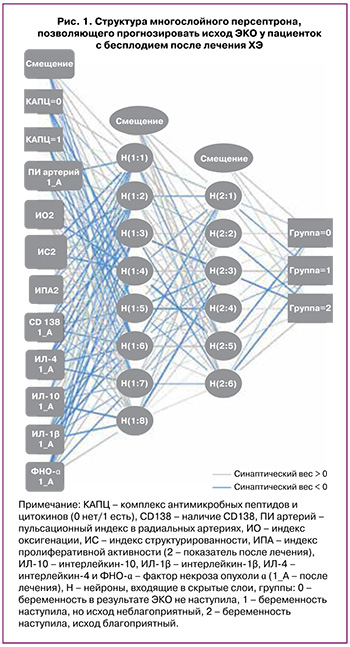
Для создания взаимосвязи взвешенных сумм объектов с последующим слоем значений данных объектов в обоих скрытых слоях и в выходном слое использовался гиперболический тангенс. В качестве функции ошибки выступала сумма квадратов. Выходной слой содержал 3 целевые (зависимые) переменные (0 – беременность в результате ЭКО не наступила, 1 – беременность наступила, но исход неблагоприятный, 2 – беременность наступила, исход благоприятный).
Модуль Neural Networks программы IBM SPSS Statistics использует алгоритм обратного распространения ошибки для обучения нейронной сети. При обучении нейронной сети веса каждого нейрона определяются путем оптимизации функции потерь или стоимости. Алгоритм обратного распространения ошибки основывается на итеративном процессе, в котором веса каждого нейрона на каждом слое обновляются с целью минимизировать ошибку модели. Ошибки вычисляются как разница между прогнозируемыми значениями нейронной сети и реальными значениями. Процесс обновления весов выполняется с помощью метода градиентного спуска, который настраивает значения весов в направлении, противоположном градиенту функции потерь. Это позволяет модели более точно предсказывать зависимую переменную. Таким образом, вес каждого нейрона определяется его важностью в предсказании зависимой переменной и итеративно обновляется в процессе обучения нейронной сети.
Важность изучаемых параметров в структуре разработанной нейронной сети, позволяющей прогнозировать вероятность наступления клинической беременности и живорождения у пациенток с бесплодием и ХЭ, отражена на рисунке 2.
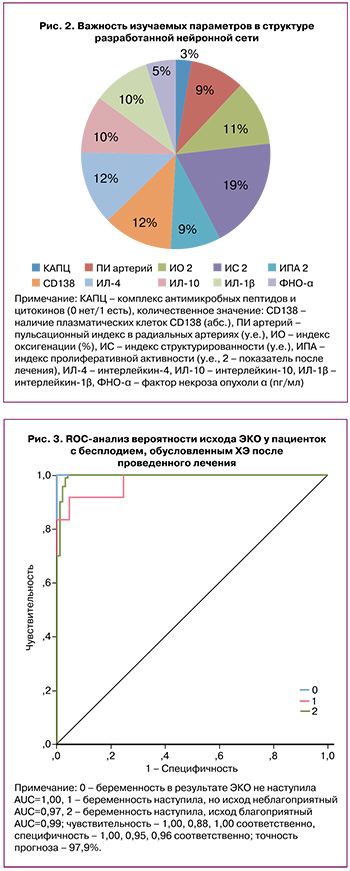
Информативность прогноза. Обращает на себя внимание тот факт, что нейросеть не испытывает трудностей в прогнозе как наступления беременности с благоприятным исходом, так и отрицательного результата применения ЭКО.
Точность прогноза разработанной модели составила 97,9%. Полученная нейронная сеть обладает высокой чувствительностью (100%) и специфичностью (96%) для прогнозирования положительного исхода – наступление клинической беременности и живорождения у пациенток с ХЭ в результате ЭКО. Для беременности с неблагоприятным исходом эти показатели тоже достаточно высоки – чувствительность (88%) и специфичность (95%), однако точность диагностики низкая (66,7%).
Информативность нейросетевого анализа данных в прогнозировании исхода ЭКО у пациенток с бесплодием, обусловленным ХЭ, подтверждена ROC-анализом (рис. 3).
Обращает на себя внимание тот факт, что при исключении из структуры нейронной сети данных лазерного конверсионного тестирования точность прогноза снижается до 94,7%, что определяет его значимую диагностическую роль. Для подтверждения оптимальности выбора исходной архитектуры многослойного персептрона использовали кросс-валидацию, которая позволяет оценить производительность модели с различными параметрами архитектуры. В ходе сравнения моделей было определено, что исходный вариант имеет наиболее высокую точность на всех фолдах.
В процессе тестирования нейронной сети на выборке пациенток, состоящей из 57 человек, процент неверных предсказаний составил 5,3% (3/57).
Таким образом, разработанная прогностическая модель наступления беременности и живорождения после лечения ХЭ у пациенток с нарушением репродуктивной функции с помощью нейросетевой технологии является эффективной с точностью прогноза 97,9%.
Программа персонализированного прогнозирования
Для практических целей была разработана Программа персонализированного прогнозирования (онлайн-калькулятор) для оценки индивидуальной вероятности беременности/живорождения у пациенток с ХЭ до выполнения ЭКО. В данную программу помимо параметров, важность которых подтверждена с помощью нейросетевой технологии, введены еще два – занятость и роды в анамнезе, которые помогают идентифицировать пациенток, у которых наступила беременность, завершившаяся живорождением, от пациенток с неблагоприятным исходом беременности.
Интерфейс программы с вариантами результатов на примере индивидуального прогноза у трех пациенток представлен на рисунке 4.

Таким образом, с помощью данной Программы в рутинной клинической практике врач может принять решение о готовности эндометрия к имплантации яйцеклетки и проведении процедуры ЭКО (при положительном результате тестирования) либо о необходимости проведения дополнительного/-ых курсов лечения ХЭ (при сомнительном или отрицательном).
Обсуждение
Согласно исследованиям последних лет, значимой причиной бесплодия является неспособность эмбриона имплантироваться, причем ХЭ – одна из основных причин, влияющих на этот процесс [20–23]. Существенное влияние на частоту наступления беременности оказывают применяемые методы лечения ХЭ перед проведением ЭКО. Так, этот показатель был значительно выше при использовании антибактериальной терапии, чем в группе без лечения, – 43,2% против 27,3% соответственно [20], комплекса мио-инозитол/фолиевая кислота – 53% против 33% [24], природных антимикробных пептидов и цитокинов в составе комплексной терапии – 57% против 38,7% [19], при внутриматочном введении мононуклеарных клеток периферической крови – OШ=2,35 [25]. Тем не менее около 50% циклов ЭКО остаются безуспешными, что приводит к необходимости проведения повторных курсов лечения ХЭ, новых попыток ЭКО, дополнительным финансовым затратам, что и определяет поиск предикторов успеха ЭКО. Однако модели прогноза у пациенток с различными формами бесплодия не нашли широкого применения ввиду их трудоемкости и недостаточной точности, тогда как исследования в этом направлении у пациенток с ХЭ не проводились.
Наше внимание привлекла возможность использования для этих целей современного метода нейросетевой технологии, который продемонстрировал перспективность в ранее проведенных исследованиях в акушерстве и гинекологии [26–28], в том числе в репродукции и эмбриологии [29–31]. Применение нейросетевой технологии позволило нам выбрать 11 наиболее значимых предикторов успеха ЭКО из 75 параметров, внесенных в электронную базу данных о пациентках.
В отличие от исследования Hansen K.R. et al. [32] и многих других, в которых указывается возраст как важный фактор, определяющий зачатие как в естественных, так и в циклах ЭКО, в настоящем исследовании мы не смогли его выделить в качестве прогностического параметра, поскольку возрастной диапазон пациенток, вошедших в анализ, был очень узок [(Q1; Q3)=(35,1; 36,1) года]. Также параметр «продолжительность бесплодия» оказался не значимым, что не совпадает с мнением других авторов, в том числе с нашим предыдущим исследованием [19, 33–35], что, вероятно, определяется не временным интервалом инфертильности, а излечением ХЭ под влиянием проведенной терапии и восстановлением рецептивности эндометрия.
Выявлена отчетливая связь между разрешением ХЭ (отсутствие плазматических клеток CD138 в строме эндометрия), приемом комплекса природных антимикробных пептидов и цитокинов, гестагена и антибиотика с увеличением шансов наступления беременности и живорождения. Данное наблюдение совпадает с выводами других исследователей о том, что лечение при условии разрешения ХЭ обеспечивает больше шансов для успешного наступления беременности и живорождения в отличие от персистирующего ХЭ [36].
Такие показатели, как пульсационный индекс в радиальных артериях матки по данным допплерометрии, уровни цитокинов в сыворотке крови, параметры, полученные методом лазерного конверсионного тестирования, в качестве предикторов наступления беременности/живорождения в программах ЭКО ранее не изучались. В настоящем анализе они выделены как важные с помощью нейросетевого анализа и являются значимыми с точки зрения патогенеза ХЭ.
Пульсационный индекс отражает уменьшение резерва эндометриального кровотока, что указывается среди причин нарушения репродуктивной функции при ХЭ в систематическом обзоре 2020 г. [37]. Иммунологическая реакция на инфекцию с избыточной локальной продукцией цитокинов у пациенток с ХЭ отражена в большом количестве отечественных и зарубежных исследований последних лет [21–23, 37]. Значение диагностики состояния эндометрия с помощью лазерного конверсионного тестирования с использованием спектрометра «Фотон-Био» в настоящее время активно изучается и дает обнадеживающие результаты [38–40]. Описание метода и клиническое значение параметров, полученных с помощью спектрометра «Фотон-Био», изложены в статье [40].
Таким образом, разработанная нами прогностическая модель наступления беременности и живорождения в результате ЭКО после лечения ХЭ у пациенток с нарушением репродуктивной функции с помощью нейросетевой технологии является уникальным инструментом, позволяющим предсказать успешность лечения с положительным результатом и точностью прогноза 97,9%, что превышает все известные модели, разработанные для вспомогательных репродуктивных технологий.
Заключение
Модель прогноза наступления беременности у пациенток с бесплодием, обусловленным ХЭ, разработанная с помощью нейросетевой технологии, имеет точность прогноза 97,9% и позволяет либо определить необходимость в проведении повторного(-ых) курса лечения ХЭ (при сомнительном/отрицательном показателе успешности наступления беременности/живорождения), либо принять решение о планировании беременности методом ЭКО (при положительном).
Воспользуйтесь калькулятором по ссылке: https://pentcroft.ru/informaciya/kalkulyatory/ishody-eko.-prognoz/



