Хромосомные анеуплоидии представляют собой нарушение количества хромосом. Они вносят значительный вклад в причины детской заболеваемости и смертности. После анеуплоидий половых хромосом наиболее распространены трисомии хромосом 21, 18, 13 [1]. Усовершенствование оказания медицинской помощи пациенткам с многоплодием является крайне актуальной задачей. Только за последние десятилетия показатель родов двойней увеличился примерно на треть: с 9,1 до 12,0 случая на 1000 родов [2]. Столь быстрый рост в основном связан с увеличением числа рождений дизиготных двоен в результате применения вспомогательных репродуктивных технологий (ВРТ) [2, 3]. Хориальность при двойне является одним из важных факторов, определяющих риски анеуплоидий. Например, при дихориальной двойне теоретический риск анеуплоидий для каждого плода вдвое превышает таковой для одноплодной беременности [4, 5]. В 60–70% случаев беременность двойней представлена дизиготными (разнояйцевыми) близнецами, в 20–30% случаев – монозиготными (однояйцевыми) близнецами [6]. При этом статистические данные могут зависеть от возраста матери, способа зачатия, от популяции (особенно при дизиготных двойнях). Дихориальность является обязательным признаком дизиготных двоен; тем не менее до 25% монозиготных двоен также имеют две отдельные плаценты [7, 8].
В связи с тем что точность выявления риска трисомии хромосом 21, 18, 13 с применением комбинированного скрининга I триместра при двойне меньше, чем для одноплодной беременности [9], представляется целесообразным внедрение более надежных методов, каким может являться неинвазивный пренатальный ДНК-скрининг анеуплоидий плода по крови матери (НИПС). В настоящее время НИПС является наиболее чувствительным методом скрининга анеуплоидий хромосом 21, 18, 13, Х и Y [10, 11]. Ранее эффективность применения НИПС при многоплодной беременности была показана в работах многих зарубежных авторов [12, 13]. Huang X. et al. в своей статье указывают на 100% чувствительность и специфичность НИПС для трисомии хромосомы 21, однако для трисомии хромосомы 18 чувствительность составила 50% [14]. Метаанализ, проведенный российскими исследователями в 2021 г., показал выявляемость трисомии хромосом 21 и 18 при беременности двойней, сопоставимую с таковой при одноплодной беременности [15].
В нашем исследовании мы также демонстрируем высокую чувствительность и специфичность выявления трисомии хромосомы 21 при беременности двойней, а в отдельных случаях и возможность применения НИПС при беременности тройней.
Материалы и методы
Дизайн исследования
Было выполнено проспективное наблюдение 90 беременных c многоплодием, которым в период с мая 2018 г. по декабрь 2023 г. в ФГБУ «НМИЦ АГП им. В.И. Кулакова» Минздрава России проводился НИПС. Критерии включения были следующими: (1) беременность двойней; (2) информированное согласие пациентки на проведение исследования; (3) срок беременности ≥10 недель (в исключительных случаях ≥8 недель). В одном случае НИПС проведен пациентке с трихориальной триамниотической тройней.
Критериями исключения были: (1) онкологическое заболевание матери; (2) отсутствие согласия пациентки на проведение исследования.
При выявлении высокого риска хромосомных анеуплоидий проводилось генетическое консультирование; в 4 наблюдениях проведена инвазивная пренатальная диагностика путем амниоцентеза. У беременной тройней забор крови на НИПС проводился одновременно с биопсий ворсин хориона трех плодов. В тех наблюдениях, где был выявлен низкий риск хромосомных аномалий по данным НИПС, проводилось стандартное наблюдение за пациентками. Исходы беременностей собирались по истории родов и при телефонном опросе.
Исследование хориальности
Основным методом определения хориальности являлась ультразвуковая диагностика [16], в ряде случаев хориальность подтверждалась гистологическим исследованием плацент после родов.
Проведение НИПС и анализ результатов
Взятие венозной крови производилось в пробирку с антикоагулянтом ЭДТА в количестве 9,0 мл. Для выделения ДНК использовались наборы Applied Biosystems MagМАХ (Thermo Fisher, США) и VAHTS Serum/Plasma Circulating DNA Kit (Vazyme, КНР). Центрифугирование проводили дважды непосредственно после взятия крови. Сначала при 2000g в течение 10 минут при 4°С, затем отбирали супернатант и центрифугировали при 10 000g в течение 20 минут при той же температуре. Выделение внеклеточной ДНК проводилось с использованием технологии Dynabeads, либо сразу после взятия крови, либо из отцентрифугированной и замороженной при -20°С плазмы. Высокопроизводительное секвенирование осуществлялось с использованием системы NextSeq550 (Illumina, США).
Биоинформатическая обработка результатов производилась с помощью программного обеспечения «АнеуСкрин» («ДНК-Технология», Россия).
Данная работа была одобрена комиссией по этике биомедицинских исследований при ФГБУ «НМИЦ АГП им. В.И. Кулакова» Минздрава России, протокол №13 от 10.12.2015.
Результаты
В ходе проведенного с мая 2018 г. по декабрь 2023 г. исследования НИПС был выполнен 89 беременным двойней и 1 беременной тройней. Средний возраст обследуемых – 34 года (от 22 до 46 лет). Сроки беременности на момент взятия крови составляли от 8 до 26 недель (в среднем – 13 недель 6 дней). В случае обнаружения фракции плодовой ДНК менее 8% взятие крови проводилось повторно через 2 недели. Средняя доля плодовой ДНК у беременных двойней составила 11,2% (от 2,3% до 28,6%). У 5 пациенток при повторном заборе содержание внеклеточной ДНК плода было достаточным для выдачи заключения. У 6 пациенток при повторном заборе фракция плодовой ДНК составила менее 8%, было рекомендовано генетическое консультирование. У 1 пациентки повторный забор крови не производился.
В 61 случае диагностирована дихориальная диамниотическая двойня, в 28 случаях – монохориальная диамниотическая двойня. В 46,6% (42/90) случаев беременность наступила самопроизвольно, в 53,3% (48/90) – с применением ВРТ.
12 беременных были направлены на НИПС в связи с изменениями сывороточных маркеров РАРР-А (ассоциированный с беременностью протеин А) и β-ХГЧ (бета-субъединица хорионического гонадотропина) по данным пренатального скрининга в I триместре. У 8 беременных имелось увеличение толщины воротникового пространства у одного из плодов (выше 95 процентиля). 5 беременных были направлены на НИПС в связи с другими ультразвуковыми маркерами хромосомной патологии плода (гипоплазия носовой кости, реверсный кровоток в венозном протоке, киста и единственная артерия пуповины). У 3 беременных имелось сочетание ультразвуковых и биохимических маркеров, у 2 беременных – структурные аномалии развития одного из плодов.
Случаи с высоким риском и исходы беременностей
У 3 пациенток с дихориальной диамниотической двойней забор крови на НИПС проводился перед проведением инвазивной диагностики. Показанием для раздельного амниоцентеза был высокий риск трисомии хромосомы 21 по данным пренатального скрининга в I триместре беременности. По данным исследования амниотической жидкости методом количественной флуоресцентной полимеразной цепной реакции во всех 3 случаях у одного из плодов выявлена трисомия хромосомы 21, в связи с чем по желанию пациенток проведена селективная редукция плода с хромосомной патологией, впоследствии родились 3 фенотипически здоровых ребенка. В 1 случае НИПС проведен в связи с увеличением толщины воротникового пространства одного из плодов у пациентки с дихориальной диамниотической двойней; установлен высокий риск трисомии хромосомы 21 у одного из плодов. От проведения инвазивной диагностики пациентка воздержалась; впоследствии родились фенотипически здоровый ребенок и ребенок с трисомией хромосомы 21, подтвержденной цитогенетическим исследованием кариотипа. В 1 случае у пациентки с монохориальной диамниотической двойней и высоким риском трисомии хромосомы 21 по данным НИПС в сроке 19 недель произошла антенатальная гибель одного из плодов, в связи с чем амниоцентез был проведен только одному плоду из двойни; выявлен нормальный кариотип плода, впоследствии произошли роды фенотипически здоровым ребенком.
У пациентки с трихориальной триамниотической тройней первое взятие крови на НИПС проведено в сроке 9 недель 4 дня перед проведением биопсии ворсин хориона. По результату инвазивной пренатальной диагностики у 1-го и 2-го плодов выявлен нормальный мужской кариотип (46,ХY, 9ph-гетерохроматиновый район на 9-й хромосоме – вариант нормального полиморфизма); у 3-го плода выявлена трисомия по хромосоме 21 (47,ХХ,+21). По данным НИПС установлен высокий риск трисомии хромосомы 21. При динамическом наблюдении по данным ультразвукового исследования в сроке беременности 12 недель 3 дня выявлены прогрессирующая дихориальная диамниотическая двойня и спонтанная редукция аномального плода. Повторный забор крови пациентки на НИПС в этом сроке гестации также показал высокий риск трисомии хромосомы 21. Полученные результаты свидетельствуют о наличии эффекта «исчезающего близнеца», так как на момент повторного забора прогрессировала беременность двумя здоровыми плодами мужского пола. Беременность завершилась в сроке 34 недели 4 дня рождением фенотипически здоровых мальчиков (таблица).
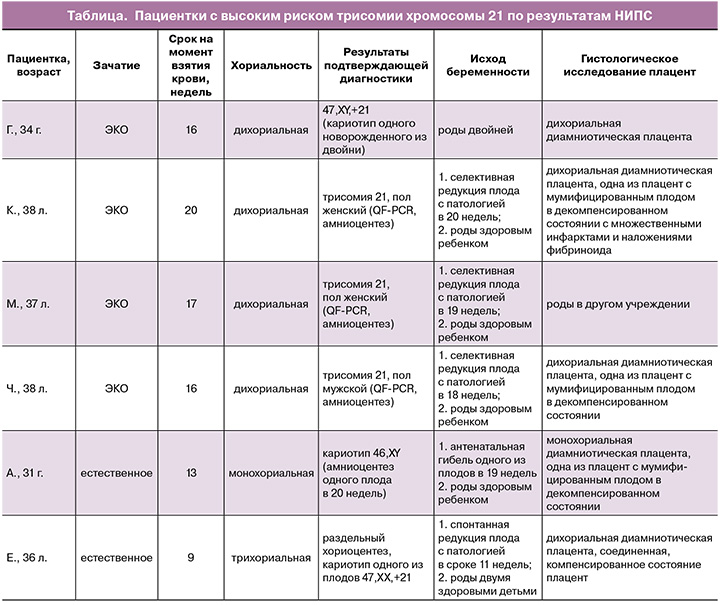
Случаи с низким риском анеуплоидий по хромосомам 21, 18, 13 по данным НИПС и исходы беременностей
Из 84 беременных с низким риском анеуплоидий 21, 18, 13 по данным НИПС 7 беременностей на момент написания статьи пролонгировались. У 2 пациенток с дихориальной диамниотической двойней после сдачи НИПС и получения результата диагностирована несостоявшаяся двойня (в сроке 11 недель и 14 недель). У 2 беременных с дихориальной диамниотической двойней диагностирована антенатальная гибель одного из плодов в сроке 16 и 18 недель. У 2 беременных с монохориальной диамниотической двойней диагностирована антенатальная гибель одного из плодов в сроке 22 недели. У 1 пациентки с дихориальной диамниотической двойней произошел самопроизвольный выкидыш в сроке 18 недель. У 4 пациенток с монохориальной диамниотической двойней беременность осложнилась развитием фето-фетального трансфузионного синдрома и прерыванием беременности в 2 случаях в сроке 16 недель и в 1 случае – в сроке 21 неделя; в 1 случае после фетоскопии, коагуляции сосудистых анастомозов плаценты произошла антенатальная гибель одного из плодов в 20 недель беременности. У 73 пациенток родились дети без фенотипических признаков трисомии хромосом 21, 18, 13.
Обсуждение
В опубликованных в 2016 г. российских клинических рекомендациях по НИПС многоплодная беременность являлась противопоказанием к его проведению [17]. Однако более низкая чувствительность и специфичность обнаружения трисомий хромосом 21, 18 и 13 при проведении комбинированного скрининга беременным двойней в сравнении с одноплодной беременностью [18, 19] диктует необходимость внедрения в практику более точных современных методов. Кроме того, нельзя не учитывать, что риск невынашивания беременности после инвазивной манипуляции при беременности двойней выше, чем при одноплодной беременности [20, 21].
В 2020 г. возможность применения НИПС при многоплодной беременности была отражена в клинических рекомендациях ряда стран и международных сообществ [22–24]. Накопленный нами опыт также демонстрирует возможность применения НИПС при многоплодной беременности, что требует пересмотра отечественных рекомендаций.
В опубликованном в 2019 г. систематическом обзоре 997 беременностей двойней авторы показали высокую точность и низкую вероятность ложноположительных результатов для трисомии хромосомы 21 – 98,2 и 0,05% соответственно (при доверительном интервале 95%) [25]. В дальнейшем аналогичные результаты были продемонстрированы другими лабораториями [26, 27].
В нашей работе мы показали практически 100% чувствительность и специфичность обнаружения трисомии хромосомы 21 по результату НИПС при многоплодной беременности, однако количество наблюдений было ограничено. У 3 беременных с дихориальной диамниотической двойней и трисомией хромосомы 21 у одного из плодов (подтвержденной по данным раздельного амниоцентеза) НИПС выявил высокий риск трисомии хромосомы 21. Также высокий риск трисомии хромосомы 21 был выявлен в случае дихориальной диамниотической двойни, завершившейся рождением ребенка с трисомией хромосомы 21, подтвержденной кариотипированием периферической крови.
В 1 случае монохориальной диамниотической двойни после выявления высокого риска по НИПС произошла антенатальная гибель одного из плодов. В связи с этим амниоцентез был проведен только одному плоду из двойни и показал нормальный результат. В данном случае, несмотря на предполагаемое происхождение близнецов из одной зиготы, объяснением возможной дискордантности по набору хромосом у плодов могло служить явление мозаицизма. К сожалению, нам не удалось подтвердить данное предположение в связи с недоступностью плаценты после родов.
У беременной с трихориальной триамниотической тройней трисомия хромосомы 21 у одного из плодов обнаружена при раздельном хориоцентезе. В этом случае НИПС, проведенный перед инвазивным вмешательством, а также после спонтанной редукции плода с патологией, выявил высокий риск трисомии хромосомы 21.
У 73 беременных с низким риском анеуплоидий хромосом 21, 18, 13 по данным НИПС родились фенотипически здоровые дети.
По нашим наблюдениям, средняя доля плодовой ДНК у беременных двойней составила 11,2%, т.е. у большинства женщин она превышает 8,0%.
Необходимо упомянуть, что, несмотря на низкую долю ложноположительных результатов, в случае обнаружения высокого риска трисомии хромосомы 21 при многоплодной беременности, как и в случае одноплодной беременности, показано генетическое консультирование для решения вопроса о проведении инвазивной диагностики. Дополнительно консультация генетика целесообразна для беременных с низкой фетальной фракцией, так как в этих случаях также может быть предложено проведение инвазивной диагностики [28].
Сравнительно мало информации доступно в литературе в отношении эффективности НИПС для обнаружения трисомий хромосом 18 и 13 при многоплодной беременности, в значительной степени в связи с их меньшей распространенностью. В нашем исследовании анеуплоидии по хромосомам 18 и 13 не наблюдались. Тем не менее оба синдрома имеют более выраженные фенотипические признаки и хорошо диагностируются при ультразвуковом исследовании. Учет нарушений по половым хромосомам при многоплодной беременности не рекомендован в большинстве стран.
Также хотелось отметить, что в связи с повышенными акушерскими рисками в случае беременности двойней проведение НИПС целесообразно на раннем сроке (начиная с 10 недель).
Заключение
В результате нашего исследования у 83 из 89 беременных двойней и одной беременной тройней был получен достоверный результат по данным НИПС. Для большинства пациенток очевидно клиническое преимущество НИПС: в первую очередь снижение обеспокоенности рождением больного ребенка, а также возможность воздержаться от проведения инвазивной диагностики, а следовательно, связанных с ней осложнений.
На основании опубликованных ранее исследований и собственных данных НИПС обладает высокой точностью в отношении трисомии хромосомы 21 и может быть предложен всем беременным двойней, начиная с 10 недель беременности. Требуются дальнейшие исследования для определения точности НИПС при беременности тремя и более плодами.



