Известно, что в последнее время частота преиндукции/индукции родов в мире имеет тенденцию к увеличению [1–3]. Однако, несмотря на широкую распространенность данной процедуры, все еще остается большое количество вопросов, по которым нет согласия в научной литературе.
Неоспоримым фактом снижения акушерских и неонатальных осложнений является успешная подготовка женского организма к родам, осуществляемая за счет различных механизмов инициации родовой деятельности. В основе этих механизмов, объединяющих воспалительную реакцию в миометрии, передачу сигналов от плода и физиологическое старение плодных оболочек, лежат процессы и сигнальные пути, скоординированная регуляция которых осуществляется посредством микроРНК (мкРНК, miR).
МкРНК являются малыми эндогенными некодирующими молекулами длиной примерно 18–22 нуклеотида, регулирующие экспрессию генов на посттранскрипционном уровне [4, 5], а способность секретироваться в составе внеклеточных микровезикул, апоптотических телец и экзосом позволяет им выступать в роли медиаторов межклеточных взаимодействий [6–9]. Ранее было показано изменение экспрессии во время инициации родовой деятельности в миометрии у членов семейства miR-200 (miR-200b/200a/429, miR-141/200c) [7], miR-199a-3p/miR-214 [7, 9, 10], miR-181 (miR-181a, miR-181b, miR-181c и miR-181d), играющих важную роль в регуляции воспалительных реакций в различных типах клеток [11, 12], а также miR-144 [13]. В ряде работ представлена роль miR-143 [14], miR-34b/с и miR-33 в качестве потенциальных участников в гормональном контроле, регуляции покоя и сократимости миометрия во время беременности и родов [15]. Однако мы не встретили в литературе данных по исследованию экспрессии мкРНК при преиндукции родов.
Принимая во внимание вышеизложенное, с использованием базы данных miRTarBase 9.0 мы осуществили поиск и последующий выбор мкРНК, вовлеченных в механизмы инициации родовой деятельности и регуляцию экспрессии ряда ключевых генов, в частности транскрипционного фактора NFKB1, белка сурфактанта легких SFTPA1, простагландинсинтазы (циклооксигеназы) PTGS2, прогестеронового рецептора PGR, с целью оценки экспрессии выбранных мкРНК у матери и плода в качестве циркулирующих и тканевых сигнальных молекул инициации родов при подготовке шейки матки к родам (преиндукции родов).
Материалы и методы
Формирование клинических групп пациентов
Проведено пилотное проспективное исследование с участием 22 беременных женщин, находящихся под наблюдением в ФГБУ «НМИЦ АГП им. В.И. Кулакова» Минздрава России.
В качестве критериев включения для основной и контрольной групп рассматривали следующие: возраст женщин от 18 до 45 лет, одноплодная беременность, головное предлежание, доношенный срок беременности, «незрелые» родовые пути, преиндукция родов, спонтанное начало родовой деятельности (физиологическая готовность к родам), показания к кесареву сечению в плановом порядке (отсутствие готовности к родам). В исследование не были включены женщины с многоплодной беременностью, наличием тяжелых экстрагенитальных заболеваний, осложнениями беременности (преэклампсия, HELLP-синдром, антифосфолипидный синдром), пороками развития плода.
Выборка беременных женщин, включенных в исследование, была разделена на 2 когорты: «роды без преиндукции» (когорта I, n=10) и «преиндукция родов» (когорта II, n=12). Когорта I была разделена на группы: беременные со спонтанными родами (группа Ia, n=5) и беременные, которым проводили плановое кесарево сечение до начала родовой деятельности (группа Ib, n=5). В когорту II вошли беременные с положительным эффектом от преиндукции (группа IIa, n=5) и беременные с отсутствием такового (группа IIb, n=7) (рис. 1).
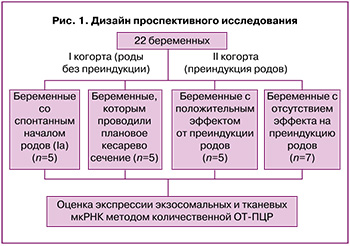
Пациенткам когорты II преиндукцию и последующую индукцию родов проводили согласно клиническим рекомендациям «Неудачная попытка стимуляции родов (подготовка шейки матки к родам и родовозбуждение)» 2021 г. [3].
Подготовку родовых путей к родам начинали при «незрелой» шейке матки (от 0 до 5 баллов по шкале Бишоп); родовозбуждение проводили при достижении «зрелых» родовых путей (от 8 баллов по шкале Бишоп и выше).
С целью преиндукции использовали прием одной таблетки мифепристона 200 мг. В случае «ответа» на преиндукцию в виде достижения степени зрелости родовых путей 8 баллов и выше по шкале Бишоп либо появления регулярной родовой деятельности в течение 24 ч данную категорию женщин относили к Ia группе; при отсутствии данного эффекта – к группе IIb.
Проведение исследования одобрено Этическим комитетом ФГБУ «НМИЦ акушерства, гинекологии и перинатологии». У всех пациенток было получено информированное добровольное согласие в письменном виде.
Получение экзосом из плазмы крови беременных и пуповинной крови плода
Забор венозной материнской крови производился для контрольной группы однократно – при госпитализации, для основной группы – дважды: перед преиндукцией родов и после индукции родов. Забор пуповинной крови из артерии и вены пуповины проводили во время операции кесарева сечения между двумя зажимами, наложенными на пуповину. Образцы крови собирали в пробирки VACUETTE, содержащие ЭДТА (BectonDickinson). Цельную кровь центрифугировали при 300×g, 4°С в течение 20 минут, затем отобранную плазменную фазу центрифугировали при 16000×g в течение 10 минут. Супернатант, не задевая осадка, переносили в чистую пробирку. Для получения экзосом из 0,5 мл плазмы крови использовали набор miRCURY Exosome Serum/Plasma Kit (Qiagen, Германия) в соответствии с инструкциями производителя. Хранение образцов экзосом перед этапом выделения и оценки экспрессии мкРНК осуществляли при температуре -75°С.
Выделение мкРНК из экзосом
Для выделения мкРНК использовали 200 мкл суспензии полученных экзосом, к которым добавляли QIAzol Lysis Reagent (1 мл) и хлороформ (200 мкл) с последовательными инкубациями. После чего центрифугировали при 12 000 g (+4◦C) в течение 15 минут. Отбирали до 600 мкл водной фазы в чистую пробирку и проводили последующее выделение мкРНК набором miRNeasy Serum/Plasma kit (Qiagen, Германия) с использованием автоматической станции QIAcube (Qiagen).
Выделение суммарной РНК из ткани миометрия и плодных оболочек, обогащение фракцией мкРНК
Забор образцов ткани миометрия (взятых из верхней части разреза на матке в нижнем маточном сегменте) и плодных оболочек осуществляли в ходе операции кесарева сечения не позднее 10 минут после родоразрешения. Образцы помещали в криопробирку и погружали в жидкий азот, в котором транспортировали для дальнейшего хранения при температуре -75°С.
Образец ткани гомогенизировали в QIAzol Lysis Reagent для дальнейшего выделения суммарной РНК из 5–10 мг ткани набором miRNeasy Micro Kit (Qiagen, Германия) с последующим обогащением низкомолекулярной фракцией мкРНК (RNeasy MinElute Cleanup Kit, Qiagen, Германия) с использованием автоматической станции QIAcube (Qiagen). Все процедуры проводили в соответствии с протоколами фирмы-производителя. Проверку качества выделенных образцов проводили на биоанализаторе Agilent 2100 (Agilent Technologies) с помощью набора RNA 6000 Nano Kit, а концентрацию измеряли на флуориметре Qubit 3.0 (Invitrogen). Образцы, входящие в диапазон соотношений молярных концентраций рибосомальных РНК (28S и 18S), равный 1,5–1,8, использовали для дальнейшего исследования.
Количественная полимеразная цепная реакция с обратной транскрипцией в режиме реального времени
С использованием реакционной смеси (miRCURY LNA RT Kit, Qiagen) проводили конвертацию мкРНК из каждого образца в кДНК. В качестве внутреннего контроля эффективности синтеза кДНК и количественной полимеразной цепной реакции (ПЦР) в режиме реального времени использовали UniSp6 RNA Spike-in в соответствии с протоколом производителя. Для определения уровня экспрессии мкРНК в ткани миометрия, плодных оболочек и экзосом, выделенных из плазмы крови матери и пуповинной крови плода, проводили количественную ПЦР в реальном времени (miRCURY LNA SYBR Green PCR Kit, Qiagen) и праймеров miRCURY LNA miRNA PCR Assay, специфичных для исследуемых мкРНК: hsa-let-7b-5p (00204750), hsa-miR-9-5p (00204513), hsa-miR-26b-5p (00204172), hsa-miR-92a-3p (00204258), hsa-miR-146a-5p (00204688), hsa-miR-181a-5p (00206081), hsa-miR-301b-3p (00204390), hsa-miR-454-3p (00205663), hsa-miR-548g-5p (02114059). Реакцию проводили в амплификаторе StepOnePlus (Applied Biosystems, США). Сравнение уровня экспрессии мкРНК в образцах относительно референсной молекулы (UniSp6 RNA Spike-in) проводили с использованием метода 2(-ΔΔСТ) [16].
Статистический анализ
Статистическую значимость различий уровня экспрессии мкРНК в исследуемых группах оценивали с помощью теста Уилкоксона–Манна–Уитни с использованием скриптов, написанных на языке R (https://www.R-project.org/). Для оценки связи экспрессии мкРНК с клиническими показателями беременных женщин использовали метод непараметрической ранговой корреляции Спирмена. В случае ненормального распределения параметр описывался как медиана (Me) и квартили Q1, Q3 в формате Me (Q1; Q3).
Результаты
Попарное сравнение в группах показало, что до индукции в группе IIa уровень экспрессии miR-181a-5p в экзосомах матери был значимо выше, чем в группе IIb (р=0,03) (рис. 2).
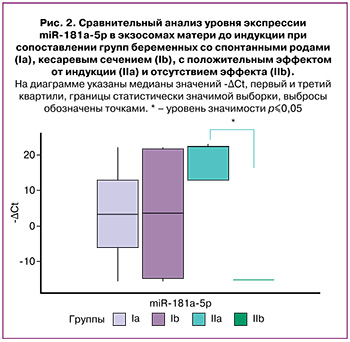
Уровень экспрессии экзосомальной miR-92a-3p в пуповинной крови (артерия пуповины) был выше, чем в крови беременных, взятой до индукции, как в группе IIa (р=0,009), так и IIb (р=0,03). При этом отмечен более высокий уровень экспрессии miR-181a-5p в экзосомах пуповинной крови относительно крови беременных, полученной до индукции в группе IIb (р=0,01) (рис. 3, табл. 1).
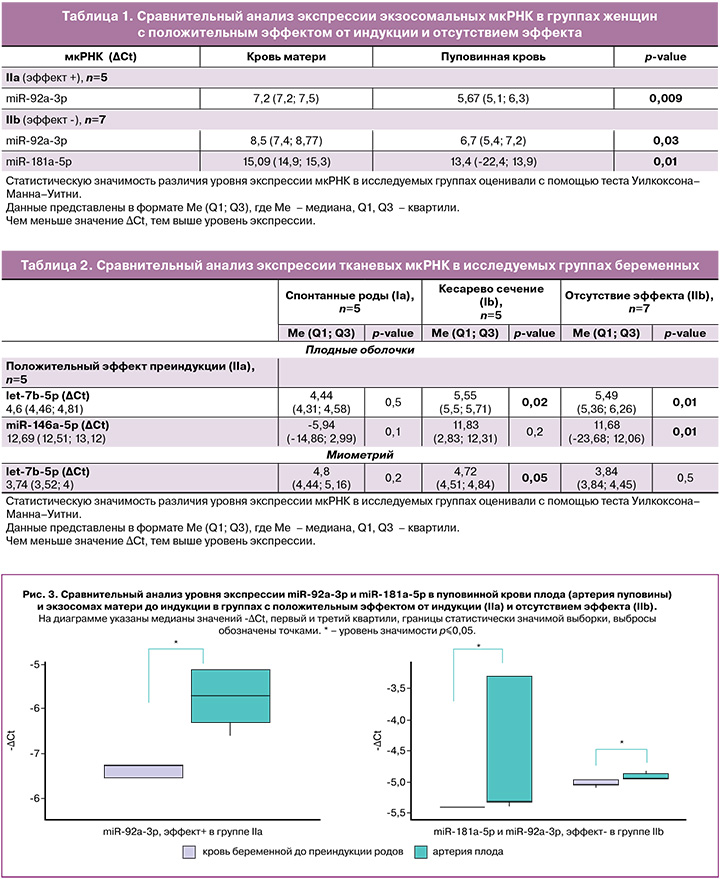
Экспрессия других мкРНК не показала значимых изменений в экзосомах. Однако интересно, что некоторые из них, в частности miR-454-3p и miR-548g-5p, были обнаружены только в образцах пуповинной крови, но не в крови женщин. Следует отметить, что данные мкРНК регулируют экспрессию белка сурфактанта легких SFTPA1. По всей вероятности, отсутствие их экспрессии в крови беременных может быть связано с их секрецией плодом.
Сравнительную оценку экспрессии тканевых мкРНК, выделенных из плодных оболочек и миометрия, проводили в тех же группах. Анализ попарного сравнения выявил значимо более высокий уровень экспрессии let-7b-5p в плодных оболочках в группе IIa относительно группы Ib (р=0,02) и группы IIb (р=0,01) (рис. 4А). При этом в миометрии экспрессия let-7b-5p также значимо выше в группе IIa по сравнению с группой Ib (р=0,05) (рис. 4Б, табл. 2).
Кроме того, экспрессия miR-146a-5p в плодных оболочках у беременных группы IIa была значимо ниже, чем в группе IIb (р=0,01) (рис. 5).
В целом у беременных с положительным эффектом преиндукции родов уровень экспрессии let-7b-5p в плодных оболочках и миометрии выше, чем у беременных с его отсутствием и беременных, которым не проводилась преиндукция.
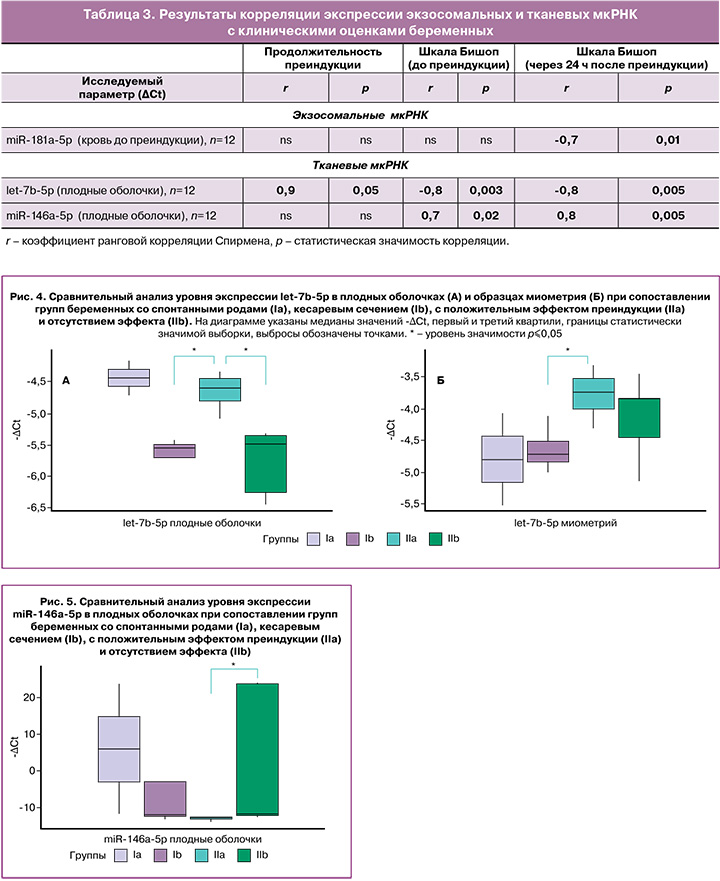
Учитывая выявленные изменения, мы оценили взаимосвязь экспрессии экзосомальных и тканевых мкРНК с клиническими показателями в группах беременных с использованием метода непараметрической ранговой корреляции Спирмена (табл. 3).
Для корреляционного поиска мы объединили исследуемые группы. Основными клиническими показателями, с которыми были установлены значимые корреляции, явились оценка степени зрелости шейки матки и срок начала индукции.
Представленность экзосомальной miR-181a-5p в крови беременных до индукции ассоциирована с увеличением балльной оценки по шкале Бишоп через 24 ч после индукции (r=-0,7; p=0,01). В плодных оболочках повышенная экспрессия let-7b-5p ассоциирована с оценкой по шкале Бишоп до индукции (r=-0,8; p=0,003), с увеличением баллов оценки через 24 ч после нее (r=-0,8; p=0,005) и уменьшением продолжительности преиндукции (r=0,9; p=0,05). Низкая экспрессия miR-146a-5p в плодных оболочках также коррелировала с увеличением оценки по шкале Бишоп (r=0,7, p=0,02; r=0,8, p=0,005 соответственно).
Обсуждение
МкРНК регулируют экспрессию белка на посттранскрипционном уровне посредством взаимодействия с генами-мишенями. Причем, каждая мкРНК обладает способностью потенциально регулировать сотни генов, оказывая, таким образом, широкое влияние на глобальную экспрессию белка.
Скоординированный интерфейс между фетоплацентарной и материнской системой представляет собой сложный многомерный массив тканей и циркулирующих факторов, который включает развивающийся плод, плаценту, децидуальную оболочку и сердечно-сосудистую систему матери [17]. Взаимодействие осуществляется посредством внеклеточных везикул (экзосомы, микровезикулы, апоптотические пузырьки), которые секретируются различными типами клеток, несут определенный груз (белки, липиды, транскрипты мРНК), а также имеют способность модулировать функцию клеток-мишеней и обладают терапевтическим потенциалом [18–21]. Изменения в экспрессии циркулирующих мкРНК могут оказывать влияние на гены, находящиеся в клетках, удаленных от места и типа клеток, в которых они экспрессируются. Menon R. et al., используя глубокое секвенирование, охарактеризовали изменения в экспрессии экзосомальной мкРНК, циркулирующей в материнской крови при доношенной беременности и преждевременных родах. Высокоэкспрессирующиеся мкРНК были связаны с воспалением и клеточным движением при доношенной беременности. Кроме того, данные показали, что экзосомы несут специфический набор мкРНК, который зависит от гестационного срока [22]. Мы не встретили данных литературы по изучению экспрессии экзосомальных мкРНК при индукции родов. В этой связи была оценена экспрессия экзосомальных мкРНК в крови матери накануне спонтанных родов, до и после индукции родов, а также пуповинной крови плода. Следует подчеркнуть, что критерии выбора мкРНК для изучения были основаны на регуляции ими ключевых генов, вовлеченных в механизмы передачи воспалительных сигналов, способствующих началу родовой деятельности.
Уровень экспрессии miR-181a-5p в экзосомах до начала индукции родов был выше у беременных с положительным эффектом, в отличие от беременных с отсутствием эффекта от индукции. Накопленные данные подтверждают вовлеченность семейства miR-181 в модуляцию воспалительных путей в различных типах клеток [12, 23, 24]. Gao L. et al. провели исследование, продемонстрировавшее, что экспрессия miR-181a в миометрии снижается на поздних сроках беременности по мере увеличения ее провоспалительных мишеней (фактор некроза опухоли (TNF-α), c-Fos и эстрогеновый рецептор (ERα)) и на фоне повышенной передачи сигналов эстрадиола-17β/ERα [12]. Наше исследование не выявило изменения экспрессии miR-181a-5р в миометрии, однако ее повышенная экспрессия в экзосомах беременных может являться отражением тканевых процессов. Если при репрессии miR-181a-5р, опосредованной повышенной продукцией эстрогена, инициируется серия провоспалительных путей, приводящих к началу родовой деятельности, то в экзосомах беременных до индукции наблюдается обратная картина – повышение ее экспрессии, вследствие чего запуска воспалительных реакций не происходит. Еще одной из доказанных мишеней miR-181a-5р является HMGB1, который входит в состав DAMP, молекул эндогенного происхождения, связанных с повреждением, и индуцирует воспалительную реакцию [25]. Как сообщалось ранее, HMGB1 может связываться с рецептором TLR4/RAGE нижестоящего пути NFKB, инициируя воспаление [26], а miR-181a-5p ослабляет воспалительную реакцию клеток путем прямого ингибирования HMGB1. Таким образом, повышенная экспрессия miR-181a-5p может создавать некий блок для инициации воспалительной реакции. Но весьма интересно, что у беременных с отсутствием эффекта на индукцию наблюдается как раз снижение ее экспрессии в крови до начала индукции. Следовательно, в этом случае запуску воспалительного каскада ничего не должно препятствовать. Однако, несмотря на это, такие беременные сложно отвечают на индукцию. Мы предполагаем, что, по всей вероятности, инициация воспалительных реакций для начала родовой деятельности у таких беременных не ограничивается запуском классического воспалительного пути. В него могут быть вовлечены другие мкРНК и мишени, или воспаление может развиваться по неканоническому пути.
Сигналы воспалительной реакции, ведущей к родам в срок, исходят как от матери [27], так и от плода [28, 29]. Следует отметить, что как у беременных с положительным эффектом от преиндукции, так и с отсутствием эффекта экспрессия экзосомальной miR-92a-3p значимо повышена в пуповинной крови плода относительно крови беременных, взятой до индукции. Рядом исследований описана роль miR-92a-3p, которая опосредует реакции воспаления, способствуя секреции TNF-α и интерлейкина-1β макрофагами через NFKB-сигнальный путь [30–32]. Интересно, что при этом экспрессия miR-181a-5p снижена в крови беременных, взятой до преиндукции. Следовательно, в этом случае воспалительный сигналинг может быть опосредован как матерью, так и плодом. Таким образом, от скоординированной передачи воспалительных сигналов, которая модулируется, в том числе, экспрессией miR-181a-5р и miR-92a-3p, может зависеть успех проводимой индукции.
На протяжении большей части беременности состояние покоя миометрия поддерживается повышенными циркулирующими уровнями прогестерона (P4), который действует через ядерный рецептор прогестерона (PR). Этот эффект передачи сигналов P4–PR частично опосредован его противовоспалительным действием, способностью подавлять экспрессию генов, кодирующих провоспалительные цитокины (интерлейкин-1, -6, -8, хемокины), и белков, ассоциированных с сокращением, таких как OXTR, GJA1 и PTGS2. Передача сигналов также блокирует активацию NF-kB путем увеличения экспрессии IkBa – ингибитора NF-kB. И напротив, повышенная экспрессия провоспалительных генов опосредуется передачей сигналов эстрадиолу-17β и ERα, которые снижают функцию PR, тем самым еще больше усиливая воспалительную реакцию, что в конечном итоге приводит к родам [33]. Следовательно, мкРНК могут являться гормонально модулируемыми медиаторами экспрессии генов, поддерживающими баланс между противовоспалительными и провоспалительными сигнальными путями [33].
В этой связи, с учетом изменения экспрессии мкРНК в экзосомах до преиндукции и пуповинной крови плода, мы оценили профиль тканевых мкРНК, выделенных из плодных оболочек и миометрия беременных на момент родов. В гестационных тканях выявлено изменение экспрессии let-7b-5p, относящейся к семейству let-7. Последнее рассматривается в качестве основного регулятора фундаментальных клеточных процессов, включая дифференцировку, плюрипотентность, пролиферацию, инвазию и миграцию, а также играет важную роль в имплантации, плацентации и росте плода [34]. При анализе выявлено значимое повышение уровня экспрессии let-7b-5p в плодных оболочках у беременных с положительным ответом на преиндукцию относительно беременных, которым проводили кесарево сечение без индукции, и беременных с отсутствием ответа. При этом в миометрии экспрессия let-7b-5p не показала значимой разницы между группами с наличием и отсутствием ответа. Однако она была также повышена относительно интактного миометрия. Следует отметить, что потенциальными мишенями let-7b-5p, среди прочих, являются NF-kB и PTGS2. Интересно, что Chan H.W. et al. ранее была установлена тканеспецифичная экспрессия семейства let-7 в плаценте, хориодецидуальной оболочке и амнионе на момент родов, а ее мишень Lin28 не экспрессировалась в плодных оболочках. При этом авторы не увидели существенных различий экспрессии в зависимости от начала родов и родоразрешения, несмотря на то, что сигнальная ось Lin28/let-7 связана с воспалительными сигналами. Исследователи сделали вывод, что воспаление в тканях во время родов опосредуется преимущественно классическим сигнальным путем NF-kB [35]. Другими авторами было показано, что повышенная экспрессия let-7 ингибирует продукцию интерлейкина-6; при этом NF-kB активирует Lin28B, подавляя ее экспрессию, что приводит к выработке интерлейкина-6 и последующему воспалению [36]. Пониженная экспрессия let-7b связана с увеличением регуляции TLR4, активацией NF-κB и повышенной экспрессией PTGS2 [37]. Учитывая полученные нами данные, демонстрирующие, напротив, повышенную экспрессию let-7b-5p в плодных оболочках и миометрии, можно предположить, что let-7b-5p задействована не в инициации воспалительной реакции, а в гормональной регуляции родовой деятельности. Наше предположение подтверждает ранее описанная роль let-7b в регуляции продукции стероидных гормонов [38]. В частности, let-7b, связываясь с геном Smad2/3 в сигнальном пути трансформирующего фактора роста (TGF-β), может влиять на секрецию эстрогена [39]. А экспрессия let-7b может напрямую индуцироваться эстрадиолом [40]. Более того, экспрессия let-7b-5р и в миометрии, и в плодных оболочках у беременных с положительным эффектом от преиндукции значимо отличалась от беременных, которым преиндукцию не проводили. Что также может являться косвенным свидетельством гормональной регуляции, опосредованной let-7b-5р. Кроме того, мы заметили существенную разницу между группами беременных со спонтанными родами и индуцированными в экспрессии let-7b-5р в плодных оболочках и миометрии. Данная разница статистически не значима в силу малочисленности выборки, хотя такая тенденция прослеживается.
В плодных оболочках у беременных после положительного ответа на преиндукцию значимо снижалась экспрессия miR-146a-5p относительно беременных с отсутствием эффекта. МiR-146-5p, подобно другим мкРНК, может нацеливаться на широкий спектр генов-мишеней и быть вовлеченной, таким образом, в регуляцию множества независимых физиологических процессов. В числе ее потенциальных мишеней также рассматриваются NF-kB и PTGS2. Известно, что miR-146a-5р участвует в контроле воспалительного ответа клеток врожденной иммунной системы, особенно моноцитов/макрофагов. Действуя через путь NF-kB, miR-146a-5р в качестве негативного регулятора может стимулировать высвобождение провоспалительных цитокинов [41]. Ранее в экспериментах с опухолевыми клетками была выявлена регуляция экспрессии по оси miR-146a-5p/COX2: низкие уровни miR-146a-5p связаны с повышенными уровнями COX2 [42]. Интересно, что Cook J.R. et al. установили влияние окситоцина на подавление экспрессии miR-146a-5p в культуре первичных миоцитов, подчеркнув тем самым, что ее экспрессия зависима от введения окситоцина [36]. В нашем исследовании мы не использовали окситоцин в качестве стимулятора, и значимых изменений экспрессии miR-146a-5p в миометрии также не выявлено. Следовательно, изменение ее экспрессии в плодных оболочках посредством регуляции COX2 может свидетельствовать о вовлеченности miR-146a-5p в передачу воспалительных сигналов от плода, стимулирующих родовую деятельность.
Принимая во внимание полученные данные об изменении экспрессии исследуемых мкРНК, мы провели корреляционный поиск с использованием метода непараметрической ранговой корреляции Спирмена. Анализ позволил установить, что экспрессия miR-181a-5р в крови матери до индукции, а let-7b-5p и miR-146a-5p в плодных оболочках коррелирует с баллами по шкале Бишоп, подтверждая их вовлеченность в процесс инициации родов.
Ограничения исследования
Ограничения нашего исследования связаны с небольшим количеством пациентов, в связи с чем необходимы дальнейшие исследования сигнальных молекул, запускающих механизм инициации родовой деятельности, на расширенной когорте беременных.
Заключение
Выявленные отличия экспрессии экзосомальных и тканевых мкРНК обусловлены высокоскоординированной регуляцией различных сигнальных путей и модуляцией экспрессии соответствующих генов-мишеней, вовлеченных в механизм коммуникации компартментов матери и плода.



