Третий триместр беременности (поздний плодовый период) – время завершения развития плаценты, начала ее физиологической инволюции, активного роста и развития органов плода, в том числе функционального становления его регуляторных систем, перестройки организма матери для подготовки к предстоящим родам, формирования родовой доминанты [1, 2].
Любое повреждающее воздействие на этом важном этапе гестации может способствовать дезадаптации и нарушению физиологического равновесия, торможению или, наоборот, ускорению генетически запрограммированных процессов донашивания беременности, ее преждевременному завершению, а также появлению осложнений для матери и плода. В настоящее время глобальной чрезвычайной ситуацией является пандемия COVID‑19. Широкое распространение новой коронавирусной инфекции (НКВИ) и регулярное появление новых штаммов вируса SARS‑CoV‑2 вызывает повышенный интерес врачей акушеров‑гинекологов, так как опасность представляет не только сама инфекция, но и ее отдаленные последствия для матери и плода.
До сих пор имеются дискуссионные вопросы: является ли НКВИ причиной осложнений течения беременности и неблагоприятных перинатальных исходов, и связан ли гестационный срок на момент постановки диагноза COVID‑19 у матери с неблагоприятными перинатальными исходами?
Многочисленные исследования сообщают об увеличении числа осложнений беременности у женщин, после перенесенной НКВИ в I [3, 4], II [5, 6] и III [7, 8] триместрах беременности. Наряду с этим имеются исследования доказывающее обратное – вирус SARS‑CoV‑2 не является причиной неблагоприятных исходов беременности [9, 10].
Необходимо дальнейшее накопление знаний о течении беременности, перинатальных исходах у женщин, перенесших НКВИ в III триместре беременности.
Цель исследования: изучить особенности течения беременности, родов, перинатальные исходы у женщин, перенесших НКВИ в III триместре, родоразрешенных в постковидном периоде.
Материалы и методы
Проведено одноцентровое ретроспективное обсервационное когортное исследование [11]. На базе COVID‑госпиталя ФГБУ «Уральский научно‑исследовательский институт охраны материнства и младенчества» Министерства здравоохранения Российской Федерации («НИИ ОММ») проведено лечение 823 беременных с подтвержденным диагнозом НКВИ легкой и среднетяжелой формы в первую, вторую и третью «волны» эпидемического процесса, согласно методическим рекомендациям по организации оказания медицинской помощи беременным, роженицам, родильницам и новорожденным при НКВИ [12]. Из них 414 пациенток в момент инфицирования SARS‑CoV‑2 имели срок беременности более 28 недель (III триместр). В основную группу включены 313 пациенток, которые были родоразрешены в постковидном периоде – после клинического выздоровления с лабораторным подтверждением отсутствия генетического материала вируса в мазке со слизистой носои ротоглотки. Основная группа была разделена на 3 подгруппы в зависимости от сроков гестации в момент инфицирования SARS‑CoV‑2: 1‑я подгруппа (n=90) – беременные, перенесшие заболевание в сроках 28,1 – 32,0 недели; 2‑я подгруппа (n=154) – беременные, перенесшие НКВИ в сроки гестации 32,1–36,6 недель; 3‑я подгруппа (n=69) – беременные, переболевшие в сроки гестации 37 и более недель.
Средний срок беременности в момент инфицирования пациенток основной группы составил 34,9 (3,9) недель: в 1‑й подгруппе – 29,4 (0,8) недель, во 2‑й подгруппе – 33,9 (1,8) недели, в 3‑й подгруппе – 38,9 (1,2) недель.
Критерии включения в основную группу: беременные с подтвержденным диагнозом НКВИ легкой и среднетяжелой формы в сроках гестации от 28 и более недель; подписанное информированное согласие на участие в исследовании, клиническое выздоровление на момент родоразрешения. Критерии невключения: срок беременности менее 28 недель на момент заболевания НКВИ, роды во время заболевания без клинического выздоровления.
Женщины после перенесенной инфекции вынашивали беременность под наблюдением женских консультаций по месту жительства; 87 пациенток были родоразрешены в НИИ ОММ, 226 пациенток – в родильных домах города Екатеринбурга и Свердловской области. Сведения о течении беременности у пациенток основной группы были получены из медицинской документации НИИ ОММ и системы «Региональный акушерский мониторинг». Группу сравнения составили 216 пациенток, родоразрешенных в «доковидном» периоде (2019 г.) без указаний на острую респираторную вирусную инфекцию (ОРВИ) в период беременности и родоразрешения. Данная группа была набрана из базы данных системы «Региональный акушерский мониторинг» методом случайного отбора с помощью таблицы случайных чисел согласно разделам 6.1.,6.2. ГОСТ «Процедуры отбора случайной выборки и рандомизации» [13]. Расчет размера выборки группы сравнения произведен с помощью калькулятора мощности [14].
Проведена морфофункциональная оценка 87 плацент от женщин, переболевших НКВИ в легкой и среднетяжелой форме в разные периоды III триместра беременности: 1‑я подгруппа (n=25) – в сроки беременности 28,1–32,0 недели; 2‑я подгруппа (n=39) – в сроки гестации 32,1–36,6 недель; 3‑я подгруппа (n=32) – в сроки доношенной беременности. Пациентки родоразрешены в постковидном периоде в НИИ ОММ. Группа сравнения (n=20) – плаценты женщин с физиологически протекающей беременностью, без указания на перенесенную ОРВИ в течение гестации.
Морфологическое исследование плацент проводилось согласно международным методическим рекомендациям [15]. Для микроскопического исследования отбирались фрагменты пуповины, оболочек, участки материнской и плодовой поверхности у пуповины и у края диска. Материал фиксировали в 10% забуференном формалине, подготовка парафиновых блоков, окрашивание срезов толщиной 4 мкм гематоксилином и эозином проводились по стандартной методике.
Статистический анализ
Для статистического анализа и построения графиков применяли пакет компьютерных программ Microsoft Excel (2010), SPSS Statistics версия 22.0 (IBM Microsoft, США). Сравнение частот для качественных признаков проводилось путем анализа четырехпольных таблиц с использованием критерия χ2. Качественные порядковые (ординальные) признаки представлены в виде медианы и IQR (интерквартильный размах) в формате Me (Q1:Q3). Проверка гипотез при этом осуществлялась по U‑критерию Манна–Уитни.
Проверка гипотезы о нормальном распределении выборки осуществлялась с помощью критерия Колмогорова–Смирнова и Шапиро–Уилка. Процедура проверки равенства дисперсий выполнена по f‑критерию в пакете SPSS Statistics версия 22.0, которая непосредственно включена в процедуру проверки гипотезы о различии средних. Данные представлены в виде среднего арифметического (М) и стандартного отклонения (SD), значения для качественных категориальных переменных представлены как число субъектов (n) и процент (%).
Относительный риск (ОР) с 95% доверительным интервалом (ДИ) был рассчитан для оценки вероятности развития наступления определенного события у лиц основной группы, подвергшихся воздействию фактора риска, по отношению к группе сравнения. С учетом поправки Бонферрони статистически значимыми считали различия признаков в группах при уровне значимости р<0,017.
Исследование одобрено этическим комитетом НИИ ОММ (протокол №12 от 21.09.2020 г.). Основным ограничением этого исследования является возможность систематической ошибки отбора из‑за одноцентрового характера исследования.
Результаты и обсуждение
Возраст пациенток основной группы колебался от 16 до 52 лет и составил в среднем 29,5 (6,1) года: в 1‑й подгруппе – 29,6 (6,6) года, во 2‑й подгруппе – 29,6 (5,9) года, в 3‑й подгруппе – 29,3 (5,9) года. Возраст пациенток группы сравнения варьировал от 20 до 47 лет, в среднем – 29,1 (5,7) года.
Сравниваемые группы сопоставимы по возрасту, паритету, акушерско‑гинекологическому анамнезу (р>0,05) (табл. 1).
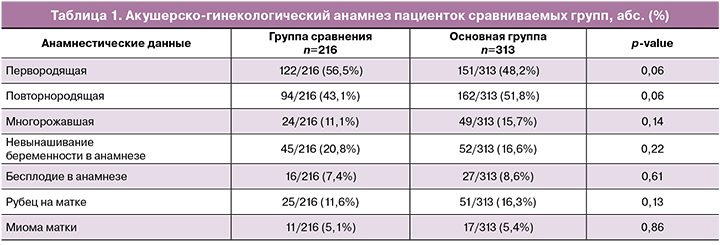
При анализе соматического анамнеза пациенток сравниваемых групп установлено, что беременные женщины основной группы чаще имели избыточную массу тела и ожирение, болезни органов дыхания (в основном хронический бронхит и бронхиальная астма). На сегодняшний день подтверждено, что данные патологии входят в число заболеваний, ухудшающих течение НКВИ [16]. Пациентки группы сравнения чаще имели болезни органов пищеварения (в основном гастрит, холецистит) и мочевыделительной системы (хронический пиелонефрит). Наиболее частыми фоновыми патологиями гестационного процесса у пациенток, инфицированных в III триместре вирусом SARS‑CoV‑2, являлись гестационный сахарный диабет (ГСД) (выявлен до НКВИ у каждой пятой пациентки, 63/313 (20,1%)) и анемия (выявлялась до НКВИ у каждой третьей пациентки основной группы, 96/313 (30,7%)). В постковидном периоде у части пациенток основной группы (1‑я и 2‑я подгруппы) ГСД и анемия, не выявлявшиеся до заболевания, зарегистрированы дополнительно у 16/313 (5,1%) и 13/313 (4,2%) соответственно. Это характеризует влияние перенесенной инфекции на метаболизм глюкозы и железа. Дефицит железа, нарушение обмена глюкозы в организме беременной создают условия для быстрого формирования гипоксических изменений, что приводит к снижению иммунного ответа на инфекцию [17] и может способствовать развитию перинатальных осложнений.
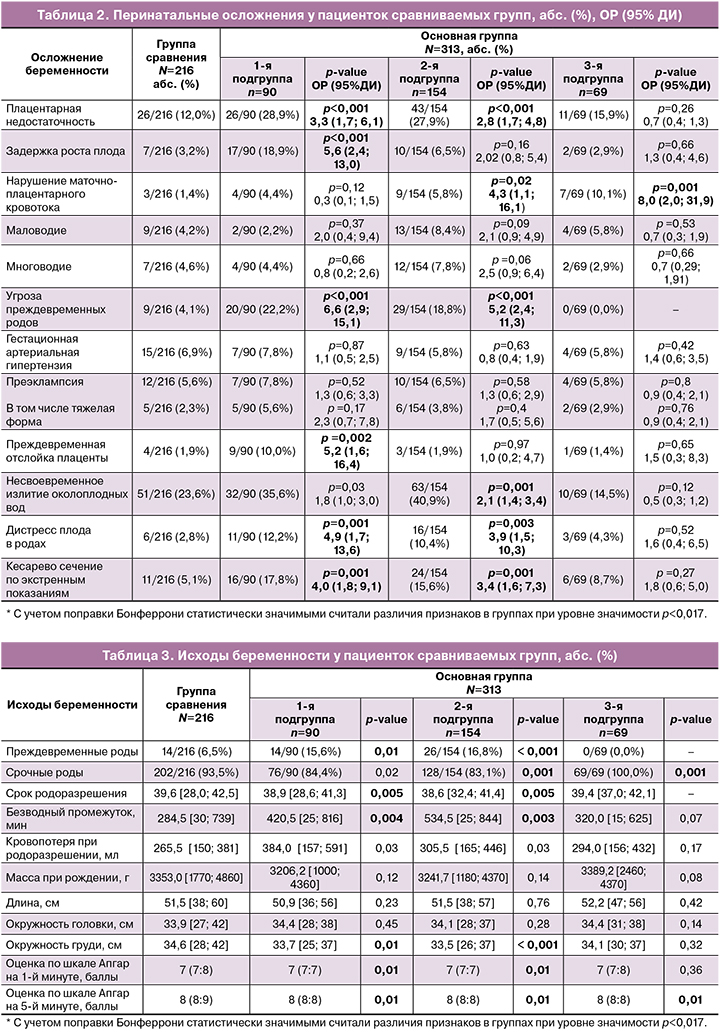
Детальный анализ течения и исходов беременности у пациенток, перенесших НКВИ в разные периоды III триместра беременности, в сравнении с вынашивающими беременность и родоразрешенными в «доковидное» время, представлены в таблицах 2 и 3. Третий триместр беременности предъявляет наиболее серьезные требования к адаптационным резервам организма беременной женщины и внутриутробного плода: с одной стороны, это обусловлено перестройкой функции органов и систем беременной для подготовки к предстоящему родоразрешению; с другой – становлением систем органов плода для подготовки его к жизни во внеутробной среде. Поэтому дополнительные патологические воздействия чреваты наиболее серьезными, порой непредсказуемыми последствиями [18].
Известно, что при физиологически протекающей беременности в начале III триместра плацента приобретает структурные признаки зрелости с максимальной эндокринной функцией (выработка плацентарного лактогена, стероидных гормонов), способностью кровоснабжения и оксигенации плода. К 32,0 неделям гестации в плаценте происходит завершение формирования виллезного дерева, одной из главных структурных образований которого являются терминальные ворсины с синцитиокапиллярными мембранами, обеспечивающие фетоплацентарный обмен веществ [1, 2]. У плода к 28 неделям беременности сформированы все системы органов, созревание которых происходит в III триместре. Так, с 28,0 по 32,0 неделю начинаются дифференцировка альвеоцитов I и II типов, выработка сурфактанта [19], происходит завершение формирования основных механизмов центральной регуляции дыхания [20].
По данным нашего исследования, у женщин 1‑й подгруппы, перенесших НКВИ в сроки с 28,1 по 32,0 неделю, течение беременности осложнилось хронической плацентарной недостаточностью с исходом в задержку роста плода (17/90 (18,9%), p<0,001), угрозой преждевременных родов (20/90 (22,2%), p<0,001).
Завершилась беременность преждевременными родами у 14/90 (15,6%) человек, что в 2 раза чаще, чем в группе сравнения (14/216 (6,5%), p=0,01). В связи с этим средний срок родоразрешения пациенток 1‑й подгруппы был значимо меньше (38,9 [28,6; 41,3]) по сравнению с пациентками, родоразрешенными в «доковидное» время (39,6 [28,0; 42,5], p=0,005).
Преждевременные роды у пациенток этой подгруппы происходили в среднем через 1 месяц от начала заболевания (34,5 [25,0; 44,0] сутки), а после констатации клинического выздоровления преждевременные роды наступали в среднем через три недели (22,5 [15,0; 30,0] сутки).
У пациенток, переболевших НКВИ в начале III триместра, длительность безводного промежутка в среднем была больше, чем в группе сравнения – 7,0 (0,9) ч против 4,7 (0,5) ч соответственно (p=0,004).
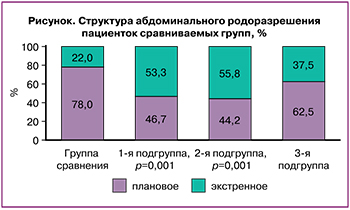
В структуре абдоминального родоразрешения преобладало экстренное кесарево сечение (рисунок), показаниями для которого послужили: дистресс плода в родах – у 11/90 (12,2%), p=0,001), у каждой десятой – преждевременная отслойка плаценты (9/90 (10,0%), p=0,002).
По данным литературы, в середине III триместра в плаценте происходит увеличение количества терминальных ворсин, возрастает объем межворсинкового пространства, что обеспечивает максимальную способность обмена веществ между кровью матери и плода [1, 2]. У плода в период с 32,0 по 36,6 неделю внутриутробного развития наблюдается интенсивный рост (в среднем масса плода увеличивается на 25 г в день), ускоряется развитие головного мозга плода, завершается миелинизация нервных волокон центральной нервной системы [20].
В проведенном нами исследовании у пациенток 2‑й подгруппы, перенесших НКВИ в сроки с 32,1 по 36,6 неделю, угроза преждевременных родов зарегистрирована у каждой пятой пациентки (29/154 (18,8%), p<0,001), так же, как и в 1‑й подгруппе.
Средний срок родоразрешения пациенток 2‑й подгруппы значимо отличался от группы сравнения в сторону уменьшения (38,6 [32,4; 41,4], p=0,005), что связано с повышенной частотой преждевременных родов (26/154 (16,8%)). Отмечено, что преждевременные роды произошли в среднем через 3 недели от начала заболевания (23,8 [14,0; 30,0] суток) и через 2 недели с момента констатации клинического выздоровления (13,5 [7,0; 22,0] суток).
Роды у женщин, перенесших НКВИ в середине III триместра, значимо чаще осложнились длительным безводным промежутком в среднем до 8,9 (1,3) ч; в группе сравнения безводный промежуток в среднем составил 4,7 (0,5) ч.
Путем операции кесарева сечения родоразрешены 27,9% женщин данной подгруппы, что значимо не отличается от группы сравнения. Однако в структуре преобладали операции по экстренным показаниям (рисунок) – 24/43 (55,8%), что в 2 раза чаще, чем в группе сравнения (11/50 (22,0%), р=0,001. Наиболее частым показанием для экстренного кесарева сечения явился дистресс плода в родах, выявленный у каждой десятой пациентки (16/154(10,4%), р=0,003).
Результаты нашего исследования подтверждают отчеты отечественных и зарубежных исследователей, описывающие случаи отслойки плаценты [21], задержки роста плода [22] у женщин, перенесших COVID‑19 во время беременности. В систематических обзорах опубликована информация об увеличении частоты преждевременных родов от 13,8 до 25,0% среди женщин с COVID‑19 [23, 24] по сравнению с общепопуляционным уровнем в Российской Федерации – 6,1% [25]. Авторы объясняют патогенетические механизмы акушерской патологии при COVID‑19. Так, нарушение гемодинамических показателей в маточно‑плацентарной системе обусловлено взаимодействием вируса с эндотелиальными клетками, что вызывает гиперкоагуляцию с образованием микротромбов в системе мать–плацента– плод [26]. Перенесенная НКВИ является триггером преждевременных родов и связана с повышенной выработкой провоспалительных цитокинов в маточно‑плацентарном комплексе, активацией гипоталамо‑гипофизарной системы матери и плода [27].
Антропометрические параметры, такие как окружность груди, оценка состояния здоровья по шкале Апгар на 1‑й и 5‑й минутах после рождения, значимо меньше у детей от пациенток, перенесших НКВИ в начале и в середине III триместра, чем у родившихся детей в «доковидную» эпоху (табл. 3). Возможно, это связано с внутриутробной гипоксией на фоне длительно текущей плацентарной недостаточности, что приводит к отставанию морфологического и функционального созревания органов, в частности задержки созревания легких [19].
У пациенток 3‑й подгруппы, перенесших НКВИ в сроках доношенной беременности и родоразрешенных после клинического выздоровления, значимо чаще выявилось нарушение маточно‑плацентарного кровотока (7/69 (10,1%), p=0,001), так же как и у пациенток 2‑й подгруппы. Новорожденные дети женщин 3‑й подгруппы имели значимо меньшую оценку состояния по шкале Апгар на 5‑й минуте, что свидетельствует о нарушении процессов ранней постнатальной адаптации. Это свидетельствует о том, что при перенесенной матерью НКВИ в сроках доношенной беременности плод остается достаточно чувствительным и уязвимым.
Не выявлено значимых различий между пациентками основной группы и группы сравнения по изменению продолжительности родового акта, частоте аномалии родовой деятельности (p>0,05).
Все вышеперечисленные особенности течения беременности и перинатальные исходы подтверждаются результатами гистологического исследования плацент (табл. 4).
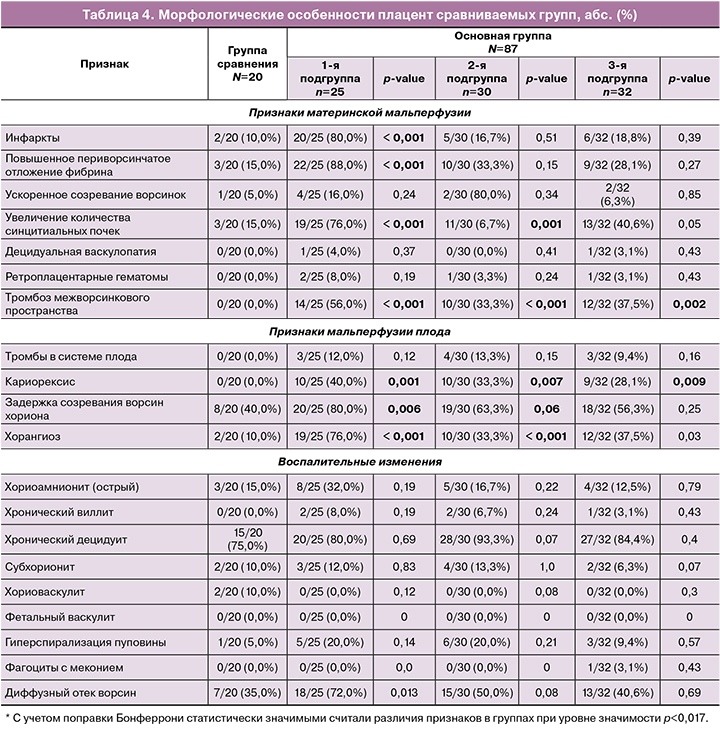
В плацентах у пациенток 1‑й подгруппы значимо чаще встречались инфаркты (в 80%), повышенное отложение фибриноида с формированием обширных афункциональных зон (в 88%); в связи с этим наблюдалось увеличение количества синцитиальных узлов (изменения Tenney Parker), что относится к признакам материнской сосудистой мальперфузии. Более чем в половине плацент наблюдался тромбоз межворсинкового пространства. Согласно данным литературы, подобные изменения в плаценте приводят к хронической плацентарной недостаточности с исходом в задержку роста плода, преждевременным родам [28]. Наряду с материнской сосудистой недостаточностью, в плацентах пациенток 1‑й подгруппы значимо чаще отмечались признаки мальперфузии плода: в 80% – задержка созревания ворсин хориона; в 76% – увеличение количества капилляров в терминальных ворсинах (хорангиоз), а в 40% – кариорексис.
В плацентах пациенток 2‑й и 3‑й подгруппы, в отличие от 1‑й подгруппы, сосудистые нарушения со стороны матери и со стороны плода выражены не так ярко. Тем не менее значимо чаще в плацентах материнская сосудистая недостаточность проявлялась увеличением количества синцитиальных почек, тромбозом межворсинкового пространства. В плацентах признаками нарушения кровоснабжения плода значимо чаще отмечались задержка созревания ворсин хориона, хорангиоз.
В отличие от плацент пациенток основной группы, в плацентах группы сравнения признаки материнской сосудистой мальперфузии регистрировались реже, были меньше по размеру и редко распространялись на всю толщу плаценты. Избыточное отложение фибриноида с формированием афункциональных зон также встречалось лишь в 15% случаев, несмотря на более поздний срок родоразрешения. Задержка созревания ворсин была отмечена в 40% случаев, что практически в 2 раза реже, чем у женщин перенесших COVID в сроки до 32 недель, то есть до полноценного формирования терминальных ворсин. Воспалительные изменения встречались в единичных случаях и не имели специфических черт.
Возможно, все вышеприведенные морфологические изменения в плаценте связаны с наличием в ее клетках рецепторов к коронавирусам: ангиотензинпревращающего фермента‑2, сериновой протеазы TMPRSS2 и Cd147. Однако нами не проводился анализ наличия или отсутствия в плацентах вируса SARS‑CoV‑2. Кроме того, это может быть связано с тромбозами, которые характерны для данного заболевания [28].
Заключение
Результаты исследования доказывают влияние НКВИ легкой и среднетяжелой формы, перенесенной в III триместре беременности, на развитие перинатальных осложнений на постковидном этапе. Наиболее серьезные последствия выявлены у пациенток, перенесших НКВИ в сроки от 28,1 до 32,0 недель: значимо возрастает риск развития хронической плацентарной недостаточности с исходом в задержку роста плода – в 6 раз, риск преждевременных родов – в 3 раза, риск преждевременной отслойки плаценты – в 5 раз, риск дистресса плода в родах – в 5 раз. При этом в родах значимо увеличивается длительность безводного промежутка.
Риск экстренного абдоминального родоразрешения увеличивается в 4 раза.
Наиболее выраженные признаки материнской и плодовой мальперфузии выявлены в плацентах пациенток, перенесших НКВИ в начале III триместра, по сравнению с плацентами пациенток, переболевших НКВИ в более поздние сроки беременности, у которых сосудистые нарушения со стороны матери и плода выражены менее ярко.



