1) Московский научно-исследовательский онкологический институт имени П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Министерства здравоохранения Российской Федерации, Москва, Россия;
2) ФГАОУ ВО «Российский университет дружбы народов», Москва, Россия;
3) ФГАОУ ВО «Первый Московский государственный медицинский университет имени И.М. Сеченова Министерства здравоохранения Российской Федерации» (Сеченовский Университет), кафедра онкологии, радиотерапии и пластической хирургии, Москва, Россия
Неоадъювантная полихимиотерапия (НАПХТ) представляет собой краеугольный камень в лечении местно-распространенного рака молочной железы (РМЖ) и опухолей с высокой химиочувствительностью, таких как тройной негативный и Her/neu-позитивные типы. Отсутствие четкого консенсуса относительно оптимального способа реконструкции молочной железы после НАПХТ привело к большому разнообразию используемых методик. Также остаются неясными факторы, влияющие на выбор оперативного вмешательства.
Поиск соответствующих источников был осуществлен в системах PubMed, Cochrane Library, eLibrary, изучены публикации с 2012 по 2023 гг., 27 из которых были использованы для написания данного обзора.
Сведения о возможности выполнения и расширения показаний к органосохраняющему лечению, выполнению реконструктивно-пластических операций, в том числе одномоментных реконструкций с использованием алломатериалов, после НАПХТ отражают современные отечественные и мировые тенденции в лечении пациентов с РМЖ. При выполнении одномоментной реконструкции могут быть использованы различные способы: собственными тканями, с использованием алломатериалов, реконструкция торакодорзальным лоскутом в комбинации с эндопротезом/тканевым экспандером и т.д. Показаниями к выполнению мастэктомии с одномоментной одноэтапной или двухэтапной реконструкцией после НАПХТ являются: отсутствие ответа опухоли на НАПХТ (NR); при частичном ответе – соотношение размера резидуальной опухоли и размера молочной железы, не позволяющие выполнить органосохраняющую операцию (ОСО) и, соответственно, достичь удовлетворительного эстетического результата; если до НАПХТ не была установлена внутритканевая метка в опухолевый узел (при CR и PR); нежелание пациентки выполнить ОСО, но при этом сохранить удовлетворительный эстетический результат после операции.
Заключение: Выполнение одномоментной реконструкции молочной железы с использованием алломатериалов является безопасным с онкологической точки зрения, не повышает частоту развития хирургических осложнений. Эстетические результаты операции также сопоставимы с аналогичными показателями у пациентов, которым не проводилась НАПХТ на первом этапе.
Вклад авторов: Зикиряходжаев А.Д., Босиева А.Р. – разработка концепции и дизайна исследования; Босиева А.Р. – сбор и обработка данных, написание текста; Зикиряходжаев А.Д. – редактирование текста.
Конфликт интересов: Авторы заявляют об отсутствии конфликта интересов.
Финансирование: Работа выполнена без спонсорской поддержки.
Для цитирования: Зикиряходжаев А.Д., Босиева А.Р. Неоaдъювантная полихимиотерапия и одномоментная реконструкция у больных раком молочной железы.
Акушерство и гинекология. 2024; 2: 31-36
https://dx.doi.org/10.18565/aig.2023.252
рак молочной железы
неоадъювантная полихимиотерапия
одномоментная реконструкция молочной железы
алломатериалы
Неоадъювантная полихимиотерапия (НАПХТ) на сегодняшний день представляет собой краеугольный камень в лечении местно-распространенного рака молочной железы (РМЖ) и опухолей с высокой химиочувствительностью, таких как тройной негативный и Her/neu-позитивные типы [1–5]. Показаниями для проведения НАПХТ являются размер опухолевого узла, молекулярно-биологический тип, метастатическое поражение лимфатических узлов и степень злокачественности. НАПХТ играет ключевую роль в уменьшении размера опухоли, увеличении возможности проведения органосохраняющего хирургического лечения по сравнению с реконструктивно-пластическими операциями [6, 7] и, таким образом, уменьшении необходимости выполнения подмышечно-подлопаточно-подключичной лимфаденэктомии [2, 8, 9]. Другим преимуществом НАПХТ является оценка ответа in vivo [2, 10, 11].
Кроме того, существует большая вариабельность ответа РМЖ на НАПХТ? и, соответственно, точная оценка ответа на лечение имеет решающее значение при определении объема лечения и необходимости выполнения дальнейших хирургических вмешательств. Тем не менее установление полного патоморфологического ответа (pCR), ассоциированного с прогнозом заболевания, позволяет онкологам обеспечить персонализированный подход в определении оптимального объема хирургического лечения [12, 13].
Методы визуализации (ультразвуковое исследование молочных желез, рентгеномаммография, магнитно-резонансная томография) играют важную роль в оценке ответа опухоли на НАПХТ и принятии решения врачом-онкологом относительно объема оперативного лечения.
Несмотря на то что НАПХТ позволяет повысить частоту выполнения органосохраняющих операций, остаются больные, у которых данный объем хирургического лечения не является оптимальным после НАПХТ. В таких случаях одномоментная реконструкция молочной железы по-прежнему остается вариантом, обеспечивающим лучшее качество жизни, высокую удовлетворенность пациента, хороший косметологический результат и психоэмоциональное благополучие.
Показаниями к выполнению мастэктомии с одномоментной одноэтапной или двухэтапной реконструкцией после НАПХТ являются:
- отсутствие ответа опухоли на НАПХТ (NR);
- при частичном ответе – соотношение размера резидуальной опухоли и размера молочной железы, не позволяющие выполнить органосохраняющую операцию (ОСО) и, соответственно, достичь удовлетворительного эстетического результата;
- если до НАПХТ не была установлена внутритканевая метка в опухолевый узел (при CR и PR);
- нежелание пациентки выполнить ОСО, но при этом сохранить удовлетворительный эстетический результат после операции.
Отсутствие четкого консенсуса относительно оптимального способа реконструкции молочной железы после НАПХТ привело к большому разнообразию используемых методик [14–16]. Также остаются неясными факторы, влияющие на выбор оперативного вмешательства.
При выполнении одномоментной реконструкции могут быть использованы различные способы: собственными тканями, с использованием алломатериалов, реконструкция торакодорзальным лоскутом в комбинации с эндопротезом/тканевым экспандером и т.д.
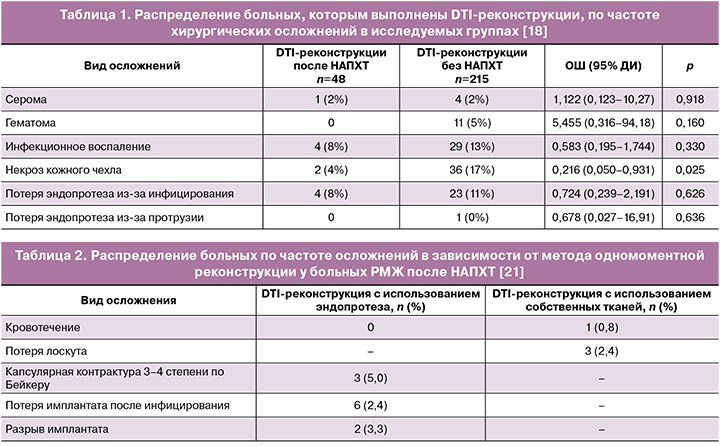
В ряде исследований продемонстрированы эквивалентные онкологические результаты у пациентов, которым выполнена DTI-реконструкция (Direct-to-Implant, одномоментная реконструкция молочной железы с использованием силиконового эндопротеза) и мастэктомия без реконструкции после НАПХТ. Так, Monrigal E. в своем исследовании отметил в 46 (21,9%) случаях развитие ранних осложнений после DTI-реконструкций: 20 липонекрозов, 9 инфицирований послеоперационных ран, 6 гематом, которые потребовали ре-операций в 23 случаях. Большинство липонекрозов отмечено при реконструкции TRAM-лоскутом (p=0,000004). У 55 пациентов отмечены поздние осложнения (26,2%), такие как капсулярная контрактура, инфицирование, протрузии, что в 23,6% (14) случаев потребовало выполнения реопераций [17]. Donker M. et al. на основании проведенного исследования установили, что нет статистически значимой разницы в показателях хирургических осложнений среди больных, которым выполнена DTI-реконструкция с/без проведением НАПХТ (p≥0,05) (табл. 1) [18].
Chi W. в 2023 г. представил результаты исследования, согласно которому возраст пациента и стадия заболевания являются основополагающими при планировании одномоментной реконструкции после НАПХТ. Всего в исследование включены 1651 больных, которые получили НАПХТ, из которых 247 (15,0%) выполнены DTI-реконструкции, а 1404 – радикальные мастэктомии. Пациенты в группе DTI-реконструкции были моложе (P<0,001), имели более низкий индекс массы тела (P<0,001) и меньшую распространенность РМЖ (P=0,003) в сравнении с обычными мастэктомиями. Пациенты в группе одномоментной реконструкции с использованием собственных тканей были старше (P<0,001) и имели более высокий индекс массы тела (P=0,007), больший размер опухоли (P=0,024). Клинически значимые осложнения, которые требовали повторного хирургического вмешательства, чаще встречались в группе одномоментных реконструкций силиконовым эндопротезом в сравнении с использованием собственных тканей (P=0,039). Авторами отмечено, что наиболее оптимальным способом одномоментной реконструкции является использование собственных тканей [19].
Авторами многих исследований отмечено, что существенное влияние на принятие решения относительно способа выполнения одномоментной реконструкции оказывает лучевая терапия. Показано, что при DTI-реконструкции выше частота капсулярной контрактуры и хирургических осложнений. Jagsi R. et al. (2018) проведено крупное проспективное исследование с включением 2247 пациентов, на основании которого авторами отмечена большая удовлетворенность пациентов эстетическими результатами операции после одномоментной реконструкции собственными тканями [20].
Безопасность выполнения DTI-реконструкции после НАПХТ доказана авторами ряда исследований. Beugels J. et al. проанализировали частоту осложнений после одномоментных реконструкций DIEP-лоскутом у больных, которым на первом этапе проведена НАПХТ. Установлено, что частота хирургических осложнений составила 10,4% со стороны реципиентного участка и 22,2% – для донорского участка. Авторами не отмечена статистически значимая разница в частоте осложнений между больными, которым проведена на первом этапе НАПХТ, и пациентами, которым она не проводилась (табл. 2) [21]. Ishiba T. et al. проанализировали результаты лечения 909 пациентов, перенесших одномоментные реконструкции с использованием эндопротеза и собственными тканями, из которых 43 получили на первом этапе НАПХТ. Установлено, что частота осложнений составила 7% при одномоментных реконструкциях после НАПХТ против 3,6%, которым не проводилась предоперационная лекарственная терапия (р=0,25). Авторы отмечают безопасность DTI-реконструкции после НАПХТ [22].
Naoum G.E. et al. проанализировали данные 300 больных, которым проведена НАПХТ с последующим выполнением реконструктивно-пластических операций и проведением адъювантной лучевой терапии. Авторами отмечено, что использование тканевых экспандеров/имплантатов было ассоциировано с повышенным риском развития инфекционных осложнений в сравнении с реконструкцией собственными тканями (ОШ 8,1; 95% ДИ 1,7–38,8; P=0,009), что позволяет предположить, что частота осложнений могла быть выше из-за необходимости выполнения повторных операций при замене экспандера на эндопротез [23].
Sabitovic A. et al. провели систематический обзор метаанализа, посвященного оценке результатов одномоментных реконструкций молочной железы у пациенток, которые ранее получили НАПХТ, в сравнении с контрольной группой [24]. В метаанализ были включены 8 исследований с участием 51 731 пациентки, из которых в 5161 случае проведена НАПХТ. Авторами не отмечено статистически значимого влияния НАПХТ на частоту осложнений после DTI-реконструкций (ОШ=1,35; 95% ДИ 0,96–1,91; p=0,09), в том числе на частоту некроза кожного лоскута (ОШ=1,39; 95% ДИ 0,61–3,17; p=0,44) или частоту повторных операций (ОШ=1,09; 95% ДИ 0,87–1,37; р=0,45). При подгрупповом анализе при выполнении одномоментной реконструкции молочной железы с использованием силиконового эндопротеза после НАПХТ отмечена меньшая частота осложнений и неудачных эстетических результатов по сравнению с двухэтапной реконструкцией тканевым экспандером/имплантатом (ОШ=0,43, 95% ДИ 0,26–0,71, р=0,0011) [24].
Yang J.-R. et al. в 2021 г. представили результаты исследования с включением 269 пациентов. Средний срок наблюдения составил 46,3 месяца. Из 269 в 46 случаях проведена НАПХТ; чаще всего выполнялись одномоментные двухэтапные реконструкции с использованием тканевого экспандера/имплантата в сравнении с одномоментной одноэтапной реконструкцией силиконовым эндопротезом непосредственно с использованием имплантата (p<0,001). Частота осложнений, а также удовлетворенность эстетическими результатами в группе НАПХТ и без проведения НАПХТ были сопоставимы (р<0,001) (табл. 3–5) [25].
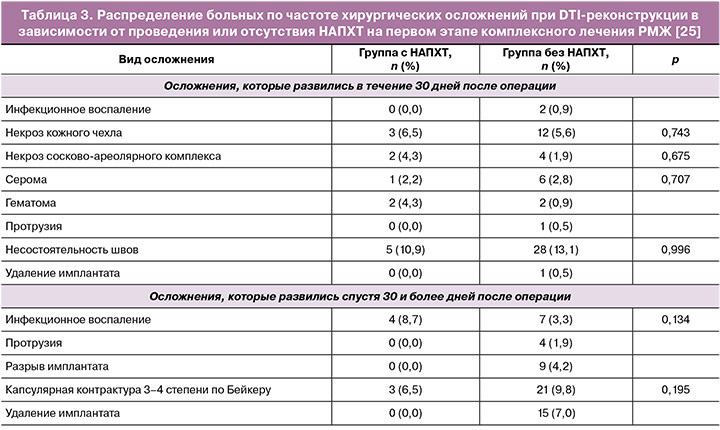
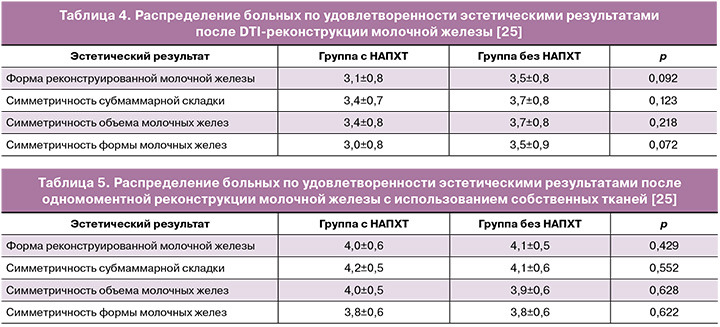
Авторами также не отмечено статистически значимой разницы в проведении/отсутствии НАПХТ и ее влиянии на удовлетворенность эстетическими результатами при одномоментной реконструкции силиконовыми эндопротезами и собственными тканями (табл. 3, 4) [25].
Bowen M.E. et al. представили результаты крупного когортного исследования, на основании которого авторы отметили, что НАПХТ не повышает риск развития хирургических осложнений [26]. Аналогичным образом, Beugels J. et al. сообщили о сопоставимой частоте послеоперационных осложнений у пациентов, получавших и не получавших НАПХТ с последующим выполнением DTI-реконструкции с использованием DIEP лоскута [27].
Заключение
Выполнение одномоментной реконструкции молочной железы с использованием алломатериалов (DTI-реконструкция) является безопасным с онкологической точки зрения, не повышает частоту развития хирургических осложнений. Эстетические результаты операции также сопоставимы с аналогичными показателями у пациентов, которым не проводилась НАПХТ на первом этапе.
- Бересток Т.С., Зикиряходжаев А.Д., Ермощенкова М.В., Аблицова Н.В., Онофрийчук И.М., Власова М.Ю., Трошенков Е.А. Осложнения после одномоментной одноэтапной и двухэтапной реконструкции имплантатами у больных раком молочной железы при проведении комбинированного/комплексного лечения. Онкология. Журнал им. П.А. Герцена. 2023; 12(3): 54-61.
- Зикиряходжаев А.Д., Фролова М.А., Рассказова Е.А., Глазкова Е.В. Лечение тройного негативного подтипа рака молочной железы. Опухоли женской репродуктивной системы. 2017; 13(2): 20-6.
- Токаев В.К., Зикиряходжаев А.Д., Трошенков Е.А., Рассказова Е.А., Поляк М.А., Никитина Е.А., Малик Д.С. Реконструктивно-пластические операции у больных раком молочной железы со стадиями T1-3N1-3M0. Современная наука: актуальные проблемы теории и практики. Серия: Естественные и технические науки. 2023; 3: 242-8.
- Cardoso F., Kyriakides S., Ohno S., Penault-Llorca F., Poortmans P., Rubio I.T. et al. Early breast cancer: ESMO clinical practice guidelines for diagnosis, treatment and follow-up. Ann. Oncol. 2019; 30(8): 1194-220. https://dx.doi.org/10.1093/annonc/mdz173.
- Burstein H.J., Curigliano G., Loibl S., Dubsky P., Gnant M., Poortmans P. et al. Estimating the benefits of therapy for early-stage breast cancer: The St. Gallen International Consensus Guidelines for the primary therapy of early breast cancer 2019. Ann. Oncol. 2019; 30(10): 1541-57. https://dx.doi.org/10.1093/annonc/mdz235.
- Puig C.A., Hoskin T.L., Day C.N., Habermann E.B., Boughey J.C. National trends in the use of neoadjuvant chemotherapy for hormone receptor-negative breast cancer: A National Cancer Data Base Study. Ann. Surg. Oncol. 2017; 24(5): 1242-50. https://dx.doi.org/10.1245/s10434-016-5733-y.
- Killelea B.K., Yang V.Q., Mougalian S., Horowitz N.R., Pusztai L., Chagpar A.B., Lannin D.R. Neoadjuvant chemotherapy for breast cancer increases the rate of breast conservation: results from the National Cancer Database. J. Am. Coll. Surg. 2015; 220(6): 1063-9. https://dx.doi.org/10.1016/j.jamcollsurg.2015.02.011.
- Mougalian S.S., Soulos P.R., Killelea B.K., Lannin D.R., Abu-Khalaf M.M., DiGiovanna M.P. et al. Use of neoadjuvant chemotherapy for patients with stage I to III breast cancer in the United States. Cancer. 2015; 121(15): 2544-52. https://dx.doi.org/10.1002/cncr.29348.
- Franceschini G., Di Leone A., Natale M., Sanchez M.A., Masett R. Conservative surgery after neoadjuvant chemotherapy in patients with operable breast cancer. Ann. Ital. Chir. 2018; 89: 290.
- von Minckwitz G., Huang C.-S., Mano M.S., Loibl S., Mamounas E.P., Untch M. et al. Trastuzumab emtansine for residual invasive HER2-positive breast cancer. N. Engl. J. Med. 2019; 380(7): 617-28. https://dx.doi.org/10.1056/NEJMoa1814017.
- Parmar V., Krishnamurthy A., Hawaldar R., Nadkarni M.S., Sarin R., Chinoy R. Breast conservation treatment in women with locally advanced breast cancer—experience from a single centre. Int. J. Surg. 2006; 4(2): 106-14. https://dx.doi.org/10.1016/j.ijsu.2006.01.004.
- von Minckwitz G. Preoperative therapy: what, when and for whom? Ann. Oncol. 2008l; 19(Supppl 5): v113-6. https://dx.doi.org/10.1093/annonc/mdn323.
- Hunt K.K., Yi M., Mittendorf E.A., Guerrero C., Babiera G.V., Bedrosian I., Hwang R.F. et al. Sentinel lymph node surgery after neoadjuvant chemotherapy is accurate and reduces the need for axillary dissection in breast cancer patients. Ann. Surg. 2009; 250(4): 558-66. https://dx.doi.org/10.1097/SLA.0b013e3181b8fd5e.
- Cen C., Chun J., Kaplowitz E., Axelrod D., Shapiro R., Guth A., Schnabel F. Margin assessment and re-excision rates for patients who have neoadjuvant chemotherapy and breast-conserving surgery. Ann. Surg. Oncol. 2021; 28(9): 5142-8. https://dx.doi.org/10.1245/s10434-020-09524-0.
- Fisher B., Bryant J., Wolmark N., Mamounas E., Brown A., Fisher E.R. et al. Effect of preoperative chemotherapy on the outcome of women with operable breast cancer. J. Clin. Oncol. 1998; 16(8): 2672-85. https://dx.doi.org/10.1200/JCO.1998.16.8.2672.
- Conti M., Morciano F., Bufi E., D'Angelo A., Panico C., Di Paola V. et al. Surgical planning after neoadjuvant treatment in breast cancer: a multimodality imaging-based approach focused on MRI. Cancers (Basel). 2023; 15(5): 1439. https://dx.doi.org/10.3390/cancers15051439.
- Monrigal E. Mastectomy with immediate breast reconstruction after neoadjuvant chemotherapy and radiation therapy. A new option for patients with operable invasive breast cancer. Results of a 20 years single institution study. Eur. J. Surg. Oncol. 2011; 37(10): 864-70. https://dx.doi.org/10.1016/j.ejso.2011.07.009.
- Donker M., Hage J.J., Woerdeman L.A.E., Rutgers E.J.T., Sonke G.S. Surgical complications of skin sparing mastectomy and immediate prosthetic reconstruction after neoadjuvant chemotherapy for invasive breast cancer. Eur. J. Surg. Oncol. 2012; 38(1): 25-30. https://dx.doi.org/10.1016/j.ejso.2011.09.005.
- Chi W., Zhang Q., Li L., Chen M., Xiu B., Yang B., Wu J. Immediate breast reconstruction after neoadjuvant chemotherapy: factors associated with surgical selection and complications. Ann. Plast. Surg. 2023; 91(1): 48-54. https://dx.doi.org/10.1097/SAP.0000000000003574.
- Jagsi R., Momoh A.O., Qi J., Hamill J.B., Billig J., Kim H.M. et al. Impact of radiotherapy on complications and patient-reported outcomes after breast reconstruction. J. Natl. Cancer Inst. 2018; 110(2): 157-65. https://dx.doi.org/10.1093/jnci/djx148.
- Beugels J., Bod L., van Kuijk S.M.J., Qiu S.S., Tuinder S.M.H., Heuts E.M. et al. Complications following immediate compared to delayed deep inferior epigastric artery perforator flap breast reconstructions. Breast Cancer Res. Treat. 2018; 169(2): 349-57. https://dx.doi.org/10.1007/s10549-018-4695-0.
- Ishiba T., Aruga T., Miyamoto H., Ishihara S., Nara M., Adachi M. et al. Short- and long-term outcomes of immediate breast reconstruction surgery after neoadjuvant chemotherapy. Surg. Today. 2022; 52(1): 129-36. https://dx.doi.org/10.1007/s00595-021-02316-3.
- Naoum G.E., Oladeru O.T., Niemierko A., Salama L., Winograd J., Colwell A. et al. Optimal breast reconstruction type for patients treated with neoadjuvant chemotherapy, mastectomy followed by radiation therapy. Breast Cancer Res, Treat. 2020; 183(1): 127-36. https://dx.doi.org/10.1007/s10549-020-05747-7.
- Sabitovic A., Trøstrup H., Damsgaard T.E. The impact of neoadjuvant chemotherapy on surgical outcomes following autologous and implant-based immediate breast reconstruction: a systematic review and meta-analysis. J. Plast. Reconstr. Aesthet. Surg. 2023; 87: 17-23. https://dx.doi.org/10.1016/j.bjps.2023.09.048.
- Yang J.R., Kuo W.L., Yu C.C., Chen S.C., Huang J.J. Reconstructive outcome analysis of the impact of neoadjuvant chemotherapy on immediate breast reconstruction: a retrospective cross-sectional study. BMC Cancer. 2021; 21(1): 522. https://dx.doi.org/10.1186/s12885-021-08256-y.
- Bowen M.E., Mone M.C., Buys S.S., Sheng X., Nelson E.W. Surgical outcomes for mastectomy patients receiving Neoadjuvant chemotherapy: a propensity-matched analysis. Ann. Surg. 2017; 265(3): 448-56. https://dx.doi.org/10.1097/SLA.0000000000001804.
- Beugels J., Meijvogel J.L.W., Tuinder S.M.H., Tjan-Heijnen V.C.G., Heuts E.M., Piatkowski A., van der Hulst R.R.W.J. The influence of neoadjuvant chemotherapy on complications of immediate DIEP flap breast reconstructions. Breast Cancer Res. Treat. 2019; 176(2): 367-75. https://dx.doi.org/10.1007/s10549-019-05241-9.
Поступила 08.11.2023
Принята в печать 24.01.2024
Зикиряходжаев Азизжон Дилшодович, д.м.н., профессор, заведующий отделением онкологии и реконструктивно-пластической хирургии молочной железы и кожи, МНИОИ им. П.А. Герцена – филиал «НМИЦ радиологии» Минздрава России, 125284, Россия, Москва, 2-й Боткинский проезд, д. 3; профессор кафедры онкологии, радиотерапии и пластической хирургии Института клинической медицины, Первый МГМУ им. И.М. Сеченова Минздрава России, 119991, Россия, Москва, ул. Трубецкая, д. 8, стр. 2; профессор кафедры онкологии и рентгенорадиологии им. В.П. Харченко, Медицинский Институт РУДН, 117198, Россия, Москва, ул. Миклухо-Маклая, д. 6,
azizz@mail.ru, http://orcid.org/0000-0001-7141-2502
Босиева Алана Руслановна, к.м.н., н.с. отделения онкологии и реконструктивно-пластической хирургии молочной железы и кожи, МНИОИ им. П.А. Герцена – филиал ФГБУ «НМИЦ радиологии» Минздрава России, 125284, Россия, Москва, 2-й Боткинский проезд, д. 3; ассистент кафедры онкологии и рентгенорадиологии
им. В.П. Харченко, Медицинский Институт РУДН, 117198, Россия, Москва, ул. Миклухо-Маклая, д. 6, +7(988)875-10-47,
ms.bosieva@mail.ru, SPIN-код: 1090-7281,
https://orcid.org/0000-0003-0993-8866
Автор, ответственный за переписку: Алана Руслановна Босиева,
ms.bosieva@mail.ru





