Симптоматика вульвовагинита, чаще всего проявляющаяся в виде патологических белей с неприятным запахом, зуда, диспареунии, является наиболее распространенной причиной обращения женщин репродуктивного возраста к специалисту [1, 2]. Чаще всего такую клиническую картину вызывают вульвовагинальные инфекции смешанной этиологии, нередко принимающие рецидивирующий характер [3, 4]. Эта нозология в настоящее время стала серьезной эпидемиологической и клинической проблемой, ведущей к крупным социальным и психологическим последствиям. Длительно текущие вагиниты, нелеченые или плохо поддающиеся лечению, могут привести к таким репродуктивным осложнениям, как бесплодие и невынашивание беременности [1, 3, 5, 6]. Всемирная организация здравоохранения (ВОЗ), IUSTI/ВОЗ и центры по контролю и профилактике заболеваний (CDC) разработали руководящие принципы по лечению выделений из влагалища [2, 7]. Однако, несмотря на эти усилия, случаев рецидивирующих вагинальных инфекций (РВИ) не становится меньше, что, вероятно, обусловлено проблемами правильной постановки диагноза и трудностями в подборе адекватной терапии [4, 8, 9]. В современных исследованиях были высказаны предположения, что не только чрезмерный рост условно-патогенных микроорганизмов является причиной патогенеза смешанных РВИ – существенное значение имеют состав лактобациллярной микрофлоры и доминирование «слабоконкурентных» с условно-патогенной микрофлорой (L. paracasei, L. iners, L. paralimentarius, L. sakei) или обладающих способностью вытеснять нормофлору (L. reuteri, L. plantarum) лактобактерий, что способствует дестабилизации микробиома [10, 11].
Это обусловило необходимость в существенном пересмотре факторов, влияющих на динамику и, следовательно, состав микробных сообществ во влагалище как в норме, так и при патологических состояниях, что в дальнейшем будет способствовать разработке эффективных стратегий диагностики и лечения.
Сообщество микроорганизмов, которые живут внутри или на внешней поверхности человеческого тела, образует человеческую микрофлору/микробиоту, и их геномная конституция называется микробиомом человека [2, 4, 12, 13]. Микробиота человека обычно включает симбионты, которые извлекают выгоду из хозяина, но, в свою очередь, могут не влиять (комменсализм) или положительно (взаимность) и отрицательно (патоген) воздействовать на функционирование, иммунитет и питание хозяина [14]. Во влагалище кооперативные отношения микробов с хозяином обеспечивают первую линию защиты от миграции условно-патогенных микроорганизмов [15]. Состав и структура вагинальной микробиоты были неоднократно описаны в литературе, начиная от анализов с использованием световой микроскопии до высокопроизводительных методов секвенирования [2, 16–20]. Наиболее распространено в составе микробиоты влагалища здоровой женщины репродуктивного возраста преобладание Lactobacillus, производящих достаточное количество молочной кислоты с рН<4,5 [2, 8, 21, 22]. При этом используемые в последнее время молекулярные методы детекции микрофлоры способствуют получению новых данных о составе микробиоты, облегчая обнаружение плохо культивируемых микроорганизмов, что может привести к созданию уникальных типов состояний микробного сообщества (community state types, CST) [23]. На основании данных об обилии и составе вагинальных видов бактерий у женщин репродуктивного возраста эти CST были классифицированы на 5 основных типов: CST-I, CST-II, CST-III и CST-V характеризуются обилием Lactobacillus crispatus, L. gasseri, L. iners и L. jensenii, а CST-IV – сочетанием различных факультативных анаэробов с низким уровнем лактобактерий [24, 25]. CST-IV в дальнейшем был разделен на 2 субтипа: CST-IV-А (содержит виды родов Anaeroccocus, Peptoniphilus, Corynebacterium, Prevotella, Finegoldia и Streptococcus) и CST-IV-В (Atopobium, Gardnerella, Sneathia, Mobiluncus, Mеgasphaera и другие таксоны отряда Clostridiales) [24, 25].
Еще одним спорным моментом в характеристике вагинального микробиоценоза является вопрос о доминировании лактобациллярной флоры, которая до настоящего времени считалась основной определяющей «здоровой» микробиоты влагалища, что подтверждалось множеством исследований о ее доминировании более чем у 70% здоровых женщин [26–28]. Однако сейчас это утверждение подвергается существенным сомнениям из-за двух моментов: во-первых, термин «полезный» и «защитный» не в полной мере применим ко всем видам семейства Lactobacillus – например, L. iners, L. jensenii и L. gasseri считаются патогенными из-за их способности повреждать клетки вагинального эпителия, наличия таких факторов вирулентности, как инеролизин и цитолизин, малой выработки перекиси водорода и молочной кислоты, зарегистрированных связей с бактериальным вагинозом и преждевременными родами, и только L. crispatus до сих пор последовательно был связан со стабильным нормоценозом и более низким риском развития вагинальных дисбиозов и вульвовагинитов, что говорит о видоспецифическом воздействии лактобактерий на хозяина [26–29]; во-вторых, представлено все больше доказательств относительно наличия высокого разнообразия вагинальных микробиомов у здоровых женщин, в которых наличие условно-патогенной микрофлоры (УПМ) носит бессимптомный характер. Кроме того, некоторые исследования показали, что эти микробиоценозы являются малопатогенными, поскольку такие виды, как, например, Atopobium, Mеgasphaera и Leptotrichia, способны продуцировать молочную кислоту и другие антимикробные вещества [30, 31]. Эти противоречия приводят к тому, что, несмотря на десятилетия исследований, до сих пор не найдено ни одного этиологического агента, ответственного за возникновение РВИ, так как это опровергает основной постулат Коха, согласно которому возбудитель необходим для возникновения заболевания и не должен присутствовать в здоровой популяции [32]. Все вышеперечисленное усложняет определение вагинального «здоровья» и нормоценоза, что может приводить в первую очередь к гипердиагностике и, соответственно, полипрагмазии.
Еще одной проблемой существования нормального локального гомеостаза влагалища является его гормональный и иммунный статус. Здоровая вагинальная флора, состоящая в основном из Lactobacillus spp. и эпителия, образует сбалансированную вагинальную экосистему, при этом окружающая среда участвует в естественной защите от патогенов [32, 33]. Необходимы достаточные уровни эстрогена, приводящие к интактному и зрелому стратифицированному плоскоклеточному неороговевающему вагинальному эпителию [34, 35]. Распад пролиферированных поверхностных вагинальных эпителиоцитов высвобождает гликоген, который служит субстратом для лактобацилл [1, 35]. Следовательно, зрелый эпителий влагалища является необходимым условием для установления и поддержания физиологической флоры [2, 15, 36].
И наконец, лечение смешанных рецидивирующих вагинитов, пожалуй, основной «камень преткновения» в исследовании данной нозологии. Представленные во многих научных и клинических работах варианты так называемой «политерапии» в большинстве случаев не оправдывают своих ожиданий, особенно при участии в микробиоте колоний микроорганизмов с бессимптомным течением, что обусловило запрет в некоторых странах на применение комбинированных противомикробных препаратов [37]. Общепринятых стандартов лечения смешанного вагинита не установлено, и, хотя современные методы лечения данного заболевания имеют широкие различия, определенные принципы терапии все же существуют: 1) в соответствии с микроорганизмами и патогенезом (например, лечение, адаптированное к присутствию трех различных компонентов: инфекции, воспаления или атрофии) стандартные методы лечения должны быть выбраны, чтобы свести к минимуму злоупотребление ненужными антибактериальными препаратами; 2) инфекции, передающиеся половым путем, лечатся совместно с половым партнером; 3) лечение начинается с деконтаминации наиболее патогенного микроорганизма, особенно если есть противоречия в назначении этиотропной терапии; 4) необходимость во втором этапе лечения, а именно в проведении деконтаминационной терапии [38]. Все вышеперечисленное диктует необходимость в выборе противомикробных средств широкого спектра с воздействием на патогенную бактериальную флору, грибы и т.д. [38, 39].
Основными целями лечения являются облегчение симптомов, устранение патогенов и, в конечном итоге, восстановление нарушенной микрофлоры влагалища. Альтернативным и достаточно действенным вариантом терапии смешанных вагинитов является использование антисептических средств с широким спектром антибактериальной и антимикотической активности с последующей пробиотической контаминацией нормальной вагинальной микрофлоры [15, 40]. При этом с целью профилактики рецидивов инфекционного воспаления слизистой влагалища существенное значение имеет создание условий, в которых вагинальный эпителий способен к наиболее полному восстановлению с поддержанием физиологического гомеостаза, и в этом плане возможным вариантом станет поддерживающая терапия ультранизкими дозами эстрогенов [2, 37, 41].
В настоящее время одними из наиболее эффективных препаратов для локального лечения смешанных вагинитов являются лекарственные средства, содержащие деквалиния хлорид (DQC) – аммониевое соединение с широким антибактериальным и антимикотическим спектром действия [26, 41, 42]. Особенно эффективным считается применение хлорида деквалиния на фоне последующей деконтаминационной терапии [21, 36, 43]. При этом практически нет исследований, оценивающих отсутствие рецидивов вульвовагинита при длительном (более 6 месяцев) мониторинге, что и определило цель нашего исследования: анализ клинической и микробиологической эффективности комплексной местной деконтаминационной (хлорид деквалиния) и контаминационной (ацидофильные лактобактерии в сочетании с ультранизкой дозой эстриола) терапии в лечении рецидивирующих смешанных вагинальных инфекций.
Материалы и методы
Дизайн исследования. Проведено исследование результатов лечения 124 женщин со смешанным вульвовагинитом (шифр по МКБ-10: N89 Другие невоспалительные заболевания влагалища). Средний возраст пациенток составил 30,2 года. База исследования – кафедра акушерства, гинекологии и перинатологии ФГБОУ ВО «Кубанский государственный медицинский университет» Минздрава России, женские консультации г. Краснодара. Обследование проводилось согласно приказу Минздрава РФ №1130н от 20.10.2020 г. «Об утверждении Порядка оказания медицинской помощи по профилю “акушерство и гинекология”».
Критерии включения: рецидивирующая (не менее двух рецидивов в год) инфекция с по крайней мере двумя идентифицированными вагинальными патогенами в концентрации не менее 106 ГЭ/мл (выявленные методом ПЦР); отрицательные результаты исследований, направленных на выявление N. gonorrhoeae, T. vaginalis, C. trachomatis, M. genitalium; наличие информированного добровольного согласия и соблюдение всей процедуры исследования. Всем женщинам, включенным в исследование, было рекомендовано в течение всего времени пользоваться барьерными методами контрацепции (мужские презервативы) и провести санацию половых партнеров.
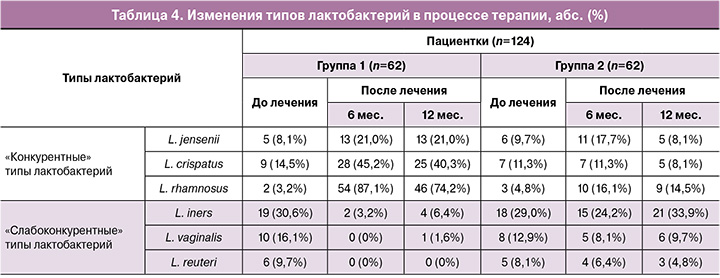
Диагноз «рецидивирующая смешанная вульвовагинальная инфекция» был установлен на основании жалоб (патологические бели (119/124, 95,9% женщин), субъективные ощущения в виде зуда и жжения (81/124, 65,3%), боли при мочеиспускании (36/124, 29%), диспареуния (41/124, 33,1%); объективного гинекологического осмотра (воспалительные изменения слизистых вульвы и влагалища – отечность, гиперемия (117/124, 94,3%), инфильтрация тканей (29/124, 23,4%), мацерация половых губ и аногенитальной зоны (33/124, 26,6%) и комплексного микробиологического исследования.
Женщинам с подтвержденным диагнозом «рецидивирующая смешанная вульвовагинальная инфекция» была назначена комплексная терапия: деквалиния хлорид («Флуомизин», Gedeon Richter, Plc. (Hungary) в партнерстве с Medinova (Switzerland), рег. № ЛСР-008618/09 от 28.10.2009 г.), вагинальные таблетки 10 мг) с последующей контаминацией («Гинофлор Э», Gedeon Richter, Plc. (Hungary) в партнерстве с Medinova (Switzerland), рег. № ЛСР-008765/09 от 28.03.2017 г.), вагинальные таблетки, содержащие лиофилизат ацидофильных лактобактерий (не менее 1×108 КОЕ) и эстриол (30 мкг).
Все пациентки были методом слепой выборки разделены на 2 группы в зависимости от продолжительности контаминационной терапии: I (основная) группа (n=62) получала местную терапию препаратом деквалиния хлорида (таблетки вагинальные 10 мг) 1 раз в день №6 и контаминационную «Гинофлор Э» (таблетки вагинальные, содержащие эубиотик + эстроген) терапию 1 раз в день №6. Деконтаминационная терапия в основной группе проводилась с 7-го по 13-й дни менструального цикла, контаминационная – с 14-го по 19-й дни (на протяжении 3 последовательных циклов); II (сравнения) группа (n=62) – те же препараты, но контаминация проводилась по стандартной схеме: «Гинофлор Э» 1 раз в день №6 в течение 1 менструального цикла.
Методы исследования и контроль эффективности лечения. Клинико-анамнестическое обследование; бактериоскопия отделяемого из цервикального канала и влагалища с оценкой окрашенного по Граму мазка по критериям Hay/Ison (от 0 до 4-й степени); ПЦР в режиме реального времени для определения условно-патогенной микрофлоры (ПЦР-РВ) – «Фемофлор 16» (OOO «НПO ДНK-Технология», Москва); pH-метрия вагинального содержимого (кольпотест). Определение вида выделенных лактобацилл проводилось с использованием метода времяпролетной матрично-активированной лазерной дезорбции/ионизации масс-спектрометрии на масс-спектрометре MALDI-ToF Microflex (Bruker Daltonics, Германия).
Определение клинической эффективности проводилось через 14 дней, 6 и 12 месяцев после окончания лечения: микроскопическое исследование вагинальных мазков (окраска по Граму с оценкой по критериям Hay/Ison) и оценка нормализации вагинальной микрофлоры по результатам ПЦР.
Статистический анализ
Статистическая обработка проводилась с помощью программы STATISTICA 10,0. Описание количественных признаков представлено в виде абсолютных (количество) и относительных (%) величин.
Результаты
Микробиологическая характеристика пациенток
Как уже говорилось, субъективные и объективные симптомы соответствовали клинической картине рецидивирующей вульвовагинальной инфекции смешанного типа (среднее количество рецидивов 2,6 в год). pH вагинального содержимого варьировал в широких пределах – от 5,3 до 6,9 (в среднем 6,4). Вагинальная микроскопическая картина также была достаточно разнообразной, но во всех случаях соответствовала понятию дисбиоза: выявлены «ключевые клетки» – у 85/124 (68,5%) женщин, мицелий и клетки дрожжевых грибов – у 59/124 (47,6%), Mobiluncus и Leptotrichia – у 61/124 (49,2%), а Lactobacillus spp. (более 5 в поле зрения) визуализировались в 39/124 (31,4%) мазках. Оценка микробиоты по критериям Hay/Ison показала 2-ю (промежуточную) степень у 19/124 (15,3%) пациенток, 3-ю и 4-ю степени (бактериальный/анаэробный вагиноз) – в 55/124 (44,4%) и 50/124 (40,3%) случаях соответственно (рис. 1).
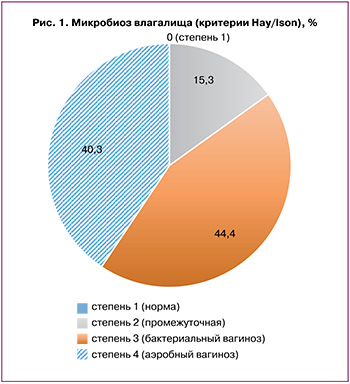
Анализ микробиома влагалища методом ПЦР показал преобладание факультативно- и облигатно-анаэробных микроорганизмов (более 104 ГЭ/мл): Gardnerella vaginalis – у 81/124 (65,3%), Atopobium vaginae – 51/124 (41,1%), Mobiluncus spp. – 44/124 (35,5%) и Bacteroides spp. – 44/124 (35,5%); кокковая микрофлора (Грам+/-) обнаружена у 42/124 (33,9%) пациенток.
Проведенная в исследовании идентификация таксономии лактобактерий (масс-спектрометрия) показала превалирование у пациенток со смешанными вульвовагинальными инфекциями «слабоконкурентных» с условно-патогенной микрофлорой типов лактобактерий (в среднем 19,6%) над «конкурентными» (9,5%). Наиболее часто обнаруживались L. iners (29,7%) и L. vaginalis (15,3%) (рис. 2).
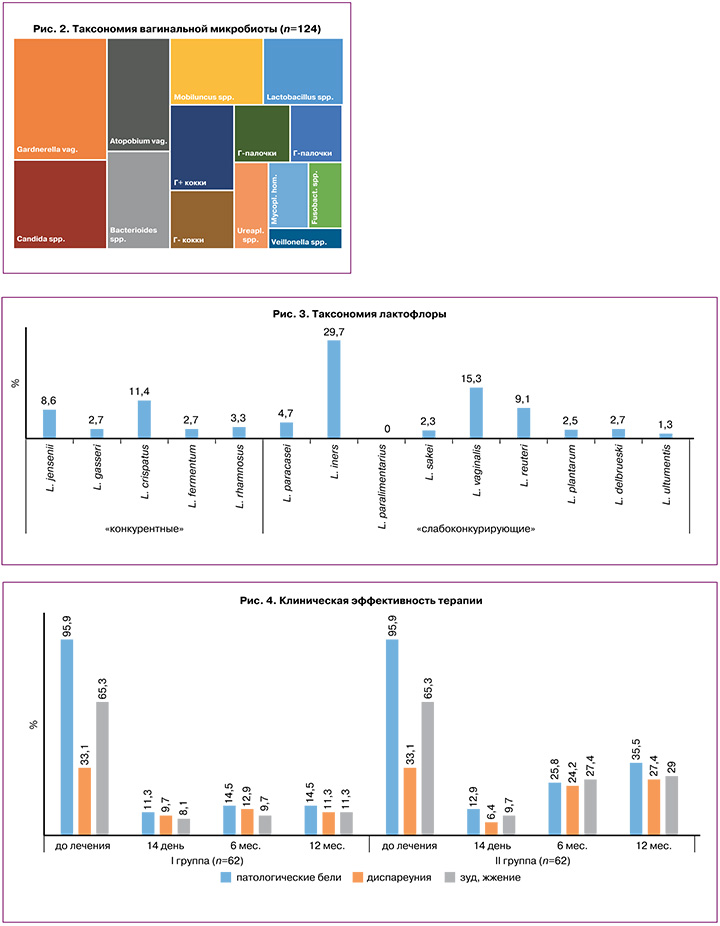
Клиническая эффективность
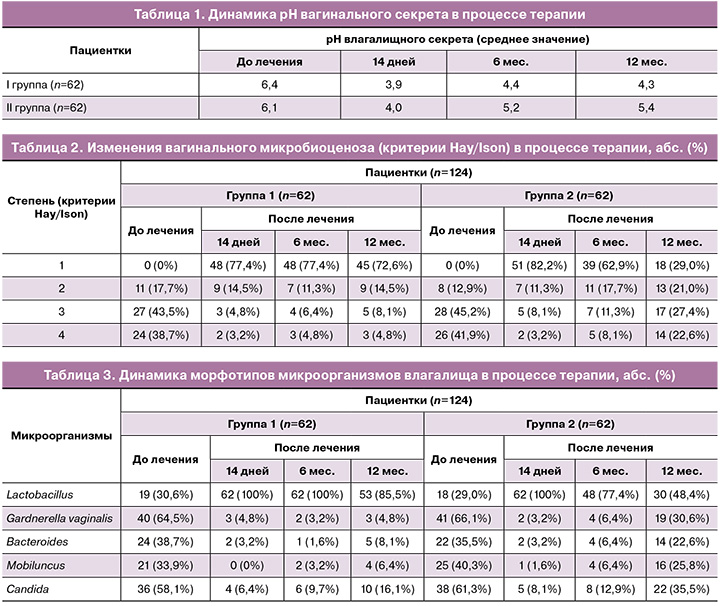
Через 14 дней после окончания лечения в группах отмечено снижение частоты выявления субъективных и объективных симптомов вульвовагинальной инфекции: зуд, жжение в области наружных половых органов и преддверия влагалища исчезли у 109/124 (87,9%) женщин; патологические бели – у 113/124 (91,1%) пациенток двух групп (различия между группами на данном сроке не определены ввиду идентичности проводимой терапии) (рис. 3). Данное нивелирование клинических симптомов может свидетельствовать о правильной тактике выбора деконтаминационной и контаминационной терапии пациенток со смешанными формами вульвовагинальных инфекций. Через 6 месяцев после окончания лечения зарегистрированы существенные различия между группами, что было, по-видимому, связано с возникшими рецидивами на фоне прекращения контаминации влагалища лактофлорой. Так, в группе сравнения (II) вагинальный дискомфорт в виде зуда и диспареунии возобновился соответственно у 17/62 (27,4%) и 15/62 (24,2%) пациенток, а патологические бели различного характера, часто сопровождающиеся неприятным запахом, – у 16/62 (25,8%) пациенток. Тогда как в I группе данная клиническая симптоматика (зуд, диспареуния и патологические бели) через 6 месяцев была отмечена у 6/62 (9,7%), 8/62 (12,9%) и 9/62 (14,5%) пациенток соответственно.
При этом в I группе (с более длительной контаминацией лактобациллярной флорой с микродозами эстрогена) количество пациенток, жалующихся на данную клиническую картину, составило 9,7% (зуд, жжение), 12,9% (диспареуния) и 14,5% (патологические выделения из половых путей), то есть по сравнению со II группой эффективность лечения на данном сроке мониторинга была выше в среднем в 2,1 раза. При дальнейшем наблюдении (в течение 1 года) клинические рецидивы вульвовагинальных инфекций зарегистрированы у 7/62 (11,3%) женщин I группы и 19/62 (30,6%) II группы.
После лечения (14-е сутки) pH вагинального секрета в двух группах снизился и составил в среднем 4,0 (табл. 1).
Бактериоскопическая оценка состояния микрофлоры влагалища (критерии Hay/Ison) через 14 дней после лечения показала норму (степень 1) у 99/124 (79,8%) пациенток, степень 3 (бактериальный вагиноз) – у 8/124 (6,5%) и степень 4 (аэробный вагиноз) – у 4/124 (3,2%) женщин. Через 6 месяцев количество пациенток с 3-й и 4-й степенью в I группе составило 7/62 (11,3%), а во II группе – 12/62 (19,4%) (табл. 2). При годичном мониторинге отмечено увеличение количества пациенток с 3-й и 4-й степенью микробиоценоза во II группе – 31/62 (50,0%) (в I группе – 8/62 (12,9%)).
Микробиологическая оценка терапии при смешанной вульвовагинальной инфекции в двух группах показала высокую антибактериальную эффективность хлорида деквалиния: через 2 недели после лечения зарегистрирована эрадикация Gardnerella vaginalis у 119/124 пациенток, что составило 96%, Bacteroides spp. и Atopobium vaginae – у 120/124 (96,8%) пациенток, Mobiluncus spp. был обнаружен лишь у 1/124 (0,8%) пациентки. Также отмечен высокий уровень полной эрадикации грибов рода Candida spp. – у 115/124 (92,7%) пациенток и количества Г+ и Г- микрофлоры женщин. Лактобациллярная микрофлора в этот период наблюдения определялась у всех женщин. При этом наблюдение в течение 6 месяцев не показало значимого увеличения условно-патогенной вагинальной микрофлоры (табл. 3). По нашему мнению, значимые различия между группами были получены через 12 месяцев: отмечено увеличение количества рецидивов вульвовагинальной инфекции с детекцией Gardnerella vaginalis у 19/62 (30,6%) пациенток II группы (при этом в I группе таких женщин было 3/62 (4,8%) – в 6,4 раза меньше), Bacteroides spp. – у 14/62 (22,6%) (в I группе – 5/62 (8,1%) – в 2,8 раза меньше), Mobiluncus spp. — у 16/62 (25,8%) (в I группе – 4/62 (6,4%) – в 4 раза меньше), грибы рода Candida во II группе отмечены у 22/62 (35,5%) пациенток (в I группе – 10/62 (16,1%) – в 2,2 раза меньше).
Видовая идентификация (генотипирование) лактобактерий проводилась через 6 и 12 месяцев после терапии – зафиксировано ожидаемое повышение колонизации лактобактериями до 106-7 КОЭ/мл на фоне снижения колонизации эпителия факультативными и облигатными микроорганизмами до 104 КОЭ/мл. Число «конкурентных» штаммов лактобацилл в I группе в среднем составило 85,6% (в основном за счет доминирования L. rhamnosus (80,6%) и L. crispatus (42,7,8%)), во II группе количество «конкурентных» штаммов составило 21,2%, то есть в 3,8 раза меньше (табл. 4).
На фоне пролонгированной деконтаминационной терапии (эубиотик+эстроген в течение трех менструальных циклов) в I группе в течение 6 месяцев наблюдения «слабоконкурентные» штаммы лактобацилл определялись у 3,2% пациенток (L. iners), а через 12 месяцев их количество увеличилось до 8,0% (к L. iners присоединилось некоторое количество L. vaginalis). Во II группе на данных сроках мониторинга количество «слабоконкурентных» штаммов составило соответственно 38,7 и 48,4% (в основном за счет L. iners). Соотношение «конкурентных» и «слабоконкурентных» лактобактерий через 12 месяцев после лечения в I группе составило 1:10,7, во II группе – 2,3:1, то есть в группе с более коротким курсом деконтаминационной терапии доминирующей стала «слабоконкурентная» лактофлора, которая может способствовать развитию дисбиотических нарушений во влагалище с рецидивами заболевания.
Клиническая безопасность
У 5/124 (4,0%) женщин, получавших предлагаемую терапию, были зарегистрированы нежелательные побочные явления в виде повышенного количества вагинальных выделений, вульвовагинального зуда и ощущения жжения во влагалище. При этом всеми респондентами эти эффекты признаны незначительными и не требующими прекращения лечения.
Таким образом, мы согласны с мнением ряда авторов в том, что при лечении смешанных вагинитов предпочтительно назначать антибактериальные препараты широкого спектра действия [23, 40]. При этом важной составляющей является длительность как деконтаминационной, так и контаминационной терапии [2, 8, 14, 32].
Заключение
По нашему мнению, выбор оптимальной полиэтиологичной локальной антибактериальной терапии способствует качественной элиминации условно-патогенной микрофлоры, но при этом полностью не может решить проблемы нарушенного вагинального биотопа и системы местного иммунного и гормонального статуса. В данном случае выбор падает на пролонгированное применение пробиотиков, что способствует стабилизации клеточного иммунитета слизистой, качественной контаминации влагалища «конкурентными» лактобактериями, а вхождение в состав некоторых пробиотиков с ультранизкой дозой эстрогена («Гинофлор Э») ведет к улучшению репаративных свойств эпителиоцитов.
Проведенное нами исследование показало, что длительный курс контаминационной терапии препаратом, содержащим комбинацию лактобактерий с ультранизкой дозой эстрогена, способствующую адгезии лактобацилл к влагалищному эпителию, на фоне местного эмпирического лечения препаратом хлорида деквалиния («Флуомизин») предпочтителен для пациенток с рецидивирующим течением вагинальных инфекций. Это подтверждают результаты его эффективности при годовом мониторинге: клинической – рецидивы в группе с трехкурсовым применением пробиотиков встречались в 2,5 раза реже, чем в группе пациенток со стандартным однокурсовым лечением (12,4% против 30,6%), и микробиологической – отсутствие условно-патогенной микрофлоры (Gardnerella vaginalis, Bacteroides spp., Atopobium vaginae и Mobiluncus spp.) было зарегистрировано более чем в 5 раз чаще в группе с пролонгированной контаминационной терапией, также в этой группе в 6 раз реже выявлялись «слабоконкурентные» штаммы лактобактерий.



