Современное определение задержки роста плода включает в себя невозможность реализации плодом своего биологического потенциала роста в результате дисфункции плаценты, которая носит полиэтиологичный характер [1, 2]. У новорожденных с задержкой роста или малым весом отмечаются высокая частота неонатальной заболеваемости и смертности, а также более высокий риск развития метаболических, сердечно-сосудистых, нервно-психических заболеваний в более взрослом возрасте [1]. Основным методом диагностики задержки роста плода на антенатальном этапе является ультразвуковое исследование с оценкой допплерометрических показателей. Принятые в клинической практике критерии, разработанные международным консенсусом в рамках протокола Delphi на основании клинических, эхографических и патологических допплерографических характеристик, позволяют диагностировать ранний и поздний фенотипы задержки роста плода [3]. Следует отметить, что в 75% случаев задержка роста или маловесный для срока гестации плод остаются невыявленными вплоть до родоразрешения [4]. Единственным «золотым стандартом» диагностики задержки роста плода является постнатальное подтверждение массы и длины тела при рождении [5, 6]. В настоящее время еще более сложным является вопрос дифференциальной диагностики между маловесным к сроку гестации плодом и задержкой его роста [7].
Таким образом, своевременная диагностика различных фенотипов, поиск значимых отличий задержки роста и маловесного к сроку гестации плода являются одними из ведущих задач современного акушерства. Одним из возможных путей решения данной проблемы является внедрение новых omics-технологий, включая использование метаболомики, которая обладает научным потенциалом не только для изучения патогенеза задержки роста плода, но и для создания новых, доступных для использования в клинической практике неинвазивных биомаркеров.
Цель исследования: определить критерии диагностики задержки роста плода на основании количественного протеомного анализа плазмы крови беременной.
Материалы и методы
В пилотное исследование «случай-контроль» были включены 50 беременных, наблюдавшихся и родоразрешенных в ФГБУ «Национальный медицинский исследовательский центр акушерства, гинекологии и перинатологии имени академика В.И. Кулакова» Минздрава России с 2019 по 2021 гг. Было сформировано 5 групп: I, II и V – основные группы, III и IV – группы сравнения. Группу I составили пациентки с ранней формой задержки роста плода (<32 недель) (n=10), группу II – с поздней формой задержки роста плода (≥32 недель) (n=10), группы III и IV – беременные, родоразрешенные до и после 32 недель (n=10/n=10), с нормальными массо-ростовыми показателями и группу V – пациентки с маловесным к сроку гестации плодом (≥32 недель) (n=10).
Для обеспечения максимальной точности определения протеома проводился индивидуальный подбор пары образцов плазмы крови беременных «основная группа/группа сравнения» (критерий: срок беременности на момент родоразрешения).
Критериями включения в исследование явились: возраст от 18 до 45 лет, одноплодная беременность, антенатально установленный диагноз «задержка роста плода», «маловесный к сроку гестации плод» (согласно диагностическим ультразвуковым и допплерометрическим критериям Delphi, а также клиническим рекомендациям Минздрава России «Недостаточный рост плода, требующий предоставления медицинской помощи матери (задержка роста плода)» [2]) – для основных групп, размеры плода, соответствующие сроку беременности, – для групп сравнения.
Критериями исключения являлись: многоплодная беременность, хромосомная патология и пороки развития плода, тяжелая экстрагенитальная патология, гипертензивные расстройства во время беременности, преэклампсия.
Постнатально была проведена оценка массо-ростовых показателей у новорожденных (n=50), согласно центильным кривым INTERGROWTH-21, для подтверждения антенатального диагноза задержки роста и маловесного плода, а также нормальной массы тела в группе сравнения (преждевременные роды до 32 и после 32 недель).
На проведение исследовательской работы было получено одобрение Этического комитета, все пациентки подписали добровольное информированное согласие.
Образцы плазмы венозной крови женщин групп I, II, V получены в день родоразрешения, групп III и IV – в день родоразрешения в сроке, соответствовавшем сроку родоразрешения в группах I, II и V. Образцы венозной крови (пробирки с EDTA) центрифугированы при 300 g и 4°C 20 минут, супернатант повторно центрифугировался при 12 000 g 10 минут, затем образцы замораживались и хранились при -80°C. Количественный анализ 125 белков плазмы крови проводили с использованием набора BAK 125 (MRM Proteomics Inc, Монреаль, Канада) методом высокоэффективной жидкостной хроматографии с тандемной масс-спектрометрией (ВЭЖХ-МС/МС) в режиме мониторинга множественных реакций (ММР). Подготовку проб и последующий анализ ВЭЖХ-МС проводили в соответствии с протоколом производителя [8]. МС/МС-анализ выполнен на масс-спектрометре QTRAP SCIEX6500+ (SCIEX, Канада). Программное обеспечение Skyline Quantitative Analysis использовалось для визуального изучения данных LC-MRM MS. Калибровочные кривые были построены с использованием взвешенной линейной регрессии 1/x2 и использованы для расчета концентраций пептидов в образцах (фмоль/мкл плазмы).
Статистический анализ
Статистический анализ проводился с использованием программ Statistica 12.6, IBM SPSS Statistics 21. Оценка соответствия нормальному распределению количественных показателей проводилась с помощью критерия Шапиро–Уилка. При нормальном распределении описание проводилось с помощью средних арифметических величин (M), стандартных отклонений (SD). При отличном от нормального распределении – с помощью медианы (Me) и нижнего и верхнего квартилей [Q1; Q3]. Категориальные данные описывались с указанием абсолютных значений и процентных долей. Сравнение трех и более групп по количественному показателю (нормальное распределение) выполнялось с помощью однофакторного дисперсионного анализа, апостериорные сравнения проводились с помощью критерия Тьюки (при условии равенства дисперсий), критерия Геймса–Хауэлла (при неравных дисперсиях), при ненормальном распределении – с помощью критерия Краскела–Уоллиса и критерия Данна. Сравнение двух групп по количественному показателю осуществлялось с помощью критерия Стьюдента для нормального распределения и с помощью критерия Манна–Уитни – для ненормального распределения. Сравнение процентных долей при анализе многопольных таблиц сопряженности выполнялось с помощью критерия хи-квадрат Пирсона. Различия между сравниваемыми величинами признавали значимыми при уровне статистической значимости p<0,05. Диагностические модели на основе логистической регрессии были созданы после предварительного процессинга данных для классификационных задач «ранняя задержка роста плода/ранний контроль», «поздняя задержка роста плода/поздний контроль», «поздняя задержка роста плода/маловесный к сроку гестации» [9, 10]. Для создания моделей на основе логистической регрессии был сформирован набор данных, включающий в качестве независимых переменных линейные значения концентраций белков, результат попарного умножения концентраций белков и квадраты значений концентраций белков. В качестве переменных отклика были обозначены группы пациенток, причем для задачи «ранняя задержка роста плода/ранний контроль»: 0 – ранний контроль, 1 – ранняя задержка роста плода; для задачи «поздняя задержка роста плода/поздний контроль»: 0 – поздний контроль, 1 – поздняя задержка роста плода; для задачи «поздняя задержка роста плода/маловесный к сроку гестации»: 0 – маловесный плод, 1 – поздняя задержка роста плода. Потенциальные переменные для модели были предварительно выбраны с использованием ортогональных проекций дискриминантного анализа на латентные структуры и выбора важности переменных (с порогом VIP больше 1). Логистическая регрессия проводилась путем пошагового добавления переменных с целью минимизации информационных критериев Акаике (AIC), при этом гарантируя, что коэффициенты маркеров имели ненулевую вероятность ниже 0,05. Затем переменные исключались шаг за шагом, начиная с переменной с наибольшей ненулевой вероятностью, пока ни один из коэффициентов маркеров не имел ненулевую вероятность выше 0,05. Качество моделей оценивали с помощью перекрестной проверки с исключением по отдельным объектам, а оптимальный порог определяли путем максимизации суммы чувствительности и специфичности. Для оценки диагностической значимости признаков при прогнозировании определенного исхода применялся метод анализа ROC-кривых с определением площади под ней (AUC). При соответствии AUC значениям 0,9–1,0 информационная ценность оценивалась критерием качество «отличное»; AUC 0,8–0,9 – качество «очень хорошее»; AUC 0,7–0,8 – «хорошее» качество; AUC 0,6–0,7 – «среднее» качество; AUC 0,5–0,6 – «неудовлетворительное» качество. Прогностическая значимость построенных моделей характеризовалась чувствительностью (Se) и специфичностью (Sp).
Результаты
Все пациентки, включенные в исследование, были сопоставимы по следующим клинико-анамнестическим характеристикам: по возрасту (p=0,39 по тесту Геймса–Хауэлла), индексу массы тела (ИМТ) (p=0,16 по тесту Геймса–Хауэлла), способу наступления беременности (p=0,43 по тесту хи-квадрат Пирсона). Статистически значимых различий в частоте соматических и гинекологических заболеваний не выявлено. Также не было различий в частоте тромбофилических мутаций низкого и высокого риска (p=0,52 и p=0,54 соответственно по тесту хи-квадрат Пирсона). Случаев антенатальной гибели плода в исследуемых группах не выявлено (табл. 1).
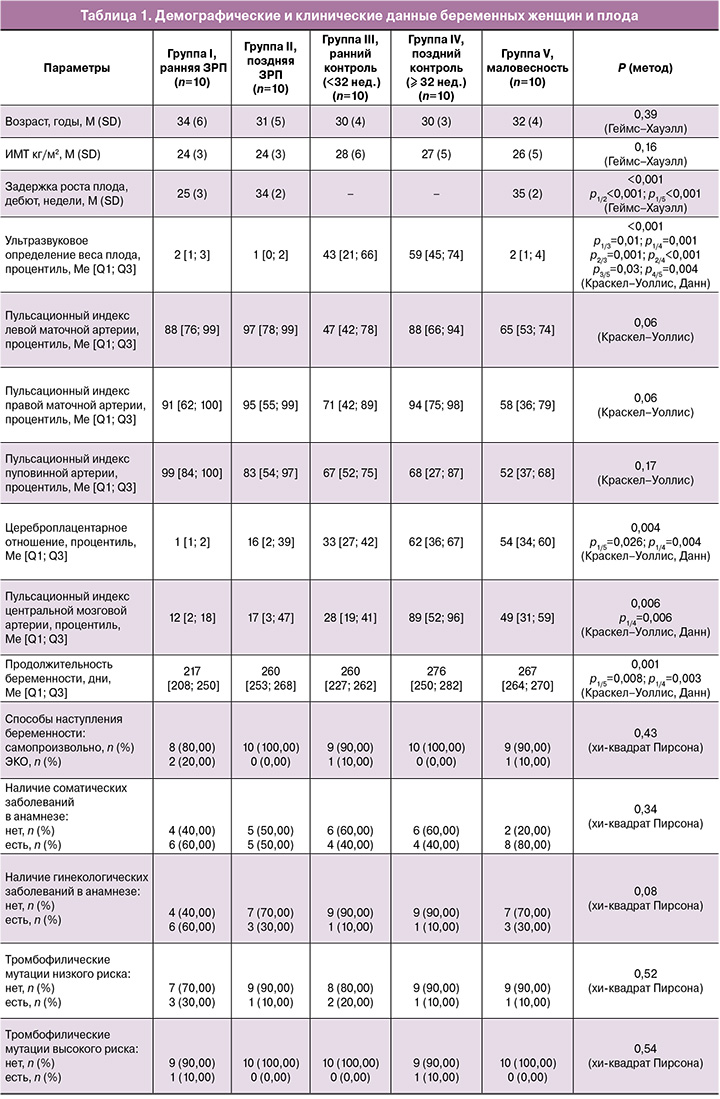
При анализе течения беременности особый интерес представляло изучение изменений ультразвуковых и допплерометрических показателей. Следует отметить, что снижение показателя предполагаемой массы плода (оценка в процентилях), нарушения кровотока по данным допплерометрии (пульсационных индексов в маточных артериях, в артерии пуповины, средне-мозговой артерии, церебрально-плацентарного отношения) чаще встречались и имели более выраженные изменения в группах с задержкой роста плода (чаще при ранней форме). По мнению ряда авторов, несмотря на то, что проведение ультразвукового исследования и допплерометрии является основным инструментом для диагностики и постановки диагноза, в ряде случаев антенатально данные методы не позволяют выявить задержку роста плода [4–6]. Следует отметить, что даже при небольшой выборке при проведении данного исследования в 10% случаев в группе ранней формы, в 20% наблюдений – при поздней форме задержки роста плода и в 30% случаев в группе маловесных к сроку гестации антенатально допплерометрических и ультразвуковых признаков не было выявлено. Полученные результаты подтверждают данные литературы о недостаточной чувствительности и специфичности функциональных методов диагностики задержки роста плода и обосновывают необходимость поиска новых неинвазивных критериев [2, 4, 5].
Было проведено количественное определение уровней 125 белков плазмы крови (набор BAK 125, MRM Proteomics Inc, Монреаль, Канада) беременных женщин при родоразрешении методом ВЭЖХ-МС/МС-ММР с внутренними стандартами. Данные белки относятся к мажорным и среднепредставленным белкам крови, составляя более 99% всей белковой массы. Различие в концентрациях исследованных белков в плазме составило 6 порядков. Большинство данных белков являются маркерами сердечно-сосудистых, онкологических и нейродегенеративных заболеваний [8, 11, 12].
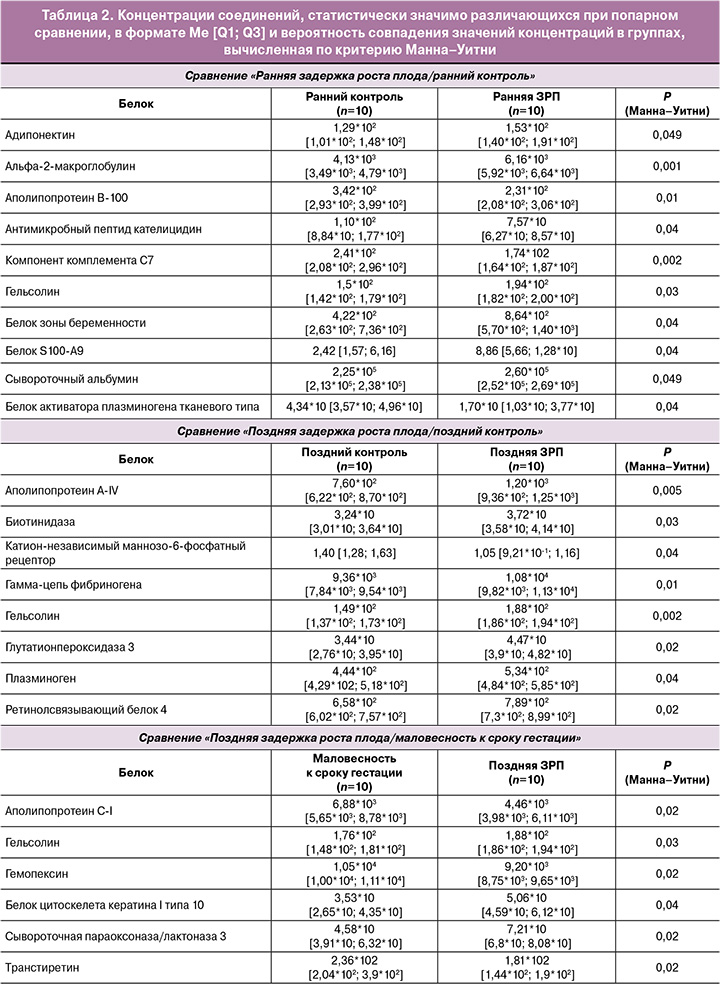
В группе I (ранняя форма задержки роста плода), в отличие от группы III (группа сравнения менее 32 недель), отмечено статистически значимое повышение уровней адипонектина (ADIPOQ), альфа-2-макроглобулина (A2M), гельсолина (GSN), белка S100-A9 (S100A9), сывороточного альбумина (ALB) и белка зоны беременности (PZP) и снижение уровней аполипопротеина В-100 (APOB100), антимикробного пептида кателицидина (ЦАМФ, CAMP), компонента комплемента С7 (C7) и активатора плазминогена тканевого типа (PLAT). При поздней форме задержки роста плода (группа II) в плазме крови матери наблю далось повышение уровней аполипопротеина A-IV (APOA4), биотинидазы (BTD), гамма-цепи фибриногена (FGC), гельсолина (GSN), глутатионпероксидазы 3 (GPX3), плазминогена (PLG) и ретинол-связывающего белка 4 (RBP4), а также снижение катион-независимого маннозо-6-фосфатного рецептора (CI-MPR). Значимые изменения в протеоме плазмы крови при сравнении поздней формы задержки роста плода (группа II) с группой «маловесный к сроку гестации плод» (группа V) были связаны с увеличением уровня гельсолина (GSN), сывороточной параоксоназы/лактоназы 3 (PON3), белка цитоскелета кератина I типа 10 (KRT10), аполипопротеина C-I (APOC1), гемопексина (HPX) и транстиретина (TTR) (табл. 2).
На основании результатов количественного протеомного анализа 125 белков плазмы крови матери были разработаны три диагностические модели с использованием метода логистической регрессии (рисунок, табл. 3).
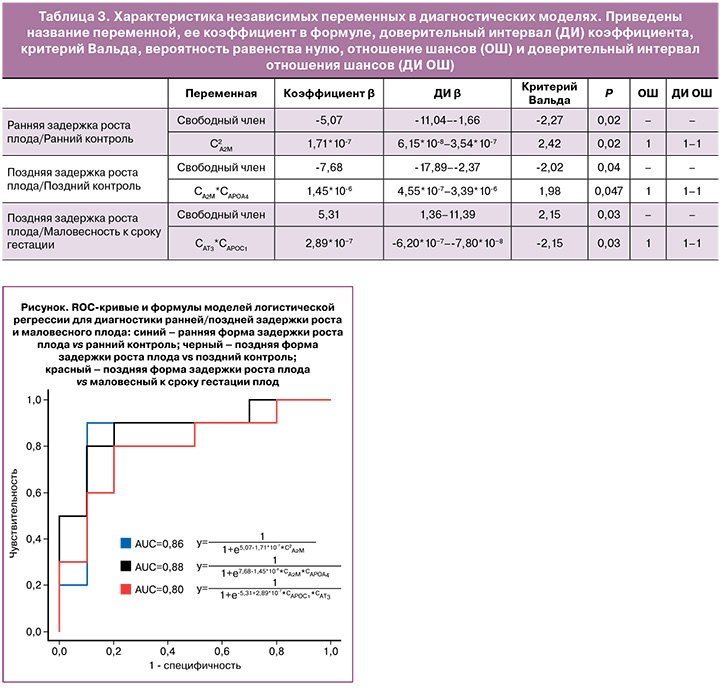
Модель «1» (AUC=0,86) для диагностики ранней формы задержки роста плода, включающая альфа-2-макроглобулин в качестве переменной, имеет формулу:

Чувствительность данной модели составила 90%, специфичность – 90%.
Модель «2» (AUC=0,88) для диагностики поздней формы задержки роста плода включала в качестве переменной белки альфа-2-макроглобулин и аполипопротеин A-IV и имеет формулу:
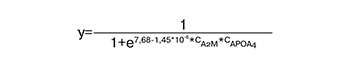
Чувствительность данной модели составила 90%, специфичность – 80%.
Модель «3» (AUC=0,80) была создана для проведения дифференциальной диагностики между поздней формой задержки роста и маловесным к сроку гестации плодом, включила в себя белки антитромбин-III и аполипопротеин C-I и имеет формулу:
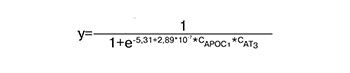
Чувствительность данной модели составила 80%, специфичность – 80%.
Обсуждение
Задержка роста плода является одной из самых изучаемых проблем современного акушерства. Особый интерес представляет поиск неинвазивных или малоинвазивных методов диагностики и возможного прогнозирования данного осложнения. По данным Sovio U. et al. [13], классическое измерение высоты дна матки с использованием сантиметровой ленты во время беременности и направление астеничных женщин и/или имеющих факторы риска формирования задержки роста/маловесного плода на ультразвуковое исследование позволяет заподозрить и выявить только в 20% случаев маловесный плод, а проведение ультразвукового исследования в III триместре беременности с оценкой фетометрических показателей имеет чувствительность 52–57% [14]. Внедрение в практику определения церебрально-плацентарного отношения, по данным [15, 16], должно было улучшить дифференциальную диагностику между задержкой роста и маловесным плодом. Однако в многоцентровом проспективном исследовании Morales-Roselló J. et al. [17] было показано, что в группе низкого риска (физиологически протекающая беременность) эффективность определения церебрально-плацентарного отношения для диагностики задержки роста/маловесного плода была умеренной. Вышеизложенное обусловило проведение исследований по поиску новых клинико-лабораторных критериев задержки роста плода. Несмотря на большое количество исследований в области транскриптомики (микроРНК), эпигенетики, липидомики и других omics-направлений, вклад открытых и изученных генов, биологически активных молекул в диагностику задержки роста плода недостаточно изучен.
На сегодняшний день идентифицировано более 2000 микроРНК человека, мишенями которых являются более 60% генов, кодирующих белки человека [18, 19]. Однако микроРНК не обладают специфичностью, так как могут регулировать активность не только нескольких генов, но и матричных РНК [20]. Применение данных, полученных в ходе эпигенетических исследований, является достаточно перспективным в перинатальной медицине в качестве прогностических маркеров развития задержки роста плода. Однако, как и в случае с микроРНК, в настоящее время сложно выделить из множества молекул специфичные для данной патологии [20]. Было предпринято много усилий для раннего выявления или прогнозирования задержки роста плода на ранних сроках беременности с определением β-хорионического гонадотропина человека (β-ХГЧ), связанного с беременностью белка плазмы-А (PAPP-A), плацентарного фактора роста (PlGF) и растворимой fms-подобной тирозинкиназа-1 (sFlt-1). К сожалению, при изолированном использовании ценность данных биомаркеров в прогнозировании задержки роста плода довольно низка. Многими исследователями было показано, что комплексное определение маркеров материнской сыворотки (β-ХГЧ, PAPP-A, PlGF, sFlt-1) при сочетании с показателями допплерометрии в группе высокого риска (задержка роста плода и преэклампсия) повышает эффективность прогнозирования неблагоприятных исходов [22–24]. В 2012 г. впервые стала появляться информация о метаболических процессах, вовлеченных в патогенез задержки роста плода [25]. Метаболомное профилирование, несмотря на относительную ограниченность данных, предполагает точность в определении различий между задержкой роста и маловесным плодом [26, 27]. В ранее проведенных исследованиях отмечены четкие различия между группами с и без задержки роста плода, и отсутствуют данные о различиях между поздней формой задержки роста и маловесным к сроку гестации плодом. Также обращает на себя внимание «клиническая» неоднородность беременных и новорожденных, включенных в исследование, а также аналитические подходы (качественная протеомика) [24]. Проведенное нами исследование имело сильные и слабые стороны. Следует отметить однородность групп как сильный аспект работы: все включенные беременные входили в исследование исключительно проспективно при строгом соблюдении критериев включения/исключения. Однако необходимо учитывать тот факт, что настоящее исследование проведено на небольшом объеме выборки и требует проверки наших результатов на более крупных когортах. В настоящем исследовании впервые проведен количественный протеомный анализ белков материнской крови при различных формах задержки роста и маловесного плода при сопоставлении с группами сравнения без задержки роста плода. Результаты настоящего исследования показывают, что нарушения в основной группе (задержка роста плода) при сопоставлении с группами сравнения происходят в липидном обмене и иммунных реакциях, что согласуется с проведенными раннее исследованиями [28–30]. При анализе особенностей протеомного профиля крови беременных с задержкой роста и маловесным плодом наблюдался не только одинаковый характер изменений, но также имелись значительные различия между группами в зависимости от фенотипа задержки роста плода. Полученные результаты согласуются с данными Priante E. et al. [24] и Miranda J. et al. [28], предполагающих, что у маловесных плодов имеют место в большей степени метаболические нарушения при сохраненной дыхательной функции плаценты, приводящие к недостаточному питанию и реализации долгосрочных нарушений в дальнейшем (в том числе и метаболических). Разработанные модели позволяют с чувствительностью и специфичностью 80% и 90% проводить дифференциальную диагностику между ранней и поздней формами задержки роста и маловесными к сроку гестации плодами.
Заключение
Результаты данного исследования могут быть использованы в формировании подходов к новым методам диагностики различных форм задержки роста и маловесного плода, а также явиться отправной точкой для будущих исследований по изучению, в том числе, потенциальных терапевтических мишеней.



