В настоящее время во всем мире сохраняется тенденция к увеличению частоты кесарева сечения (КС), достигающей в некоторых странах 40,5% [1, 2]. В России в 2020 г. этот показатель составил 30,3% [3].
В связи с увеличением количества КС отмечается повышенный интерес как к оценке состояния рубца во время беременности и в родах, так и к выявлению и изучению дефектов рубца на матке (РМ) после КС вне беременности.
Дефект рубца следует определять как истончение зоны рубца по сравнению с прилежащим интактным миометрием. Он может быть с образованием ниши или без таковой [4].
Дефект РМ может быть причиной нарушений менструальной функции, хронической тазовой боли, вторичного бесплодия, эктопической беременности в рубце, врастания и предлежания плаценты, разрыва матки.
В связи с этим особенно важна точная оценка состояния РМ вне беременности с целью своевременной хирургической коррекции выраженных дефектов.
Наиболее доступными и распространенными методами исследования являются ультразвуковые методы (2D и 3D ультразвуковое исследование (УЗИ), а также эхогистеросальпингография (ЭхоГСГ) с использованием контрастных сред) [5–7].
Еще одним информативным и доступным методом диагностики является магнитно-резонансная томография (МРТ), которая позволяет достаточно точно оценить все параметры РМ, в том числе анатомические характеристики рубцовой зоны. Также возможно применение МРТ с контрастированием с целью оценки перфузионного кровотока в зоне рубца [8–14].
Среди специалистов нет единого мнения относительно преимуществ и недостатков данных методов, общепринятой методики измерения и, соответственно, нет признанного «золотого стандарта» диагностики дефектов РМ.
Целью нашей работы стало повышение эффективности оценки состояния РМ после КС на основании сравнения различных методов исследования.
Материалы и методы
Это сравнительное исследование проводилось на базе ФГБУ «Национальный медицинский исследовательский центр акушерства, гинекологии и перинатологии имени академика В.И. Кулакова» Министерства здравоохранения России (НМИЦ АГиП). В группу исследования была включена 61 пациентка с РМ после операции КС в нижнем маточном сегменте (после последнего КС прошло более 1 года), заинтересованная в повторной беременности. Критериями включения являлись: возраст пациенток от 18 до 45 лет; планирование беременности; подозрение на истончение РМ после операции КС в нижнем маточном сегменте; подписанное информированное согласие на участие в исследовании. Критериями исключения являлись: возраст до 18 лет и старше 45 лет; острые воспалительные заболевания органов малого таза; тяжелые сопутствующие соматические заболевания; злокачественные новообразования [15].
На первом этапе всем пациенткам было выполнено экспертное УЗИ (эУЗИ) органов малого таза. Для дальнейшего диагностического поиска и верификации диагноза на втором этапе всем выполнялась МРТ органов малого таза; 30 пациенткам из них на третьем этапе была выполнена ЭхоГСГ.
эУЗИ выполнялось женщинам в пролиферативную фазу на 5–11-й день менструального цикла с помощью аппарата Samsung WS80А Elite (Samsung Medison, Ю.Корея) трансвагинальным датчиком с частотой 7,5 МГц. Для дальнейшего сравнительного анализа исследования проводились двумя специалистами отделения ультразвуковой и функциональной диагностики НМИЦ АГиП. Первый исследователь – специалист с опытом работы менее 15 лет; второй исследователь – специалист с опытом работы более 25 лет. Проводилось стандартное описание топографии и анатомических особенностей внутренних половых органов [15]. Отдельно проводилось измерение параметров РМ согласно стандартизованной методике, принятой в исследовании Delphi [16]. Измерялись: максимальные длина и глубина ниши (в сагиттальной плоскости); минимальная толщина рубца (мТР) (в сагиттальной плоскости, перпендикулярно серозной оболочке от верхнего внутреннего контура дефекта до серозной оболочки; при этом эндометрий и серозная оболочка не включались в измерение); максимальная ширина ниши (в поперечной плоскости); толщина интактного миометрия (ТИМ) – толщина передней стенки матки рядом с верхним краем ниши (в сагиттальной плоскости).
МРТ проводили на МР-томографе GE Signa 1,5Т HDX фирмы General Electrics (США) с напряженностью магнитного поля 1,5Т, без контрастного усиления, при малом и среднем наполнении мочевого пузыря с получением Т1ВИ, Т2ВИ, Т2FS, FIESTA, выполненных в Sag, Cor, Ax плоскостях. Производилось описание топографии и анатомических особенностей внутренних половых органов, измерение параметров РМ по алгоритму Delphi. Описание снимков и измерение параметров РМ, как и во время УЗИ, производилось двумя независимыми исследователями с различным уровнем подготовки. Первый исследователь – специалист с опытом работы более 25 лет; второй исследователь – специалист с опытом работы менее 10 лет. Полученные первым и вторым исследователями результаты были неизвестны друг другу до окончания измерений.
Дополнительно 30 пациенткам была выполнена ЭхоГСГ с целью уточнения диагноза. ЭхоГСГ проводилась на 7-11 день менструального цикла на ультразвуковом сканере WS80A (Samsung Medison, Ю. Корея) трансвагинальным датчиком с частотой 7,5 МГц по стандартной методике опытным специалистом со стажем работы более 15 лет, специализирующимся на проведении ЭхоГСГ (более 300 исследований ЭхоГСГ) [15]. Выполнялись описание топографии и анатомических особенностей внутренних половых органов, измерение параметров РМ по алгоритму Delphi [16].
Статистический анализ
Статистическая обработка и анализ данных были выполнены с помощью программного обеспечения Microsoft Excel 2010 и STATISTICA 10. Для оценки нормальности распределения данных использовался критерий Колмогорова–Смирнова и Шапиро–Уилка. Данные с нормальным распределением представлены как среднее (стандартное отклонение). Для сравнения полученных данных использовался критерий Стьюдента. Согласованность различных измерений, полученных двумя независимыми исследователями (как при УЗИ, так при МРТ), анализировалась с помощью построения графиков Блэнда–Альтмана [15]. При проверке статистических гипотез значимым считался уровень значимости р<0,05.
Результаты
Средний возраст пациенток составил 35,4 (4,2) года и колебался от 25 до 44 лет. 37 пациенткам в анамнезе было выполнено 1 КС, 19 пациенткам – 2 КС, 5 пациенткам – 3 КС. При выявлении у одной пациентки дефектов нескольких рубцов после КС в исследование включался дефект с наименьшей мТР, при равных значениях мТР – с наибольшими параметрами ниши. На момент исследования у всех женщин после КС прошло более одного года. У 40/61 (65,6%) пациенток последнее КС было выполнено в экстренном порядке, у 21/61 (34,4%) человек – в плановом порядке.
Наиболее частыми клиническими проявлениями дефекта РМ являлись скудные кровянистые выделения из половых путей после менструации – у 39 пациенток (от 2 до 20 дней, в среднем по 7,6 дня); в середине менструального цикла – у 2 пациенток (в среднем по 3,8 дня). Отсутствие наступления беременности при регулярной половой жизни без контрацепции более 1 года отмечали 16 пациенток; альгоменорею, возникшую после КС, – 9 пациенток (табл. 1).
Для сравнения результатов двух методов исследования (эУЗИ и МРТ) был проведен расчет средних значений параметров РМ, полученных двумя независимыми специалистами в каждом методе (табл. 2), и далее проведен сравнительный анализ полученных результатов (табл. 3).
На основании критерия Колмогорова–Смирнова и Шапиро–Уилка в исследуемых группах значения мТР подчинялись закону нормального распределения, а параметры ниши – не подчинялись. Сравнительный анализ измерений мТР и параметров ниши проводился с помощью t-критерия Стьюдента.
При сравнительном анализе данных эУЗИ и МРТ были выявлены статистически значимые различия при измерении мТР. В свою очередь, различия в измерении ширины, длины и глубины ниши не были статистически значимыми (табл. 3).
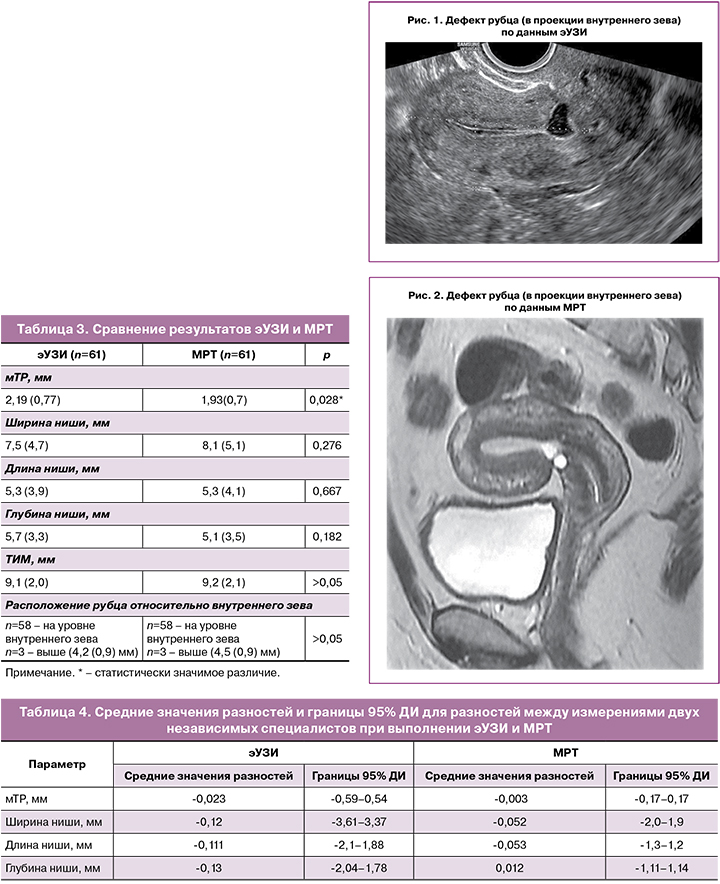
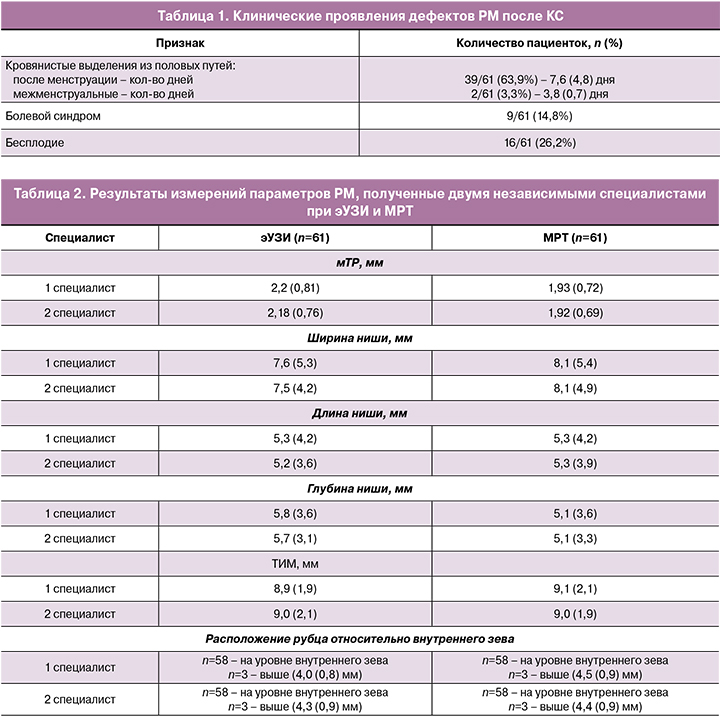
По данным эУЗИ и МРТ рубец на матке определялся в области нижней трети передней стенки матки в 3 случаях, а в остальных случаях – в проекции внутреннего зева (рис. 1, 2).
С целью оценки согласованности измерений одних и тех же параметров, полученных двумя специалистами с разным уровнем подготовки в рамках каждого метода исследования (эУЗИ и МРТ), был проведен сравнительный анализ для независимых переменных, который не выявил статистически значимых различий. В связи с этим был использован анализ Блэнда–Альтмана. Были вычислены средние значения разностей между измерениями двух независимых специалистов, а также верхние и нижние границы 95% доверительного интервала (ДИ) для разностей между измерениями двух исследователей в рамках каждого метода (табл. 4). Чем ближе к «0» были расположены средние значения разностей и чем меньше была ширина 95% ДИ, тем более однородными являлись измерения.
Поскольку основополагающее значение для принятия решения о необходимости хирургической коррекции РМ имеет величина мТР, на основании полученных данных были построены графики Блэнда–Альтмана для определения согласованности измерений именно этого показателя (рис. 3).
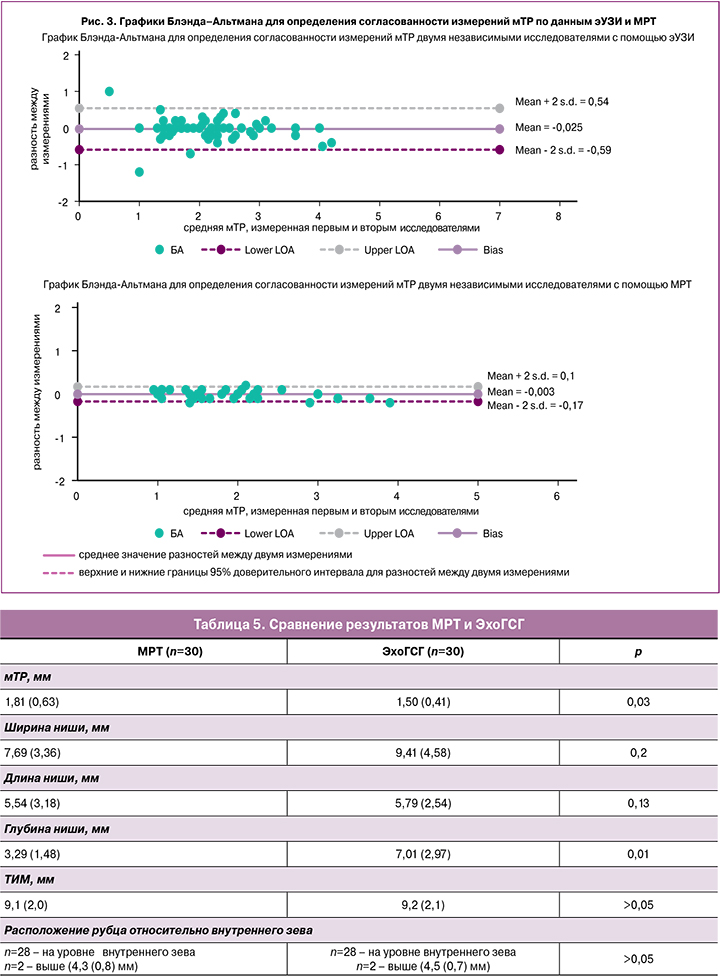
При анализе графиков Блэнда–Альтмана было выявлено, что средняя разность между значениями, полученными первым и вторым исследователем, как при эУЗИ, так и при МРТ, была приближена к 0, что свидетельствовало о хорошей согласованности измерений. Однако в большей степени обращал на себя внимание тот факт, что разности между результатами, полученными при эУЗИ, имели более широкий 95% ДИ по сравнению с данными, полученными при МРТ, что свидетельствовало о бóльшем разбросе результатов при выполнении эУЗИ и, соответственно, более выраженной согласованности и однородности результатов при использовании МРТ.
В ранее проведенном нами исследовании [15] при сравнительном анализе заключений эУЗИ и ЭхоГСГ, полученными двумя специалистами с различным уровнем подготовки, мы также получили хорошую согласованность измерений при обоих методах. При этом разности между результатами, полученными при ЭхоГСГ, имели более узкий 95% ДИ, по сравнению с данными, полученными при эУЗИ, что выявило более выраженную согласованность и однородность результатов при ЭхоГСГ.
При сравнительном анализе данных МРТ и ЭхоГСГ были выявлены различия в измерении мТР, ширины, длины и глубины ниши; при этом отмечалось занижение мТР и бóльшие параметры ниши по данным ЭхоГСГ. Статистически значимые различия были выявлены при измерении мТР (р=0,03) и глубины ниши (р=0,02) (табл. 5).
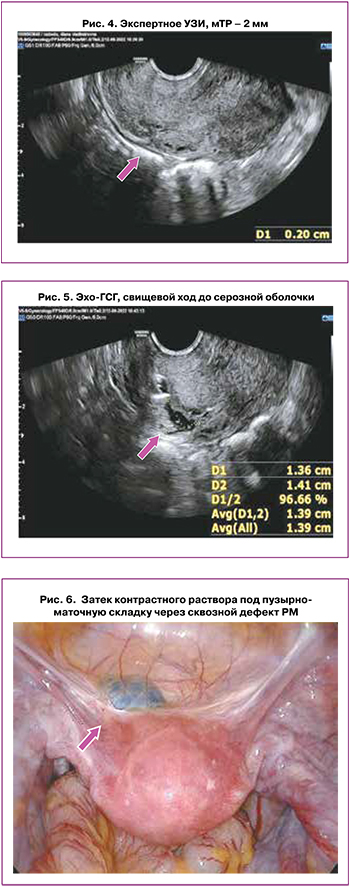
При выполнении ЭхоГСГ у одной пациентки по данным ЭхоГСГ был выявлен свищевой ход, доходящий до серозной оболочки матки; при этом по данным УЗИ и МРТ мТР составила 2 мм (рис. 4, 5). У другой пациентки был выявлен сквозной дефект рубца (затек контрастного раствора под брюшину пузырно-маточной складки), при этом мТР по данным УЗИ составила 3 мм, по данным МРТ – 3,3 мм. Полученные при ЭхоГСГ дополнительные данные были подтверждены в последующем во время хирургического вмешательства (рис. 6).
Обсуждение
Важность точной оценки состояния рубца после КС не вызывает сомнений, поскольку влияет на формирование тактики лечения таких пациенток, в том числе хирургической. Результаты нашего предыдущего исследования показали значительную вариабельность ультразвуковых параметров РМ в зависимости от уровня медицинского учреждения, в котором оно выполнялось, а также преимущества ЭхоГСГ за счет его высокой воспроизводимости. В данном исследовании изучали возможности МРТ в диагностике дефектов РМ по сравнению с эУЗИ и ЭхоГСГ, а также проводили оценку согласованности результатов измерений, полученных при МРТ.
Согласно полученным нами данным, при МРТ отмечались статистически значимые различия в измерении некоторых параметров РМ, по сравнению с УЗИ. Так, отмечались меньшие значения основного параметра – мТР, которая оказалась в среднем на 0,26 мм меньше, чем при УЗИ (р=0,023). Также отмечалось большее значение ширины ниши по данным МРТ.
Разница в измерениях параметров РМ при УЗИ и МРТ была подтверждена и другими исследователями [9, 10, 12]. Bolten K. et al. [9] в своем исследовании сравнили эффективность измерения толщины передней стенки матки в зоне рубца после КС с помощью МРТ и трансвагинального УЗИ. Согласно полученным данным, мТР была значительно меньше по данным МРТ по сравнению с УЗИ как после планового КС (7,9 мм против 12,0 мм соответственно), так и после экстренного КС (8,1 мм против 9,5 мм соответственно).
Также в ретроспективном исследовании Yao M. et al. [10], включающем 282 пациентки, авторы отметили, что МРТ показала бóльшую длину, ширину ниши, а также меньшую мТР в сравнении с трансвагинальным УЗИ (2,91 мм и 2,98 мм соответственно, p=0,598).
В работе Tang X. et al. [12] сравнительная оценка использования УЗИ и МРТ выявила, что средняя длина и глубина дефекта были значительно больше при МРТ, чем при УЗИ, однако авторы не обнаружили значимых различий в оценке мТР.
В исследовании Ножницевой О.Н. и соавт. [13] УЗИ обладало чувствительностью 63%, специфичностью 62%, а МРТ – чувствительностью 80%, специфичностью – 71%. При этом мТР по данным МРТ была больше, по сравнению с УЗИ: 3,44 (1,64) мм и 3,3 (1,54 мм) соответственно, однако разница была статистически незначимой.
В проспективном исследовании случай-контроль, проведенном Satpathy G. et al. [14], авторы также отметили бóльшие значения мТР по данным МРТ в сравнении с УЗИ.
Таким образом, большинством авторов подтверждаются меньшие значения мТР, полученные при МРТ, по сравнению с УЗИ, что согласуется с нашими собственными результатами. На наш взгляд полученная разница в измерениях может быть объяснена более четкой дифференциацией тканей при МРТ, позволяющей при оценке толщины рубца включать в измерение только соединительнотканный или соединительнотканно-мышечный компонент, без базального слоя эндометрия и серозной оболочки матки, которые могут измеряться при УЗИ.
Неоднородность данных, полученных разными исследователями [9, 10, 12–14], может быть следствием отсутствия единой методики измерений. Как показало наше предыдущее исследование, проведение ультразвуковой диагностики на аппаратах неэкспертного уровня без использования стандартизованной методики приводит к значительному разбросу полученных результатов [15]. Именно на стандартизации исследований был сделан акцент экспертами группы Delphi [16]. Поскольку зачастую специалисты МРТ даже со значительным стажем работы не имеют большого опыта в исследовании рубцов на матке после КС, особенно в многопрофильных медицинских учреждениях, мы считаем важным условием внедрение методики Delphi не только в практику специалистов ультразвуковой диагностики, но и в работу рентгенологов, выполняющих МРТ.
На сегодняшний день не проводилось больших сравнительных исследований по диагностике дефектов РМ с помощью ЭхоГСГ и МРТ, поэтому мы уделили особое внимание анализу этих двух методов.
Согласно полученным нами данным, мТР по данным ЭхоГСГ была в среднем на 0,31 мм меньше, чем при МРТ, полученная разница была статистически значимой (р=0,03), ширина и длина ниши не имели значимых различий; при этом отмечалось значимо бóльшее значение глубины ниши по данным ЭхоГСГ по сравнению с МРТ (7,01 мм и 3,29 мм, соответственно, р=0,02). Меньшие значения мТР по данным Эхо-ГСГ (по сравнению как с МРТ, так и с УЗИ) могут быть связаны с растяжением тканей и «расправлением» ниши вследствие введения контрастного раствора в полость матки. При этом внутриматочное введение контраста позволяет определять сложные дефекты РМ в виде ответвлений и сквозных свищевых ходов до серозного покрова.
Нами была выявлена бóльшая согласованность измерений, полученных специалистами с различным уровнем подготовки при МРТ и ЭхоГСГ, по сравнению с УЗИ. Высокая воспроизводимость ЭхоГСГ была показана в более ранних исследованиях [15, 17], однако воспроизводимость МРТ в оценке дефектов РМ была оценена нами впервые. Так как даже у врачей с небольшим опытом работы полученные результаты сопоставимы с заключениями опытных специалистов (при соблюдении алгоритма Delphi), МРТ наряду с ЭхоГСГ может рассматриваться в качестве метода окончательной верификации состояния РМ после КС.
Заключение
Таким образом, МРТ и ЭхоГСГ являются высокоэффективными методами оценки состояния РМ после КС. Измерения основных параметров РМ, полученные при МРТ и ЭхоГСГ, статистически значимо отличаются от измерений, полученных при эУЗИ. Выявлены статистически значимые различия между МРТ и ЭхоГСГ в измерении мТР и глубины ниши; при этом оба метода обладают высокой воспроизводимостью, позволяющей минимизировать получение неоднородных результатов.
УЗИ следует рассматривать в качестве метода исследования 1-й линии; при этом преимуществом пользуется эУЗИ с использованием алгоритма Delphi. При выявлении дефекта РМ по данным эУЗИ для решения вопроса о необходимости хирургического лечения целесообразно выполнить ЭхоГСГ или МРТ с использованием алгоритма Delphi (методы 2-й линии) в зависимости от возможностей медицинского учреждения.
Однако, учитывая преимущества ЭхоГСГ перед МРТ за счет наполнения полости матки контрастом и возможности выявления сложных дефектов РМ в виде ответвлений и сквозных свищевых ходов до серозного покрова, его следует рассматривать в качестве «золотого стандарта» диагностики пациенток с РМ после КС.
Ввиду статистически значимых различий в оценке основных параметров РМ, полученных при эУЗИ, МРТ и ЭхоГСГ, следует учитывать этот факт при разработке пороговых значений для направления пациенток на хирургическое лечение.



