Гиперпролактинемия — это состояние, которое характеризуется стойким избыточным содержанием в сыворотке крови пролактина (ПРЛ) [1], сопровождается различными патологическими изменениями, такими как нарушение половой функции, бесплодие, ожирение, метаболический синдром, остеопороз и т.д. Гиперпролактинемия является важной междисциплинарной медицинской проблемой, что указывает на необходимость знакомства с ней не только акушеров-гинекологов, эндокринологов, но и врачей других специальностей (андролога, уролога и т.д.). Накопленные клинические и экспериментальные данные показали, что нарушение секреции пролактина и связанного с ним симптомокомплекса возникает как при первичном поражении пролактинсекретирующих структур, так и при других эндокринных и неэндокринных заболеваниях, а также при приеме некоторых фармакологических препаратов. Эти данные легли в основу современного представления о первичной гиперпролактинемии как самостоятельной нозологической единицы и ее вторичных формах, наблюдаемых при других заболеваниях [2, 3].
Синдром гиперпролактинемии — симптомокомплекс, который развивается на фоне гиперпролактинемии и сопровождается нарушениями менструальной и репродуктивной функций у женщин. В нашей стране синдромом гиперпролактинемии могут страдать от 214 000 до 2 млн человек, 80% из них – женщины детородного возраста [4]. Частота гиперпролактинемии при нарушениях менструального цикла по типу олигоменореи, аменореи составляет 40%, а при бесплодии – 18–25% [5].
Функциональная гиперпролактинемия характеризуется увеличением секреции ПРЛ при неясной причине этого состояния. Данный диагноз в качестве самостоятельного заболевания устанавливают только после исключения всех известных причин гиперпродукции ПРЛ. Этиология заболевания остается неясной. Предполагают, что в ее основе лежат нарушения нейромедиаторного контроля продукции гормона на уровне гипоталамуса [2, 5, 6]. Частота идиопатической гиперпролактинемии у женщин с бесплодием составляет 12–45% [2, 5, 7]. Вариабельность показателей зависит от точности диагностики, которая, в свою очередь, определяется спектром клинико-лабораторных и рентгенологических методов обследования. Возможно, в дальнейшем проведение фундаментальных исследований, посвященных изучению механизмов синтеза, секреции ПРЛ и его биологических эффектов, а также совершенствование методов диагностики поставят под сомнение существование такой формы заболевания, как идиопатическая гиперпролактинемия [5].
Основные клинические проявления гиперпролактинемии неопухолевого генеза — нарушение менструального цикла по типу олигоменореи (~62%) на фоне ановуляции или недостаточности лютеиновой фазы (НЛФ), регулярный ритм менструаций (~38%) при наличии полноценной или неполноценной лютеиновой фазы цикла, галакторея (~30–78%). Активность ПРЛ в плазме крови не превышает 3000 мМЕ/л, и почти у каждой второй, особенно при регулярном ритме менструаций, нарушение его секреции имеет транзиторный характер. Преобладает первичное бесплодие [1, 4, 5, 8]. Гиперпролактинемия проявляется нарушениями менструального цикла по типу гипо-, олиго-, опсо- и аменореи, а также бесплодием. У женщин с гиперпролактинемией нередко наблюдается галакторея, причем она не всегда коррелирует с уровнем ПРЛ. Так, галакторея возможна и при нормальном его уровне, что связано с гиперчувствительностью рецепторов пролактина в молочной железе.
Терапия пациенток с гиперпролактинемией не ограничивается применением селективных и неселективных дофаминомиметиков. Существуют и другие возможности коррекции патологической гиперпролактинемии, в том числе с помощью растительных средств [9]. Доказано, что растение Agnus castus обладает дофаминергическим действием, приводит к мягкому снижению продукции ПРЛ [10], что крайне важно при коррекции функциональной гиперпролактинемии с невысокими цифрами ПРЛ.
Цель исследования – представить собственный опыт применения Прегнотона в восстановлении менструального цикла у пациенток с функциональной гиперпролактинемией.
Материалы и методы
В период с 2018 по 2019 г. на клинической базе кафедры акушерства и гинекологии лечебного факультета МГМСУ им. А.И. Евдокимова, женская консультация при ГКБ № 57 им. Д.Д. Плетнёва, проведено обследование 135 пациенток репродуктивного возраста с функциональной гиперпролактинемией и нарушениями менструального цикла. Прегнотон принимали по одному саше 1 раз в день перед едой. Продолжительность курса составила 3 месяца. Обследование пациенток выполняли трижды: до лечения, после 1-го месяца лечения и после лечения через 3 месяца.
Критериями включения стали: репродуктивный возраст; отсутствие инфекций репродуктивного тракта; отсутствие выраженной соматической патологии, исключены эндокринные синдромы (синдром поликистозных яичников (СПКЯ), неклассическая форма врожденной дисфункции коры надпочечников (НК-ВДКН)); отмена за 3 и более месяцев, предшествовавших исследованию, гормональных препаратов и других медикаментов, влияющих на уровень половых стероидов; отсутствие сопутствующей эндокринной патологии (нарушения функции щитовидной железы); исключение рака молочной железы (РМЖ), эндометрия или других гормонозависимых опухолей.
Критерии исключения: нарушения овуляции, непроходимость маточных труб, распространенный эндометриоз.
Все пациентки, участвовавшие в исследовании, дали свое письменное согласие. Исследование было одобрено на заседании этической комиссии при ГКБ № 57 им. Д.Д. Плетнёва.
У всех пациенток, включенных в исследование, на начальном этапе был проведен сбор анамнестических данных и заполнены специально разработанные анкеты. При оценке показателей созревания репродуктивной системы учитывали: возраст менархе, характер становления менструального цикла, последовательность появления вторичных половых признаков (телархе и пубархе). Уточняли возраст возникновения, причины, длительность, характер нарушений менструального цикла. Активность пролактина определяли на 4–5-й день менструального цикла методом иммуноферментного анализа на анализаторе Sunrise (TECAN Austria GmbH) с использованием наборов Biofource, Бельгия. Уровень пролактина колебался от 890 до 1000 мМЕ/мл. В качестве нормативных значений использовали пределы нормы, разработанные в лаборатории эндокринологии Национального медицинского исследовательского центра акушерства, гинекологии и перинатологии им. академика В.И. Кулакова (концентрация ПРЛ в сыворотке крови у женщин репродуктивного возраста, от 120 до 500 мМЕ/л). Используемая биологически активная добавка Прегнотон не вызвала аллергических реакций и других побочных явлений.
Результаты и обсуждение
Выбор препарата Прегнотон для лечения нарушений менструального цикла был не случайным. Препарат отличают полифункциональность, мягкость действия, наличие эффекта последействия, отсутствие развития лекарственной болезни и эффекта «отмены». Хорошо изучен механизм действия входящего в состав данного препарата экстракта растения Agnus castus, который действует как конкурентный ингибитор D2-рецепторов допамина (препятствует супрафизиологическому высвобождению ПРЛ из лактотрофов гипофиза). Кроме того, устраняет действие допамина, серотонина, норадреналина и других нейротрансмиттеров и способствует улучшению созревания фолликула и повышению активности желтого тела [5–7].
Средний возраст исследуемых женщин составил 31±5 лет. Ни у одной пациентки не было выраженных метаболических расстройств. При изучении преморбидного фона у больных с гиперпролактинемией превышения числа перенесенных в детском возрасте инфекционных заболеваний по сравнению с данными в популяции не отмечено. Средний возраст наступления менархе составил 12,9±0,5 года. У всех респонденток менструальный цикл установился сразу. Вместе с тем у 30/135 (22,2%) обследованных пациенток имели место заболевания центральной нервной системы и перенесенные травмы головного мозга. Практически у каждой второй пациентки в структуре сопутствующей экстрагенитальной заболеваемости преобладала патология желудочно-кишечного тракта, в том числе гепатобилиарной системы 15/135 (11,1%). В этом аспекте немаловажен тот факт, что 40/135 (29,6%) пациенток в течение двух предшествовавших настоящему обследованию лет перенесли эндоскопическую холецистэктомию по поводу желчнокаменной болезни, еще у 3 клинические проявления совпали с тяжелыми стрессовыми ситуациями в семье. Наши данные, как и многочисленные указания в литературе, в том числе эпидемиологические исследования, подтверждают значимость стрессорного фактора в развитии неопухолевой гиперпролактинемии [5, 7, 8]. К провоцирующим факторам возникновения гиперпролактинемии также можно отнести длительное применение эстроген-гестагенных оральных контрацептивов (1,5–2 года) [5]. Влияние данной категории препаратов на секрецию ПРЛ общеизвестно. Как эндогенные, так и экзогенные эстрогены, входящие в состав комбинированных оральных контрацептивов и препаратов для заместительной гормонотерапии, использующихся в пери- и постменопаузальном периоде, активируют эстроген-чувствительный элемент гена ПРЛ и способствуют увеличению синтеза и секреции последнего. Оральные контрацептивы, возможно, не вызывают образования пролактином, но способны стимулировать их развитие и обычно не назначаются пациенткам с такими опухолями [2, 11].
При тщательном анализе особенностей менструальной функции, из нарушений менструального цикла до лечения, у пациенток были выявлены: гипоменорея – у 20/135 (14,8%), олигоменорея – у 25/135 (18,6%), опсоменорея – у 10/135 (7,4%), полименорея – у 30/135 (22,2%) и у 50/135 (37%) пациенток была отмечена альгоменорея.
Динамика уровня ПРЛ у исследуемых пациенток представлена в таблице.

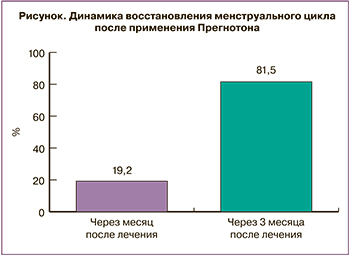 Прегнотон обладает пролактинингибирующим действием. Допаминергическая активность данного препарата доказана в клинико-экспериментальных исследованиях. При этом он не снижает базальный уровень ПРЛ. В случаях латентной гиперпролактинемии наблюдаются некоторое снижение или, по меньшей мере, тенденция к снижению активности пролактина и улучшение клинической картины. В связи с этим препараты из экстрактов плодов Vitex agnus castus в гинекологической практике применяются при нарушениях менструального цикла, недостаточности желтого тела, предменструальном синдроме, циклической масталгии и фиброзно-кистозной мастопатии [6, 7, 12]. Через месяц приема Прегнотона 80/135 (59,2%) наблюдаемых отметили значительное улучшение своего общего состояния, у 26/135 (19,2%) менструальный цикл восстановился. После прохождения полного курса Прегнотона (3 месяца) значительное улучшение состояния было отмечено у 115/135 (85,2%) пациенток, восстановление менструального цикла – у 110/135 (81,5%) (рисунок). Таким образом, существенный эффект от приема Прегнотона следует ожидать после прохождения 3-месячного курса лечения.
Прегнотон обладает пролактинингибирующим действием. Допаминергическая активность данного препарата доказана в клинико-экспериментальных исследованиях. При этом он не снижает базальный уровень ПРЛ. В случаях латентной гиперпролактинемии наблюдаются некоторое снижение или, по меньшей мере, тенденция к снижению активности пролактина и улучшение клинической картины. В связи с этим препараты из экстрактов плодов Vitex agnus castus в гинекологической практике применяются при нарушениях менструального цикла, недостаточности желтого тела, предменструальном синдроме, циклической масталгии и фиброзно-кистозной мастопатии [6, 7, 12]. Через месяц приема Прегнотона 80/135 (59,2%) наблюдаемых отметили значительное улучшение своего общего состояния, у 26/135 (19,2%) менструальный цикл восстановился. После прохождения полного курса Прегнотона (3 месяца) значительное улучшение состояния было отмечено у 115/135 (85,2%) пациенток, восстановление менструального цикла – у 110/135 (81,5%) (рисунок). Таким образом, существенный эффект от приема Прегнотона следует ожидать после прохождения 3-месячного курса лечения.
Заключение
Применение сбалансированного витаминно-минерального комплекса (Прегнотон) оказывает положительный эффект на общее самочувствие женщины (улучшает настроение, налаживает сон) и может использоваться при лечении нарушений менструального цикла у пациенток с функциональной гиперпролактинемией.



