В клинической практике кардиохирург может встретиться с объемным образованием сердца, происходящим из матки, и от выбранной тактики будет зависеть продолжительность жизни и благополучие пациентки. В прошлом году L.R. Mckenna и соавт. описали случай лейомиосаркомы матки, распространявшейся по нижней полой вене (НПВ): пациентке выполнили абдоминальную гистерэктомию, а год спустя компьютерная томография выявила внутрисердечную опухоль, которую удалили в условиях искусственного кровообращения (ИК). Пять лет спустя вновь возник рецидив [1].
В прошлом году вышла близкая по теме публикация Н.В. Сорока с cоавт., в которой представлен клинический случай поражения трехстворчатого и легочного клапанов у пациента с карциноидной опухолью [2]. Десять лет назад опубликовано сообщение из ННИИПК им. акад. Е.Н. Мешалкина об успешной правосторонней нефрэктомии по поводу неоплазмы с прорастанием в НПВ и правые отделы сердца [3]. В отечественной литературе мы не нашли работ по хирургической реабилитации миксоидного внутривенного лейомиоматоза матки, и наше сообщение, возможно, является первой такой отечественной публикацией.
 Описание клинического наблюдения
Описание клинического наблюдения
Пациентка З-на, 49 лет, поступила в отделение приобретенных пороков сердца 14.05.2012 с жалобами на одышку при ходьбе до 50 м, отеки голеней, перебои в работе сердца, боли в нижней трети живота, метроррагии. Больна с лета 2011 г., когда впервые выявлено новообразование органов малого таза. С того же времени отмечает одышку с постепенным снижением толерантности к нагрузкам. Объективно: состояние больной тяжелое по заболеванию, стабильное. Видимые слизистые оболочки обычной окраски. Периферические лимфатические узлы не увеличены. Относительные границы сердца расширены влево. Выслушивается диастолический шум над трехстворчатым клапаном. Пальпируется образование в нижней трети живота, умеренно болезненное, бугристое, верхняя граница на уровне пупка. Пальпируются паховые лимфоузлы. Бимануальное исследование: тело матки увеличено до 22 недель беременности, бугристое. Придатки не пальпируются.
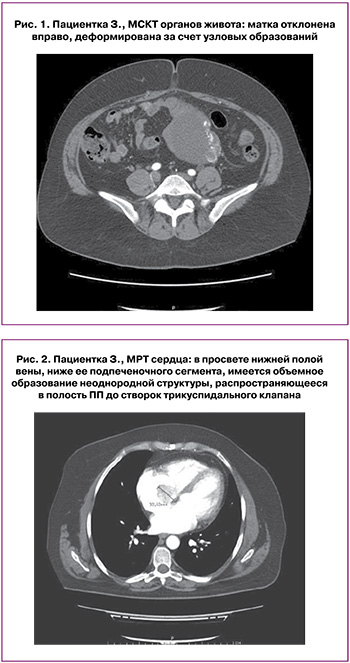
Мультиспиральная компьютерная томография (МСКТ) органов живота (рис. 1): матка в anteversio, anteflexio, отклонена вправо, деформирована за счет узловых образований, накапливающих контраст наиболее сильно в правых отделах свода – до 60×65 мм, неровные бугристые контуры. В левых отделах матки объемные кистозные изменения с утолщенными стенками, наиболее крупные кисты до 85×142×63 мм, в полости кист неполные септы с участками интенсивного контрастирования в артериальную фазу. Яичники: в их проекции кистозно-солидные изменения, неотделимые от матки. От левого контура матки бугристые образования кистозной структуры распространяются вдоль левой яичниковой вены на протяжении до 6 см. Вену сопровождает извитая яичниковая артерия диаметром до 3,5 мм. В просвете левой яичниковой вены объемное образование распространяется в НПВ и в полость правого предсердия (ПП) до уровня створок трикуспидального клапана (ТК), занимает от 1/2 до 3/4 поперечного просвета вен, на всем протяжении до полости предсердия интенсивно накапливает контраст в артериальную фазу, с частичным вымыванием контраста в венозную фазу. Лимфоузлы портальной и чревной групп до 10–15 мм. Единичные парааортальные лимфоузлы, размером по длинной оси до 10–15 мм. В костях объемных деструктивных изменений не выявлено.
По данным УЗИ сердца: объемное образование из НПВ до полости ПП. Чреспищеводная ЭХО-кардиография: показатели сократимости миокарда в норме. В полости ПП и просвете НПВ подвижное фрагментированное образование, 5,6/2,6 см. Магнитно-резонансная томография (МРТ) сердца (рис. 2): в просвете НПВ ниже ее подпеченочного сегмента объемное образование неоднородной структуры, гипер-изоинтенсивное на Т2-ВИ, занимает до 3/4 поперечного просвета вены без деформации ее наружного контура. Диаметр НПВ над диафрагмой 38×37 мм. Образование распространяется в полость ПП до створок ТК, имеет в его полости округлый вид, размерами 40×35×32 мм, прилежит к септальной створке ТК. Нарушения функции ТК не выявлено.
17.05.2012 выполнена операция: Экстирпация матки с придатками. Удаление объемного образования ПП. Удаление объемного образования НПВ, удаление левой яичниковой вены. Удаление большого сальника.
Проведена нижняя срединная лапаротомия до мечевидного отростка. В области левых придатков объемное образование в гладкой капсуле, многокамерное, заполненное белой студенистой массой, 25×20×15 см, уходящее забрюшинно. Матка не увеличена, смещена объемным образованием вправо. Правые придатки кистозно изменены, 2×2,5×3 см, капсула гладкая, блестящая, тонкая. Придатки вместе с круглой связкой прошиты и провязаны. На ребро матки в области проекции маточной артерии наложены зажимы, артерия пересечена, прошита. Левая маточная артерия лигирована на зажимах, пересечена. Экстирпация матки с верхней третью влагалища, правым придатком, удалено объемное образование. Выделена левая яичниковая вена, диаметром 2 см, до почечной вены (рис. 3). Вена заполнена студенистой белой массой, не прорастающей в стенку сосуда.
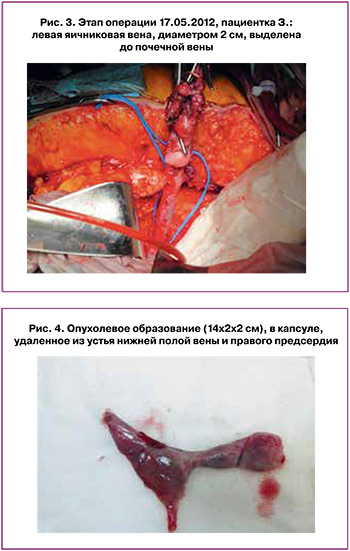 Срединная стернотомия. Канюлированы восходящая аорта, верхняя полая вена, ПП. Окклюзия аорты, кардиоплегия. Гипотермия до 18°С. Циркуляторный арест. Вскрыто ПП. В полости ПП и НПВ студнеобразное образование, в капсуле, в стенки не прорастает. Снят зажим с яичниковой вены, и образование беспрепятственно удалено из устья НПВ, ПП, размер 14×2×2 см (рис. 4). Ревизован ТК. Гидравлическая проба удовлетворительна. Яичниковая вена отсечена возле места ее впадения в почечную вену. Культя ушита нитью 5–0. ПП герметизировано двойным непрерывным швом. Восстановлено кровообращение. Согревание. Экспресс-цитологическое исследование с культи влагалища: заподозрено наличие атипичных клеток, удален большой сальник. Перитонизация культи влагалища. Гемостаз адекватный. По ходу яичниковой вены, забрюшинно установлена дренажная трубка, с активной аспирацией. Рана послойно ушита. Время ИК – 177 мин, циркуляторный арест – 19 мин. Время искусственной вентиляции легких – 24 ч, инотропная поддержка в течение 3 суток. Пребывание в отделении интенсивной терапии – 3 суток.
Срединная стернотомия. Канюлированы восходящая аорта, верхняя полая вена, ПП. Окклюзия аорты, кардиоплегия. Гипотермия до 18°С. Циркуляторный арест. Вскрыто ПП. В полости ПП и НПВ студнеобразное образование, в капсуле, в стенки не прорастает. Снят зажим с яичниковой вены, и образование беспрепятственно удалено из устья НПВ, ПП, размер 14×2×2 см (рис. 4). Ревизован ТК. Гидравлическая проба удовлетворительна. Яичниковая вена отсечена возле места ее впадения в почечную вену. Культя ушита нитью 5–0. ПП герметизировано двойным непрерывным швом. Восстановлено кровообращение. Согревание. Экспресс-цитологическое исследование с культи влагалища: заподозрено наличие атипичных клеток, удален большой сальник. Перитонизация культи влагалища. Гемостаз адекватный. По ходу яичниковой вены, забрюшинно установлена дренажная трубка, с активной аспирацией. Рана послойно ушита. Время ИК – 177 мин, циркуляторный арест – 19 мин. Время искусственной вентиляции легких – 24 ч, инотропная поддержка в течение 3 суток. Пребывание в отделении интенсивной терапии – 3 суток.
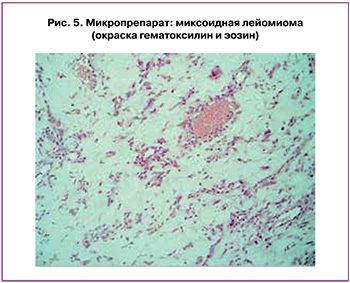
Ранний послеоперационный период протекал с явлениями сердечной недостаточности, гипоксической энцефалопатией, кардиотоническая поддержка в течение 3 суток, симптоматическая нейропротекторная терапия. В дальнейшем выраженный астенический синдром, фебрильная лихорадка. Общий срок госпитализации 64 дня. На момент выписки состояние удовлетворительное. По результатам цитологического исследования – образование определено как лейомиосаркома с ростом до диссеминации в венах. Для уточнения диагноза, дифференциации с текомой, интервенозной миомой, проведен иммуногистологический анализ интраоперационных образцов опухоли: миксоидная лейомиома с внутривенозным распространенным лейомиоматозом (рис. 5).
На момент публикации срок наблюдения за пациенткой составляет 3 года. Данных за рецидив заболевания не получено. Боли в животе, одышка, отеки не наблюдались.
Обсуждение
Внутривенный лейомиоматоз, описанный Durck в 1907 г., является редким осложнением объемных образований матки, которые, распространяясь в системе НПВ, достигают правых отделов сердца. Долгое время опухоль асимптомна, а при манифестации заболевания симптомы неспецифичны. У опухоли есть риск малигнизации, что является фактором риска при неполном удалении опухоли: 3–4% злокачественных гинекологических опухолей приходится на саркомы, наиболее распространена лейомиосаркома (52%), эти цифры стабильны из года в год [4]. Для предоперационной идентификации референтными методами являются КТ и МРТ [5].
Граница между доброкачественными и злокачественными гинекологическими опухолями всегда нечеткая: G. Toledo с соавт. сообщили о 18 случаях лейомиосаркомы, в половине случаев которых отчетливо наблюдалась миксоматозная строма [6]. Миксоматозные изменения лейомиомы встречаются в 15%, а их гиалиновая дегенерация — в 4‒10%. Вагинальное бимануальное исследование не позволяет верифицировать злокачественные ткани. УЗИ во многих случаях также не различит лейомиому и лейомиосаркому. Интраоперационно на малигнизацию указывают желеобразный вид и инвазивные признаки, но даже гистологически иногда невозможно поставить окончательный диагноз: из-за низкого митотического индекса малигнизация происходит постепенно и органичено (мозаично). В связи с этим, злокачественность при этой патологии нужно предполагать априори и выполнять радикальную операцию – это обеспечит перспективу благоприятного прогноза и хорошего качества жизни [7].
 Присутствие внутривенного распространения лейомиомы матки на современном этапе гистопатологически пока трудно определять, контрастная КТ в артериальной фазе визуализации остается референтным предоперационным методом [8]. Миксоидная лейомиосаркома в большинстве случаев идентифицируется лишь после операции, и, учитывая риск малигнизации, методом выбора будет одноэтапная операция с применением ИК. Первое сообщение о ее выполнении было сделано 16 лет назад N.A. Stolf и соавт., описавшими случай внутривенного лейомиоматоза матки с распространением до правого желудочка и успешной одноэтапной операции под ИК [9]. В ходе накопления мирового опыта лечения распространяющейся к сердцу опухоли, K.C. Coard и соавт. 13 лет назад предложили термин «внутривенный лейомиосаркоматоз матки», они же описали и рецидив опухоли в НПВ сразу через 3 месяца после гистерэктомии [10].
Присутствие внутривенного распространения лейомиомы матки на современном этапе гистопатологически пока трудно определять, контрастная КТ в артериальной фазе визуализации остается референтным предоперационным методом [8]. Миксоидная лейомиосаркома в большинстве случаев идентифицируется лишь после операции, и, учитывая риск малигнизации, методом выбора будет одноэтапная операция с применением ИК. Первое сообщение о ее выполнении было сделано 16 лет назад N.A. Stolf и соавт., описавшими случай внутривенного лейомиоматоза матки с распространением до правого желудочка и успешной одноэтапной операции под ИК [9]. В ходе накопления мирового опыта лечения распространяющейся к сердцу опухоли, K.C. Coard и соавт. 13 лет назад предложили термин «внутривенный лейомиосаркоматоз матки», они же описали и рецидив опухоли в НПВ сразу через 3 месяца после гистерэктомии [10].
Внутривенный лейомиоматоз – редкое неопластическое состояние, характеризующееся доброкачественной внутрисосудистой пролиферацией гладкомышечных клеток, происходящих из любой стенки вен матки, лейомиомы матки, таящее, помимо рисков рецидивов и малигнизации, еще и риск тромбоэмболий и вторичных метастазов. В 2007 г. D.K. McDonald и соавт. описали первый клинический случай сопутствовавшей внутрисосудистой опухолевой эмболии легочной артерии [11], а S.K. Nguyen с соавт. первыми описали вторичные метастазы лейомиосаркомы в структуры сердца с развитием миомы сердца. По мнению авторов, хирургическая резекция метастатических образований, при условии, что она еще возможна, может обусловить более длительную выживаемость [12].
Резюмируя, можно заключить, что только симультанная одномоментная операция является залогом успеха, и в прошлом году это продемонстрировали M. Sogabe с соавт., описав случай 45-летней женщины, у которой КТ выявила наличие внутривенной лейомиомы, происходящей из матки и проходящей в НПВ, ПП, в правый желудочек. Пациентке была одномоментно успешно выполнена кардиотомия под гипотермическим ИК и лапаротомия; без рецидивов опухоли на протяжении 10-месяцев наблюдения [13]. Однако не менее важным фактором, влияющим на успех, является злокачественность самой опухоли. К 2014 г. в мире в целом зарегистрировано 30 случаев миксоидной лейомиосаркомы, показавших, что, несмотря на радикальность резекций и налаженную систему ведения пациента по месту жительства, часты рецидивы и метастазы [14]. Внутривенный лейомиоматоз более благоприятен по прогнозу, и важно, что есть возможность его своевременного обнаружения для снижения риска малигнизации. J. Shang и соавт. ретроспективно проанализировали 19 случаев внутривенного лейомиоматоза с внутрисердечным распространением и выявили, что опухолевые клетки были положительны по SMA, ER, PR, но отрицательны по HMB45 и S-100. CD10 и CD34 были положительны у 4 больных и отрицательны у остальных [15].
Заключение
В описанном клиническом наблюдении показана эффективность и безопасность симультанного одноэтапного лечения лейомиоматоза матки с внутрисосудистым распространением в ПП. Пациентке показано диспансерное наблюдение онкогинеколога; плановые УЗИ сердца и живота, контроль уровня онкомаркеров.



