Склероатрофический лихен (САЛ) – хроническое воспалительное поражение кожи и слизистых оболочек, наиболее часто встречающееся в генитальной области и проявляющееся зудом, болезненностью, атрофией и рубцовой деформацией тканей [1, 2].
В основе патогенеза САЛ лежат сосудистые и иммунные нарушения: ухудшение микроциркуляции и дефицит влагоудерживающих субстанций в совокупности с дисрегуляцией иммунной системы приводят к нарушению метаболизма коллагена и фибробластов (гликации, уменьшению количества волокон, эластозу). В результате увеличиваются растяжимость и истончение гиподермы, уменьшаются увлажненность, эластичность, толщина кожи и активность кератиноцитов, нарушается меланогенез. Данные патологические изменения обусловливают появление морщин, сухости и атрофии, неравномерной пигментации.
Пациенты с САЛ чаще всего имеют жалобы на выраженный зуд, болезненность в аногенитальной области, трещины, сухость кожи и слизистой оболочки вульвы и влагалища. В случае позднего начала лечения САЛ и прогрессирования заболевания вследствие расчесов появляются гиперкератоз, эрозии, локализованные кровоизлияния, трещины и прогрессирующее рубцевание.
Течение заболевания можно разделить на 3 стадии. Начальные проявления (1-я стадия) сопровождаются появлением отека и покраснения половых органов, вызванных нарушением микроциркуляции и гипоксией тканей. По мере развития заболевания (2-я стадия) кожа становится атрофичной. В результате это может приводить к уменьшению малых половых губ, сужению входа во влагалище, нарушению мочеиспускания, диспареунии, а также к перианальному стенозу и болезненной дефекации. Появляются нарушение пигментации, сухость, лихенификация. Третья стадия характеризуется развитием полной атрофии и рубцового склероза наружных гениталий [3, 4]. Особенностью заболевания является его склонность к частому рецидивированию и прогрессированию процесса с ухудшением качества жизни.
Нередко течение заболевания осложняется присоединением дисбиоза и воспалительных процессов в виде вульвовагинита [5]. САЛ вульвы с хроническим гиперкератозом и эрозиями может осложниться плоскоклеточной карциномой [6].
С целью лечения САЛ проводят продолжительную местную терапию глюкокортикостероидами (ГКС) и ингибиторами кальциневрина [7, 8]. Однако при длительном применении местные ГКС (клобетазола пропионат, мометазона фуроат) вызывают атрофию эпителия, что может приводить к рецидивированию заболевания [9] или появлению побочных эффектов топических ГКС, связанных с усилением атрофии на фоне длительного применения.
В связи с этим целесообразно использовать ГКС совместно с препаратами других фармакологических групп с целью увлажнения кожи и слизистых оболочек и профилактики рецидивов [8, 10].
Появление на рынке увлажняющих средств, содержащих низкомолекулярную гиалуроновую кислоту, способную проникать в глубокие слои кожи с целью увлажнения, обосновало целесообразность разработки схемы эффективного их применения при САЛ с целью профилактики атрофических процессов многослойного плоского эпителия гениталий и предупреждения рецидивов заболевания.
Цель исследования: сравнить эффективность монотерапии топическими ГКС и сочетанной терапии ГКС со средством на основе низкомолекулярной гиалуроновой кислоты для местного применения (крем дозированный «Эстрогиал» и гель «Эстрогиал») в терапии САЛ у женщин.
Материалы и методы
В проспективном рандомизированном контролируемом сравнительном исследовании добровольно приняли участие 66 женщин с САЛ в возрасте 26–70 лет. Группы были разделены случайным образом. 1-ю группу составили 20 пациенток, 2-ю – 46 пациенток. Всем пациенткам была назначена комплексная терапия: аппликации крема, содержащего топический ГКС (мометазона фуроат 0,1%), в течение 3 месяцев по схеме: 1-й месяц – 2 раза в сутки, 2-й месяц – 1 раз в сутки, 3-й месяц – 2 раза в неделю. Во 2-й группе дополнительно был назначен крем дозированный «Эстрогиал» на ночь во влагалище 1 раз в день 10 дней каждого месяца в течение 6 месяцев и гель «Эстрогиал» на область вульвы 2 раза в день в течение 6 месяцев. Эффективность лечения оценивали через 2, 6, 12 недель и 6 месяцев после начала лечения по динамике наличия/отсутствия симптомов, а также выраженности наиболее частых из них (зуд, атрофия и бледность вульвы), выявленных по результатам обследования перед началом терапии.
Статистический анализ
Статистическая обработка данных была проведена с использованием пакетов статистического анализа Microsoft Office Excel 2016, Statistica 12, GraphPad Prism 8.0. Численные значения анализируемых показателей при соответствии закону нормального распределения, установленном на основании расчета критерия Шапиро–Уилка, представляли в виде среднего значения (М) и стандартного отклонения (SD), в противном случае – в виде медианы (Ме) и интерквартильного размаха (Q25; Q75). Для множественного сравнения количественных зависимых переменных использовали ранговый дисперсионный анализ Фридмана с проведением апостериорных сравнений при помощи теста Данна и расчета выраженности эффекта с помощью W-критерия Кендалла. Сравнение дихотомических данных связанных выборок проводили при помощи теста Q-Кохрана с последующим попарным сравнением методом Хи-квадрат (χ2) МакНемара с поправкой Эдвардса. Межгрупповые сравнения количественных переменных при нормальном распределении проводили с помощью t-критерия Стьюдента, при ненормальном – U-критерия Манна–Уитни с расчетом размера эффекта путем вычисления разности медиан (оценка Ходжеса–Лемана) и 95% доверительного интервала (ДИ). Качественные независимые переменные сравнивали с использованием точного критерия Фишера с расчетом относительного риска (ОР) и ДИ. За критический уровень значимости при попарном сравнении принимали значение р<0,05, при множественном – p<0,005 (с учетом поправки Бонферрони).
Результаты
Из исследования были исключены пациентки со значительной сопутствующей соматической патологией (выраженным ожирением, декомпенсированным сахарным диабетом и артериальной гипертензией, аутоиммунными заболеваниями), с наличием инфекций, передаваемых преимущественно половым путем, и воспалительными заболеваниями малого таза, а также пациентки, получающие терапию по поводу САЛ или имеющие таковую в анамнезе (применение ГКС более 5 дней).
Исследуемые группы до начала лечения не отличались по возрастному составу, средней длительности заболевания, наличию сопутствующих заболеваний, таких как миома матки, хронический цистит, артериальная гипертензия. Также исходно группы не различались по наличию симптомов САЛ и выраженности основных (зуд, атрофия, бледность) (табл. 1).

На момент начала исследования основными проявлениями САЛ у всех пациенток в обеих исследуемых группах в области вульвы были зуд, атрофия и бледность, выявленные в результате внешнего осмотра. Кроме того, подавляющее число женщин в обеих группах имели жалобы на болезненность и жжение.
При оценке динамики наличия симптомов САЛ у женщин в обеих группах установлено, что у пациенток 1-й группы, принимавших только топические ГКС, большинство симптомов (зуд, атрофия, бледность, кровоизлияния, шелушение, болезненность, жжение, лихенификация) регрессировали в ходе лечения (p<0,001). Однако, оценивая влияние данной терапии на динамику таких симптомов, как ригидность и склероз, статистической значимости выявлено не было (p=0,06 и р=0,03 соответственно). В то же время у пациенток 2-й группы было отмечено улучшение всех симптомов САЛ в ходе терапии (p<0,001) (табл. 2).

Исходя из данных таблицы 3, можно сделать вывод, что ведущие симптомы САЛ (зуд, атрофия, бледность, шелушение) эффективно устраняются уже в первые 2 недели лечения, независимо от выбранной тактики. В то же время жжение, ригидность, лихенификация и склероз сохраняются у пациентов достаточно длительное время и элиминируют лишь через несколько месяцев от начала лечения. Также следует отметить, что к исходу периода наблюдения (6 месяцев) пациентки, получающие терапию только топическими ГКС (группа 1), отмечали возвращение ряда симптомов, таких как кровоизлияние, шелушение, жжение, ригидность, лихенификация и склероз, хотя в раннем периоде лечения данные симптомы были эффективно устранены. Это может свидетельствовать о рецидиве заболевания в связи с прекращением терапии (3 месяца согласно Клиническим рекомендациям), а также о негативном влиянии длительного применения ГКС ввиду их способности вызывать атрофические изменения кожи и слизистых. Напротив, сочетанное применение средств гиалуроновой кислоты с топическими ГКС (группа 2) на протяжении 3 месяцев с продолжением приема «Эстрогиала» успешно и стабильно купировало вышеперечисленные симптомы – к исходу 6 месяцев лечения было обнаружено статистически значимое уменьшение всех проявлений САЛ по сравнению с исходными значениями, отсутствие рецидива заболевания (табл. 3).
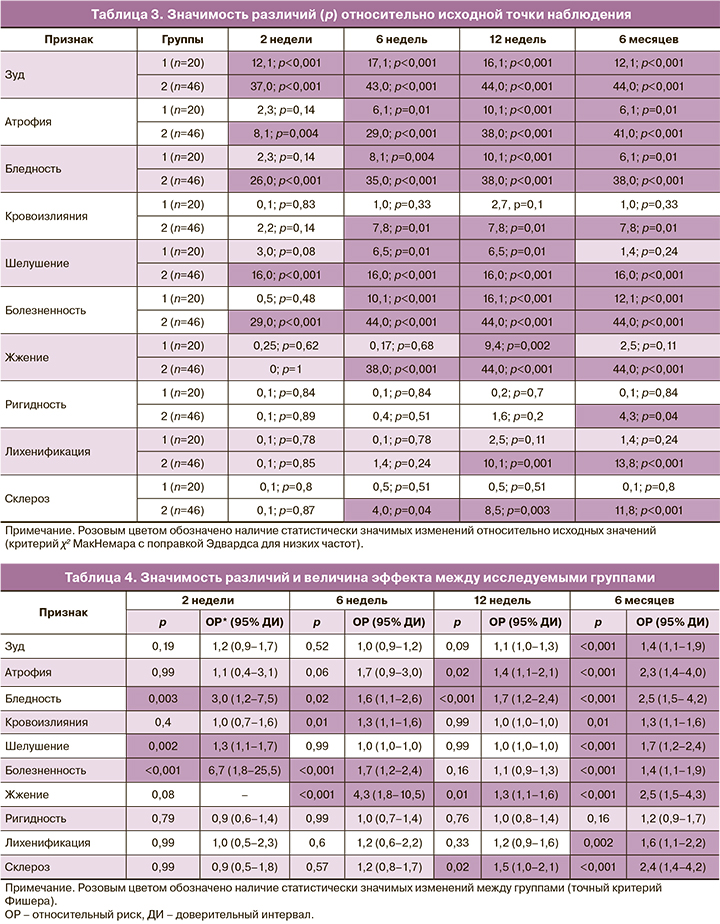
При межгрупповой оценке различий динамики наличия симптомов САЛ было установлено, что добавление крема дозированного и геля «Эстрогиал» к основной терапии топическими ГКС сопровождалось наиболее стойким и продолжительным эффектом. Так, к концу лечения была выявлена статистически значимая разница между исследуемыми группами относительно наличия большинства симптомов САЛ (за исключением ригидности). Наиболее выраженный эффект к 6-му месяцу наблюдения отмечался между группами в отношении атрофии, бледности, жжения и склероза. Также ряд значимых отличий наблюдался между группами в ходе терапии (2, 6, 12 недель) (табл. 4).
В рамках настоящего исследования была также исследована динамика выраженности в баллах основных симптомов САЛ (зуд, атрофия, бледность) (табл. 5).

Методом непараметрического дисперсионного анализа было установлено, что терапия топическими ГКС как изолированно, так и совместно со средствами гиалуроновой кислоты приводила к улучшению динамики зуда, атрофии и бледности. При апостериорном внутригрупповом сравнении было, однако, установлено, что у пациенток 1-й группы к исходу 6-го месяца наблюдения отмечалось обратное развитие атрофических изменений, что свидетельствовало о рецидиве заболевания на фоне отмены топических ГКС и отсутствия поддерживающей терапии с целью восстановления естественного барьера кожи и слизистых оболочек – различий по выраженности данного симптома относительно исходных значений не получено (р=0,13). При этом пациентки 2-й группы на протяжении всего периода лечения отмечали стойкое уменьшение выраженности всех симптомов САЛ. Суммарная величина лечебного эффекта была также выше в отношении зуда, атрофии и бледности у пациенток 2-й группы (табл. 6).
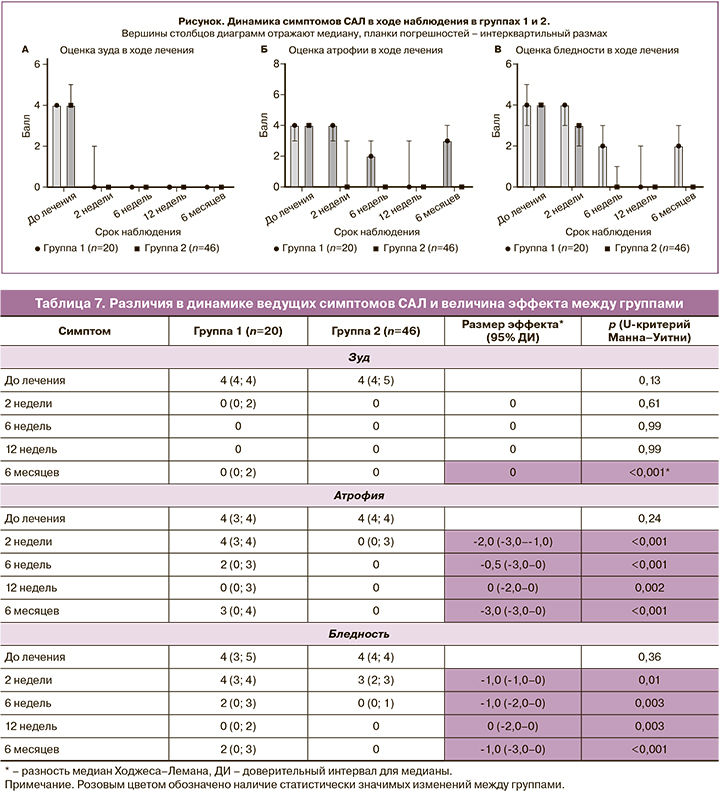
При оценке межгрупповых различий в динамике проявлений зуда, атрофии и бледности установлено, что выраженность зуда в ходе терапии практически не отличалась между группами – лишь в последней контрольной точке (6 месяцев) проявления зуда были значимо менее выражены в группе пациентов, принимающих сочетанную терапию (ГКС + «Эстрогиал»). Однако отличия в динамике атрофии и бледности были более значительными – в каждой контрольной точке выраженность данных симптомов у пациентов 2-й группы была статистически значимо ниже, чем в группе контроля. Наибольший размер эффекта к концу 6-го месяца наблюдения отмечался в отношении атрофии – разность медиан между группами составила -3,0 (-3,0–0), р<0,001 (табл. 7, рисунок).
Обсуждение
Согласно современным данным и клиническим рекомендациям, применение топических ГКС является основой терапии САЛ. При неосложненном течении заболевания данная стратегия является эффективной на ранних стадиях лечения более чем в 70% случаев [2, 11]. Однако длительное применение данной группы препаратов (более 3 месяцев) не рекомендовано ввиду высокого риска развития атрофических изменений кожи и слизистых. В связи с этим даже при высокой эффективности терапии вероятность рецидивирования заболевания без поддерживающей или альтернативной терапии является высокой [12]. С учетом высокой склонности к рецидивному течению САЛ важной и актуальной задачей на настоящий момент является использование средств, дополняющих базисную терапию САЛ. В линейке продуктов «Эстрогиал» (гель и два крема дозированных – «Эстрогиал» и «Эстрогиал Плюс») в качестве основных активных компонентов содержатся натриевая соль гиалуроновой кислоты и фитокомплекс – экстракты шишек хмеля, травы клевера, а также цветков календулы.
Крем дозированный имеет форму свечей для удобства введения и упакован в контурные ячейки. Крем дозированный «Эстрогиал» и «Эстрогиал Плюс» отличаются составом вспомогательных компонентов. «Эстрогиал Плюс» имеет более насыщенную жирами основу и рекомендуется при более выраженной атрофии.
Экстракт цветков календулы оказывает антиоксидантное, противовоспалительное действия, увеличивает скорость регенерационных процессов в тканях, способствует восстановлению и формированию эпителия в области повреждения. Экстракт травы клевера (фитоэстроген, содержащий 4 изофлавона) – антиоксидант, стимулирует синтез коллагена и гиалуроновой кислоты, способствует гидратации слизистых оболочек, имеет выраженное успокаивающее действие на раздраженную кожу и слизистые, бактерицидные свойства позволяют устранять зуд и дискомфорт. Экстракт шишек хмеля обладает противовоспалительным, бактерицидным, тонизирующим действиями, активирует выработку эластина и коллагена. Всем пациентам с САЛ рекомендуется применять следующие увлажняющие и смягчающие средства: гиалуронат натрия в комбинации с фитокомплексом в форме дозированного крема – в преддверие влагалища по 1 дозе 1–2 раза в день в течение 20–30 дней, далее 2–3 раза в неделю в течение 3–4 недель, затем 1–2 раза в неделю (длительность применения не ограничена); и/или гиалуронат натрия в комбинации с фитокомплексом в форме геля для наружного применения – по 1–2 аппликации в день, длительность применения не ограничена [13]. При необходимости возможно сочетание обеих форм для усиления эффекта.
В проведенном исследовании показана высокая эффективность применения комбинированной терапии САЛ в виде 3-месячного курса терапии топическими ГКС наряду с длительным применением средств на основе низкомолекулярной гиалуроновой кислоты («Эстрогиал»), обладающей высокой способностью всасывания в слои кожи и слизистых оболочек с целью увлажнения тканей и поддержания естественного защитного барьера. Согласно инструкции по применению, средство «Эстрогиал» применяется топически при наличии жалоб на зуд, сухость, диспареунию, дискомфорт различного генеза в области половых органов как комплексно, так и в монотерапии. Компоненты, входящие в состав средства «Эстрогиал», способствуют устранению большинства атрофических симптомов в аногенитальной области, ассоциированных с зудом, сухостью, раздражением и болезненностью. Кроме того, «Эстрогиал» обладает выраженным аддитивным эффектом к сильнодействующим ГКС, что было продемонстрировано как в данном исследовании, так и в других работах [14].
Заключение
Длительная терапия топическими ГКС (мометазона фуроатом 0,1% 1 раз в сутки в течение 3 месяцев) приводит к улучшению течения САЛ вульвы у женщин на начальных этапах, однако не предотвращает развитие рецидива заболевания. Применение крема дозированного и геля «Эстрогиал» в составе комплексной терапии с топическими ГКС приводило к лучшим результатам лечения в течение первых 3 месяцев наблюдения по сравнению с изолированной терапией ГКС. Монотерапия средствами низкомолекулярной гиалуроновой кислоты в последующие 3 месяца приводила к значительному снижению рецидивов заболевания. Крем дозированный и гель для локального применения «Эстрогиал» могут рассматриваться как дополнение к базисной терапии САЛ.



