Проблема задержки роста плода не теряет своей актуальности не только в рамках клинических специальностей (акушерство-гинекология, неонатология, перинатология, педиатрия), но также в структуре общественного здравоохранения. Ее решение позволит обеспечить максимально раннюю профилактику не только осложнений в раннем неонатальном периоде, но и ряда хронических заболеваний [1, 2]. Данный синдром является основной детерминантой перинатальной и детской смертности/заболеваемости, а также формирования хронических заболеваний уже во взрослом возрасте (неврологические, сердечно-сосудистые, метаболические и другие расстройства) [3–5].
Под задержкой роста плода понимают патологическое состояние, возникающее, когда плод не может достичь генетически обусловленного потенциала роста. Этот синдром полиэтиологичен и включает в себя факторы как со стороны беременной, так и плода, а также плаценты. При этом патологические изменения в последней являются наиболее частой причиной данного осложнения [6–9].
По данным мировой статистики, задержка роста плода сопровождает около 10% всех беременностей, в структуре перинатальной смертности занимает второе место и составляет около 30% числа всех мертворождений; является одной из ведущих причин ятрогенных преждевременных родов и внутриутробной гипоксии у плода [2, 10–12]. Следует отметить, что частота встречаемости данной патологии варьирует в зависимости от уровня экономического развития в различных странах мира, достигая 25% в странах с низким и средним уровнями доходов [1, 13, 14]. Отмечено, что, несмотря на большое количество исследований, в настоящее время точно определить частоту встречаемости задержки роста плода во всем мире достаточно сложно в связи с сохраняющейся недостаточной специфичностью методов предикции и диагностики [15–18]. Для развивающихся стран это осложняется фактом отсутствия стандартного ультразвукового исследования, в том числе для определения точного срока беременности, не говоря уже о качественном проведении первого генетического скрининга с расчетом рисков формирования задержки роста плода [19–21].
По данным Crovetto F. et al. [22], для развитых стран частота прогнозирования задержки роста плода варьирует от 12 до 47%, а частота ложноположительных результатов составляет около 10%, что и определяет важность данной акушерской проблемы. Гуменюк Е.Г. и соавт. [23] подробно проанализировали историю изучения и поиска предикторов задержки роста плода. Авторами были показаны ограничения в использовании как классических методов (определение высоты стояния дна матки, ультразвуковой фетометрии), так и более современных методов (например, определение риска формирования задержки роста плода по данным первого генетического скрининга). В последнее время стали появляться результаты метаболомных исследований с применением искусственного интеллекта, что, по мнению ряда авторов, открывает перспективы предикции и диагностики данного осложнения [4, 24, 25].
В связи с вышеизложенным актуальным является проведение исследований, направленных на поиск значимых факторов риска, создание и оптимизация моделей прогнозирования и/или диагностики задержки роста плода на основании клинических, анамнестических, ультразвуковых и допплерометрических показателей, которые отвечали бы следующим требованиям: были общеприняты, просты, доступны и внедрены на разных уровнях организации акушерской помощи и регулярно применяемы в практике.
Цель исследования: на основании клинических, анамнестических факторов и данных обследования во время беременности разработать модель прогнозирования и диагностики задержки роста плода.
Материалы и методы
Для реализации поставленной цели исследования проведено ретроспективное когортное исследование, в которое были включены 473 беременные с диагнозом при поступлении «задержка роста плода», «плацентарная недостаточность», а также женщины с физиологически протекающей беременностью, наблюдавшиеся и родоразрешенные в ФГБУ «Национальный медицинский исследовательский центр акушерства, гинекологии и перинатологии им. академика В.И. Кулакова» Минздрава России. Критериями включения явились следующие параметры: отсутствие тяжелой соматической и гинекологической патологии у беременных в возрасте от 18 до 45 лет с одноплодной беременностью, без хромосомной патологии и/или врожденных пороков развития у плода, с антенатально выставленным диагнозом задержки роста плода (согласно критериям Delphi). Критериями исключения из исследования явились: многоплодная беременность, хромосомная патология и пороки развития плода, тяжелая экстрагенитальная патология, беременность, наступившая в результате вспомогательных репродуктивных технологий.
Постнатально была проведена оценка массоростовых показателей у новорожденных (n=473) согласно центильным кривым INTERGROWTH-21, что позволило сформировать основную группу, которую составили 202 беременные с задержкой роста плода. В группу сравнения включены 206 женщин без задержки роста плода, родоразрешенных в сроках, соответствующих срокам в основной группе.
Проведены анализ особенностей соматического и гинекологического анамнеза, особенностей течения беременности и родоразрешения, данных ультразвуковых исследований (УЗИ) и допплерометрии, а также комплексная оценка состояния здоровья новорожденных на этапе госпитализации в неонатальные отделения. На основании выявленных статистически значимых факторов риска были построены математические модели для прогнозирования задержки роста плода.
Статистический анализ
Статистический анализ проводился с использованием программ Statistica 12.6, IBM SPSS Statistics 21. Оценка соответствия нормальному распределению количественных показателей проводилась с помощью критерия Шапиро–Уилка (при числе исследуемых менее 50) или критерия Колмогорова–Смирнова (при числе исследуемых более 50). При нормальном распределении описание проводилось с помощью средних арифметических величин (M) и стандартных отклонений (SD), границ 95% доверительного интервала (95% ДИ). При сравнении двух групп по количественному показателю, имевшему нормальное распределение (при равенстве дисперсий), был использован t-критерий Стьюдента; при наличии распределения, отличного от нормального, использован U-критерий Манна–Уитни. При отличном от нормального распределении описание данных проводилось с помощью медианы (Me) и нижнего и верхнего квартилей (Q1; Q3). Анализ четырехпольных таблиц сопряженности выполнен при помощи критерия хи-квадрат Пирсона (при значениях ожидаемого явления более 10), точного критерия Фишера (при значениях ожидаемого явления менее 10), многопольные таблицы сопряженности проанализированы с использованием критерия хи-квадрат Пирсона. Категориальные данные описывались с указанием абсолютных значений и процентных долей. Различия между сравниваемыми величинами признавали значимыми при уровне статистической значимости p<0,05. С целью оценки влияния факторов на формирование патологии плода вычисляли отношение шансов (ОШ) с расчетом 95% доверительного интервала (ДИ).
Построение прогностической модели вероятности определенного исхода выполнялось при помощи метода логистической регрессии. Мерой определенности, указывающей на ту часть дисперсии, которая может быть объяснена с помощью логистической регрессии, служил коэффициент R² Найджелкерка. Для оценки диагностической значимости признаков при прогнозировании определенного исхода применялся метод анализа ROC-кривых, с определением площади под ней (AUC). При соответствии AUC значением 0,9–1,0 информационная ценность оценивалась критерием «качество отличное»; AUC 0,8–0,9 – качество «очень хорошее»; AUC 0,7–0,8 – «хорошее» качество; AUC 0,6–0,7 – «среднее» качество; AUC 0,5–0,6 – «неудовлетворительное» качество. Разделяющее значение количественного признака в точке cut-off определялось по наивысшему значению индекса Юдена. Прогностическая значимость построенных моделей характеризовалась чувствительностью (Se) и специфичностью (Sp).
Результаты
Клинико-анамнестическая характеристика обследованных пациенток представлена в таблице 1. Группы исследования были сопоставимы по возрастным характеристикам.
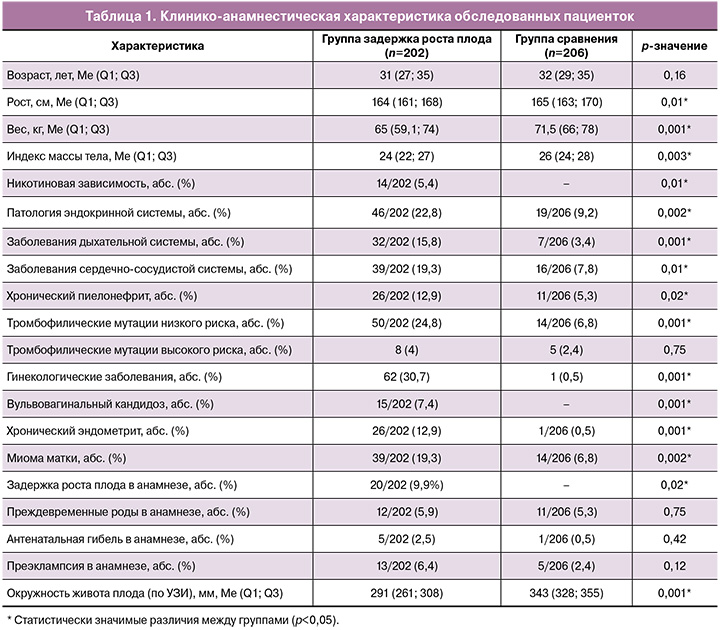
Обращает на себя внимание, что у беременных в группе с задержкой роста плода отмечались более низкие показатели индекса массы тела (p=0,003), а при анализе наследственного анамнеза выявлено, что частота сахарного диабета 2 типа была в 1,8 раза выше, чем в группе сравнения (95% ДИ: 1,04–3,13) (у 59/202 (29,2%) и 38/206 (18,4%) женщин соответственно).
Учитывая влияние хронической никотиновой интоксикации, алкоголизма и наркомании как факторов риска формирования задержки роста плода, проведен анализ их частоты встречаемости в исследуемых группах. Женщины, вошедшие в исследование, не страдали алкогольной и наркотической зависимостью. Вместе с тем хроническая никотиновая интоксикация статистически значимо чаще встречалась в группе с задержкой роста плода – 14/202 (5,4%) (p=0,01).
Анализ структуры соматической патологии установил, что для пациенток основной группы по отношению к группе сравнения была характерна более высокая частота встречаемости патологии эндокринной (в 2,9 раза (95% ДИ: 1,42–5,79) – 46/202 (22,8%) и 19/206 (9,2%) соответственно), дыхательной (в 5,4 раза (95% ДИ: 1,85–15,58) – 32/202 (15,8%) и 7/206 (3,4%) соответственно), сердечно-сосудистой систем (в 2,9 раза (95% ДИ: 1,35–6,22) – 39/202 (19,3%) и 16/206 (7,8%) соответственно), а также хронического пиелонефрита (в 2,8 раза (95% ДИ: 1,10–6,95) – 26/202 (12,9%) и 11/206 (5,3%) соответственно).
Учитывая важность вклада наследственных врожденных тромбофилий (МКБ-10: 099.1, D68.2) в патогенез задержки роста плода, нами была проанализирована частота распространенности данной патологии в исследуемых группах. В основной группе они встречались у каждой третьей женщины, что было в 4,2 раза выше, чем в группе сравнения (95% ДИ: 2,11–8,39; 61/202 (30,2%) и 19/206 (9,2%) соответственно). При этом тромбофилические мутации низкого риска в группе с задержкой роста плода выявлялись в 7,5 раза чаще, чем в группе сравнения (95% ДИ: 2,89–19,37; 50/202 (24,8%) и 14/206 (6,8%) соответственно).
При анализе структуры гинекологической заболеваемости у беременных основной группы по отношению к группе сравнения достоверно чаще диагностировали гинекологические заболевания – 62/202 (30,7%) и 1/206 (0,5%) женщин (95% ДИ: 7,07–379,39): вульвовагинальный кандидоз – 15/202 (7,4%) и 0/206 (0%) (р<0,001), хронический эндометрит – 26/202 (12,9%) и 1/206 (0,5%) (95% ДИ: 2,31–129,12) и миома матки – 39/202 (19,3%) и 14/206 (6,8%) (95% ДИ: 1,48–7,31) пациенток (по группам соответственно).
При анализе акушерского анамнеза установлено, что у каждой десятой беременной основной группы – 20/202 (9,9%) и 0/206 (0%) в анамнезе имело место рождение детей с задержкой роста плода (p=0,02), в 5 раз чаще встречалась антенатальная гибель плода – (5/202 (2,5%) и 1/206 (0,5%) (p=0,42), в 3 раза чаще – преэклампсия – 13/202 (6,4%) и 5/206 (2,4%) (p=0,12) (по группам соответственно). Частота преждевременных родов в анамнезе в группах не различалась – 12/202 (5,9%) и 11/206 (5,3%) (p=0,75) (по группам соответственно) (табл. 1).
Анализ течения беременности и родов установил более высокую частоту угрозы прерывания беременности – 97/202 (48%) и 63/206 (30,6%) (95% ДИ: 1,30–3,39), гипертензивных расстройств – 57/202 (28,2%) и 18/206 (8,7%) (95% ДИ: 2,07–8,69) при задержке роста плода (соответственно по группам). При сопоставлении частоты встречаемости истмико-цервикальной недостаточности, гестационного сахарного диабета, гипотиреоза статистически значимых различий не выявлено (р=0,27, р=0,09, p=0,09).
Медиана срока родоразрешения в основной группе составила 264 (247–272) дня, в группе сравнения – 274 (269–280) дня (р<0,001). В группе с задержкой роста плода очень ранние преждевременные роды встречались в 5 раз чаще, а ранние преждевременные роды – в 2 раза чаще, родоразрешение путем операции кесарева сечения – в 2 раза чаще в экстренном порядке по отношению к группе сравнения – 177/202 (87,6%) и 103/206 (50%) (р<0,001). Показанием для родоразрешения у каждой второй беременной при задержке роста плода было ухудшение его состояния по данным функциональных методов диагностики (р<0,0001), в отличие от группы сравнения, где в каждом третьем случае показаниями были рубец на матке после предыдущего кесарева сечения и/или миомэктомии, а в каждом пятом случае – заключение смежных специалистов о выключении потужного периода (р=0,0003 и р=0,001 соответственно). При оценке длительности пролонгирования беременности от момента постановки диагноза до родоразрешения при задержке роста плода медиана составила 34 (15–84) дня.
Клиническая характеристика новорожденных представлена в таблице 2.
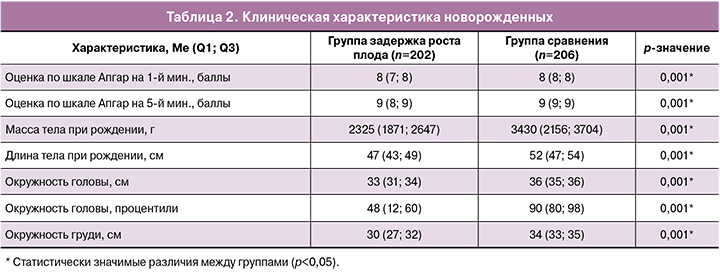
При задержке роста плода отмечались более низкая масса и длина тела, меньшая окружность головы и груди, а также более низкие баллы оценки по шкале Апгар на 1-й и 5-й минутах (р<0,001).
Интерес в работе представлял анализ течения раннего неонатального периода. В структуре неонатальной заболеваемости у новорожденных основной группы отмечалась статистически значимая более высокая частота врожденной пневмонии – 62/202 (30,7%) и 30/206 (14,6%) (р=0,0001), респираторного дистресс-синдрома – 53/202 (26,2%) и 19/206 (9,2%) (р<0,0001), внутрижелудочковых кровоизлияний 1-й степени – 19/202 (9,4%) и 7/206 (3,4%) (р=0,02), ДВС-синдрома – 23/202 (11,4%) и 9/206 (4,4%) (р=0,01), врожденной анемии – 25/202 (12,4%) и 7/206 (3,4%) (р=0,002), гипербилирубинемии недоношенных – 60/202 (29,7%) и 32/206 (15,5%) (р=0,001), неонатального холестаза – 11/202 (5,4%) и 0/206 (0,0%) (р=0,03), дискинезии желудочно-кишечного тракта – 28/202 (13,9%) и 12/206 (5,8%) (р=0,01).
По данным Verlohren S. et al. [16] и Hoopmann M. et al. [26], эффективность антенатальной диагностики и предикции задержки роста плода составляет в среднем 29,9–32,0%. Sharp A. et al. [20] указывают, что, несмотря на рутинность проведения УЗИ при беременности, антенатально возможно выявить от 10 до 36% новорожденных с массой тела при рождении <10-го процентиля. Вместе с тем при проведении аудитов оказываемой перинатальной помощи (УЗИ) часто выявляется неадекватная диагностика задержки роста плода [19, 21, 24, 26, 27].
Учитывая необходимость повышения предиктивной и диагностической эффективности задержки роста плода на следующем этапе исследования на основании применения метода бинарной логистической регрессии, нами была разработана прогностическая модель, включающая клинико-анамнестические факторы риска.
Наблюдаемая зависимость описывается следующим уравнением:
P=1/(1+e-z),
z=1,068X1+1,139X2+2,562X3+0,935X4+23,203 X5-0,043,
где P – вероятность наличия задержки роста плода, X1 – хронический пиелонефрит (0 – не было, 1 – был), X2 – тромбофилические мутации низкого риска (0 – не было, 1 – были), X3 – хронический эндометрит (0 – нет, 1 – есть), X4 – миома матки (0 – нет, 1 – есть), X5 – рождение детей с задержкой роста плода в анамнезе (0 – нет, 1 – есть).
Полученная регрессионная модель является статистически значимой (p<0,001). Исходя из значения коэффициента детерминации Найджелкерка, модель объясняет 24,1% наблюдаемой дисперсии наличия задержки роста плода. Данный показатель согласуется с данными Armengaud J.B. et al. [28], указывающими, что задержка роста плода встречается при 10–15% всех беременностей.
При оценке зависимости вероятности развития задержки роста плода от значения логистической функции P с помощью ROC-анализа была получена следующая кривая (рис. 1).
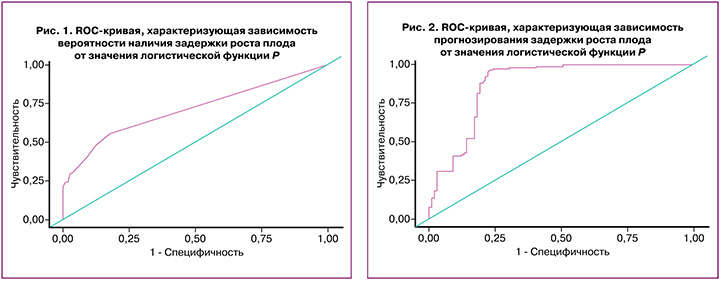
Площадь под ROC-кривой составила 0,71 с 95% ДИ: 0,65–0,77. Полученная модель была статистически значимой (р<0,001).
Пороговое значение логистической функции P в точке cut-off, которому соответствовало наивысшее значение индекса Юдена, составило 0,7. Развитие задержки роста плода прогнозировалось при значении логистической функции P выше данной величины или равном ей. Чувствительность и специфичность модели составили 55,6 и 82,3% соответственно.
На следующем этапе исследования, учитывая необходимость повышения предикции задержки роста плода во время беременности, создана модель, включающая, помимо клинико-анамнестических данных, параметры, полученные при УЗИ во время беременности, такие как масса плода (в граммах и в процентилях), окружность живота (мм), бипариетальный размер головки (мм). Модель была разработана с помощью метода бинарной логистической регрессии. После статистической обработки параметров в конечную формулу включен лишь ультразвуковой показатель «окружность живота».
Наблюдаемая зависимость описана уравнением:
P=1/(1+e-z),
z=41,445+0,475X1+0,501X2+3,35X3+0,832X4-0,131X6,
где P – вероятность наличия задержки роста плода, X1 – хронический пиелонефрит (0 – не было, 1 – был), X2 – тромбофилические мутации низкого риска (0 – не было, 1 – были), X3 – хронический эндометрит (0 – нет, 1 – есть), X4 – миома матки (0 – нет, 1 – есть), X6 – окружность живота, мм.
Полученная регрессионная модель прогнозирования и диагностики задержки роста плода является статистически значимой (р<0,001). Исходя из значения коэффициента детерминации Найджелкерка, модель объясняет 80,1% наблюдаемой дисперсии задержки роста плода.
При оценке зависимости вероятности прогнозирования задержки роста плода от значения логистической функции P с помощью ROC-анализа была получена следующая кривая (рис. 2).
Площадь под ROC-кривой составила 0,87 с 95% ДИ: 0,83–0,92. Полученная модель была статистически значимой (р<0,001).
Пороговое значение логистической функции P в точке cut-off, которому соответствовало наивысшее значение индекса Юдена, составило 0,5. Задержка роста плода диагностировалась при значении логистической функции P выше данной величины или равном ей. Чувствительность и специфичность модели составили 96,7 и 76,8% (соответственно).
В ходе исследования была получена прогностическая модель 1 с чувствительностью и специфичностью 55,6 и 82,3% соответственно. Однако для верификации задержки роста плода на разных сроках беременности нами были внесены полученные ультразвуковые параметры, что позволило получить диагностическую модель 2 с высокими показателями чувствительности и специфичности – 96,7 и 76,8% (соответственно). Следует отметить, что окружность живота является достаточно рутинным и простым для определения показателем при проведении фетометрии, не требующим использования специальных ультразвуковых формул для его расчета, что позволяет снизить вероятность ошибки при проведении УЗИ. Также данный параметр определяется повсеместно вне зависимости от степени квалификации врача ультразвуковой диагностики, что позволит в дальнейшем обеспечить маршрутизацию беременной.
Обсуждение
Задержка роста плода является важной проблемой как для акушеров-гинекологов, так и для неонатологов во всем мире. В-первую очередь это связано с полиэтиологичностью данного осложнения, вследствие чего предикция и своевременная диагностика, как и возможное последующее лечение, сложны и все еще недостаточно изучены. Несмотря на многочисленные исследования в антенатальном периоде, лишь очень немногие являются достаточно надежными, чтобы быть использованными в клинической практике. Диагностика задержки роста плода с помощью рутинного УЗИ или измерения высоты дна матки над лоном является неоптимальной, что и приводит к запоздалой диагностике данного состояния [1, 2, 11, 19]. Обращает на себя внимание работа Haragan A. et al. [24], которые описывают и признают ограничения УЗИ для прогнозирования предполагаемой массы плода в популяции. В ходе исследования было выявлено, что УЗИ завышает предполагаемую массу плода более чем у 75% новорожденных, вошедших в исследование. Это было особенно ярко показано для новорожденных с задержкой роста плода или детей, рожденных маловесными: 32% имели чрезмерную ультразвуковую ошибку в прогнозировании их массы тела на момент рождения. При этом наиболее значимым это было у новорожденных с массой тела менее 500 г. На формирование описываемой погрешности не влияет выбор формулы для расчета веса плода, так как проведенное Hoopmann M. et al. [26] исследование не выявило большую точность какой-либо формулы, используемой для определения предполагаемой массы плода.
В настоящее время предложено использование различных биохимических маркеров сыворотки крови в качестве «маркеров плацентарной дисфункции»: связанный с беременностью белок плазмы A (PAPP-A), активин, растворимая FMS-подобная тирозинкиназа 1 (SFLT-2), плацентарный фактор роста (PlGF), ингибин A. Они имеют доказанную корреляцию с неблагоприятными исходами беременности и входят в клиническую практику в развитых странах. Однако принимая во внимание дороговизну и возникающую из-за этого сложность внедрения в развивающихся странах, происходит ограничение данного метода [16, 29].
Особый интерес представляет использование модели прогнозирования задержки роста плода на основании сочетания маркеров, основанных на выявлении плацентарной дисфункции (соотношение sFlt-1/PlGF), с такими параметрами допплерометрии, как пульсационный индекс маточных артерий, которая в исследованиях показала улучшение частоты выявления случаев данного осложнения. Однако, по данным García B. et al. [21], универсальный скрининг во II триместре с использованием определения пульсационного индекса в маточных артериях для выявления задержки роста плода имеет чувствительность 60–80% и специфичность 90–95%, однако обладает низкой положительной прогностической ценностью 10–20%. В своей работе Herraiz I. et al. [29] определили, что оптимальным сроком использования оценки соотношения sFlt-1/PlGF в сочетании с определением пульсационного индекса в маточных артериях для выявления задержки роста плода в группе женщин с высоким риском развития (на основании данных 1 скрининга и анамнестических, соматических факторов риска) является проведение оценки на 26-й неделе беременности. Тем не менее остается открытым вопрос, надо ли оценивать соотношение данных маркеров и пульсационного индекса в маточных артериях в группах низкого риска по данным 1 скрининга или при увеличении индекса при нормально протекающей беременности. Papastefanou I. et al. [18] разработали новую модель конкурирующих рисков для прогнозирования рождения плодов с задержкой роста и маловесных к сроку гестации и продемонстрировали, что новый подход имеет более высокую эффективность по сравнению с традиционными методами. Однако использование допплерометрии маточных артерий, несомненно, требует соответствующей подготовки специалистов УЗИ, наличия соответствующей техники, что может являться сложным вопросом в развивающихся странах, а внедрение общей методологии может быть проблематичным и в развитых странах, учитывая разную степень знаний и квалификации специалистов ультразвуковой диагностики. Авторы отмечают, что остался не решенным пока вопрос об использовании данной модели в группе беременных с высоким риском задержки роста плода.
В связи с вышеизложенным полученная нами в исследовании модель 2, включающая как клинико-анамнестические факторы риска, так и ультразвуковые параметры, а именно окружность живота, позволяет верифицировать диагноз задержки роста плода и улучшить диагностику антенатально. Преимуществом данной модели является отсутствие инвазивных маркеров, таких как биохимические параметры (PAPP-A, активин, SFLT-2, PlGF, ингибин A), в отличие от исследования модели, основанной на соотношении sFlt-1/PlGF с допплерометрией, которые требуют дополнительных экономических вложений, дополнительного обучения специалистов УЗИ, она достаточно проста и может быть использована рутинно в клинической практике. Следует отметить, что, несмотря на то, что полученная модель обладает хорошей чувствительностью и специфичностью, необходимо проведение дальнейших исследований звеньев патогенеза задержки роста плода и получения более информативных и достоверных ранних маркеров формирования заболевания с использованием достижений, в том числе мульти-omics подходов. Дальнейшее усовершенствование полученных в результате поиска и анализа факторов риска биометрических параметров плода, математических моделей при помощи omics-технологий, машинного обучения и искусственного интеллекта позволит расширить спектр вопросов по проблеме предикции и своевременной диагностики задержки роста плода.
Заключение
Таким образом, в ходе проведенного исследования была получена прогностическая модель 1 с чувствительностью и специфичностью 55,6 и 82,3% соответственно. Однако для верификации задержки роста плода на разных сроках беременности нами были внесены полученные ультразвуковые параметры, что позволило разработать диагностическую модель 2 с высокими показателями чувствительности и специфичности – 96,7 и 76,8% соответственно, объясняющую 80,1% наблюдаемой дисперсии задержки роста плода. Разработанные на основании применения метода бинарной логистической регрессии модели могут быть предложены для использования в практическом здравоохранении для выделения группы риска, прогнозирования и диагностики задержки роста плода, что позволит провести своевременную профилактику для снижения частоты перинатальных осложнений.



