Папилломавирусная инфекция – одна из наиболее распространенных инфекций, регистрируемых у женщин в различные возрастные периоды. У женщин моложе 40 лет вирус папилломы человека (ВПЧ) обнаруживался в 89% аденокарцином, в возрасте 60 лет и старше – в 43% [1, 2].
Частота передачи инфекции даже при однократном половом контакте может достигать 60–80% [1]. Инфицирование одним или несколькими типами ВПЧ высокого онкогенного риска связывают c 96,7% случаев плоскоклеточного рака шейки матки (РШМ) [2], причем корреляционные связи между ВПЧ и плоскоклеточным РШМ значительно выше, чем между курением и возникновением рака легких. Риск возникновения аденокарциномы шейки матки ряд исследователей также связывает с ВПЧ, при этом корреляционные связи, доказывающие степень возникновения риска, более слабые [2].
Заболеваемость РШМ в Российской Федерации (РФ) по состоянию на 2021 г. составила 124 случая на 100 тыс. женщин, смертность – 8,13 на 100 тыс. женщин в год, с регистрацией максимальных показателей в возрастном диапазоне 15–39 лет [3]. Особого внимания заслуживают не только рак, но и предраковые поражения, предшествующие развитию инвазивного цервикального рака, которые, согласно цитологической классификации Bethesda, именуются плоскоклеточными интраэпителиальными поражениями (squamous intraepithelial lesion, SIL), а по гистологической классификации – интраэпителиальными неоплазиями шейки матки (cervical intraepithelial neoplasia, CIN). В различных популяциях частота SIL низкой степени колеблется в пределах 1,5–7,7%, SIL высокой степени – 0,4–1,5% [4–6]. CIN I–II наиболее часто выявляются у женщин в возрасте 24–27 лет, а CIN III – в 35–42 года [6].
Независимо от тяжести CIN и наличия ВПЧ-инфекции высокого риска вероятность регрессии заболевания снижается на 21% каждые 5 лет [6]. Так, LSIL (CIN I) в 50% случаев подвергается обратному развитию, в 10% прогрессирует до HSIL (CIN III) и менее чем у 2% пациенток переходит в инвазивный РШМ. Встречаемость и исходы SIL описаны только в диссертационных исследованиях, научных статьях, но не в статистических отчетах. Создание информационных систем для регистрации заболеваемости SIL – мероприятие, требующее экстренного решения в масштабах страны. Электронный регистр пациенток, разработанный для настоящего исследования, может стать моделью организованной системы сбора информации о пациентках, имеющих заболевания шейки матки, взятых на учет территориальными органами здравоохранения. В регистр включены женщины с диагнозами по МКБ-10: N87.X + B97.7 CIN I–II, получающие/получившие конкретное лечение.
C точки зрения фармакоэпидемиологии регистр является проспективным, обсервационным (наблюдательным) когортным исследованием пациентов с конкретным заболеванием, определенными факторами риска или одинаковым клиническим состоянием [7]. Обоснованность создания регистра с эпидемиологической точки зрения связана с важностью оценки эпидемиологии изучаемых и описываемых заболеваний, рутинной клинической практики и динамического наблюдения за пациентками [8].
В РФ регистры пациентов уже активно применяются в ряде областей медицины (онкология, лечение сахарного диабета). В масштабах мировой эпидемиологической практики гинекологические регистры распространены достаточно широко. Например, в Австралии, где весьма эффективно осуществляется программа скрининга заболеваний шейки матки в рамках общенационального скринингового онкологического регистра, отслеживаются случаи выявления ВПЧ и анализируется их связь с заболеваниями шейки матки [9]. В Ирландии существует регистр цервикального скрининга, с помощью которого не только отслеживаются эпидемиологические особенности заболеваний шейки матки, но и осуществляются напоминания пациентам, рассылаются извещения о необходимости обследований или иных манипуляций [10, 11].
В настоящее время тактикой при выраженной дисплазии шейки матки является хирургическое вмешательство [12], которое устраняет морфологические проявления ВПЧ-опосредованного цервикального канцерогенеза, но не влияет на состояние факторов противовирусного иммунитета – важной составляющей в стратегии терапии ВПЧ-ассоциированных поражений шейки матки. Большинством ученых подтверждается тот факт, что ВПЧ-ассоциированные поражения шейки матки развиваются в сочетании с иммунными нарушениями в виде уменьшения количества и снижения функционально-метаболического статуса Т- и В-лимфоцитов, субпопуляционного состава этих клеток, баланса про- и противовоспалительных цитокинов, α-интерферонов: обнаружено 5-кратное повышение концентрации интерлейкина ИЛ-1α и ИЛ-1β на фоне низкого уровня ИЛ-8, фактора некроза опухоли (ФНО)-α, интерферона (ИФН)-α [13]. Таким образом, тактика лечения должна учитывать патогенетические механизмы взаимодействия ВПЧ и иммунной системы человека, достоверно влияющие на исход заболевания.
Цель исследования: оценить влияние иммуномодулирующих препаратов на изменения кольпоскопических и цитологических характеристик при ВПЧ-ассоциированных поражениях шейки матки.
Материалы и методы
Для анализа влияния иммуномодулирующих препаратов на состояние пациенток, имеющих изменения кольпоскопических и цитологических характеристик при ВПЧ-ассоциированных поражениях шейки матки, был создан электронный регистр. Основой его создания стала наблюдательная программа «Оценка эффективности и безопасности препарата «Иммуномакс» в комплексной терапии доброкачественных дисплазий шейки матки при подтвержденной ВПЧ-инфекции», которая была реализована в 2020–2021 гг. на базе территориальных женских консультаций 7 регионов Российской Федерации: Москвы, Волгограда, Краснодара, Нижнего Новгорода, Ростова-на-Дону, Санкт-Петербурга. В программу были включены обезличенные данные 500 женщин с ВПЧ-ассоциированными поражениями шейки матки в возрасте от 18 до 60 лет, полученные в результате открытого, многоцентрового, рандомизированного исследования. Медиана возраста обследуемых – 33 года.
Критерии включения в исследование: добровольное согласие, наличие доброкачественных ВПЧ-ассоциированных заболеваний шейки матки (МКБ-10: N87.X + B97.7 CIN I–II), отсутствие беременности и согласие использовать надежные методы барьерной контрацепции на весь период исследования. Критерии невключения: РШМ, включая carcinoma in situ, беременность, лактация; наличие выраженных нарушений функции почек и/или печени; алкогольная или наркотическая зависимость, психические заболевания в анамнезе; активный туберкулез; аллергические реакции, вирусные и бактериальные заболевания дыхательных путей, использование иммуномодулирующей терапии в период до 6 месяцев от начала надлежащего исследования. Критерии исключения: выявление в процессе исследования несоответствия критериям включения/невключения; нарушение пациентом процедур «Протокола исследования» и/или режима лечебного учреждения; отказ от участия в исследовании и отзыв письменного информированного согласия; решение врача-исследователя для пользы пациента прекратить его участие в исследовании (непереносимость препарата, развитие серьезных нежелательных явлений, неэффективность проводимой монотерапии и т. п.).
Женщины, включенные в исследование, были обследованы в соответствии со стандартами, принятыми при данном заболевании. Изучены анамнестические данные, осуществлен осмотр шейки матки в зеркалах, проведена визуальная оценка шейки матки после обработки уксусной кислотой (VIA). Проведен забор материала для бактериоскопического и цитологического исследования содержимого экзо- и эндоцервикса. Молекулярно-генетическое исследование проводилось методами качественной детекции ВПЧ методом ПЦР. Лабораторно подтверждена ВПЧ-инфекция у 100% пациенток. При обнаружении аномальной кольпоскопической картины либо при расхождении результатов цитологического исследования, ВПЧ-тестирования и данных кольпоскопии проводилась прицельная биопсия шейки матки (punch-биопсия). Основным методом терапии было эксцизионное воздействие, назначенное всем участницам исследования. В послеоперационном периоде были использованы иммуномодулирующие препараты «Иммуномакс», «Аллокин-альфа», препараты с МНН инозин пранобекс [13–19], назначенные в соответствии с инструкциями производителя. 59 пациенток с диагнозом N87.X + B97.7 CIN I–II получали хирургическое лечение без иммуномодулирующей терапии. Через 3 и 6 месяцев после окончания лечения проводилась повторная ПЦР-детекция ВПЧ, цитологическое и кольпоскопическое исследование.
Статистический анализ
Статистические расчеты проведены попарным сравнением показателей дисперсий с использованием одностороннего точного критерия Фишера.
Данные об элиминации ВПЧ, нормализации кольпоскопической картины при использовании иммуномодулирующих препаратов и без них проанализированы на основании оценки критерия и величины Хи-квадрат (χ2). Уровень значимости принят равным стандартному значению 0,05. Таким образом, нулевая гипотеза исследования отвергалась при p>0,05.
За «нулевую гипотезу» исследования было принято следующее утверждение: «При применении изучаемого препарата происходит нормализация оцениваемого параметра, без применения препарата нормализация не происходит». Подтверждение либо опровержение «нулевой гипотезы» для результатов, полученных после применения иммуномодулирующих препаратов, осуществляется на основе величины χ2, определяемой путем расчета критерия разницы между ожидаемым и наблюдаемым показателями по формуле:
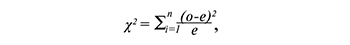
где o – наблюдаемый результат, e – ожидаемый результат.
Этические аспекты исследования
Исследование проведено в соответствии с Хельсинкской декларацией Всемирной медицинской организации (Сеул, 2008), Правилами надлежащей клинической практики и применяемыми на территории РФ нормативными документами для открытого, многоцентрового, рандомизированного исследования. Всеми женщинами подписано информированное добровольное согласие на участие, отказа от участия в исследовании не было.
Результаты
Возраст женщин, включенных в исследование от 18 до 55 лет (медиана возраста – 33 года). 100% пациенток имели правильно развитые вторичные половые признаки, индекс массы тела от 18,5 до 24,99, у 85,5% женщин менструальный цикл был регулярным, у 14,5% менструации были нерегулярными. Средний возраст начала половой жизни 16,3±0,7 года, 56,5% пациенток имели постоянного партнера, 44,5% указывали на наличие 3 и более половых партнеров. На наличие цервицита в анамнезе указали 85,8% женщин, у 37,6% в анамнезе имел место острый эндометрит, у 26,3% – воспалительный процесс придатков матки, у 89,1% – вульвовагинит. При осмотре пациентки указывали, что при выявлении вышеперечисленных заболеваний всегда проводилось соответствующее лечение. Генотипы ВПЧ высокого канцерогенного риска (ВКР) распределились, как показано на рисунке 1.

У пациенток с ВПЧ-ассоциированными поражениями шейки матки были выявлены генотипы ВКР: ВПЧ 16, 18, 31, 33, 45. Наибольший процент женщин имели ВПЧ 16, полученные результаты согласуются с выводами ранее проведенных исследований [20, 21]. Распределение генотипов ВПЧ низкого канцерогенного риска (НКР) представлено на рисунке 2.
У пациенток с ВПЧ-ассоциированными поражениями шейки матки были выявлены генотипы НКР: ВПЧ 6, 26, 39, 44, 52, 56, 58, 59, 68. Наибольший процент женщин имели ВПЧ 11, полученные результаты согласуются с выводами ранее проведенных исследований [22, 23]. У пациенток с CIN, включенных в исследование, выявлено более 1 типа ВПЧ. В ассоциациях высокоонкогенных и низкоонкогенных штаммов присутствовали ВПЧ 33, 18, 16, 6, 51, 35, 56, 45, 44, 11, 59, 39, 52, 66, 53, 58, 68,73. Анализ пациенток с CIN, инфицированных более чем 1 генотипом ВПЧ, представлен на рисунке 3.
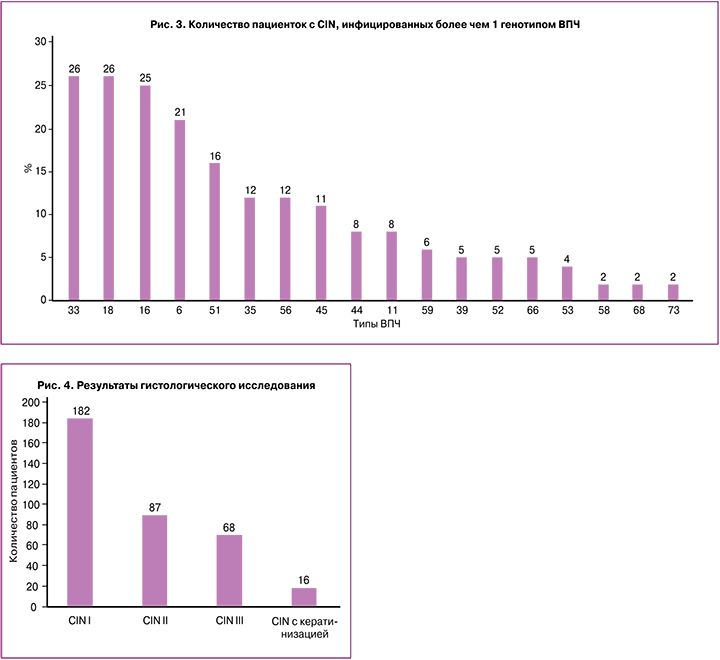
По результатам гистологического исследования CIN различной степени были обнаружены у 182 женщин, при этом CIN I – у 87 пациенток, CIN II – у 68, CIN III – у 11 и CIN с кератинизацией (лейкоплакия с атипией) – у 16 (рис. 4).
Отсутствие элиминации ВПЧ в зависимости от применяемой иммуномодулирующей терапии
В комплексной терапии пациенток, включенных в регистр, были использованы препараты «Иммуномакс» (n=114), «Аллокин-альфа» (n=95) и препараты с МНН инозин пранобекс (n=154), данные об отсутствии элиминации ВПЧ в зависимости от применяемой иммуномодулирующей терапии представлены на рисунке 5.
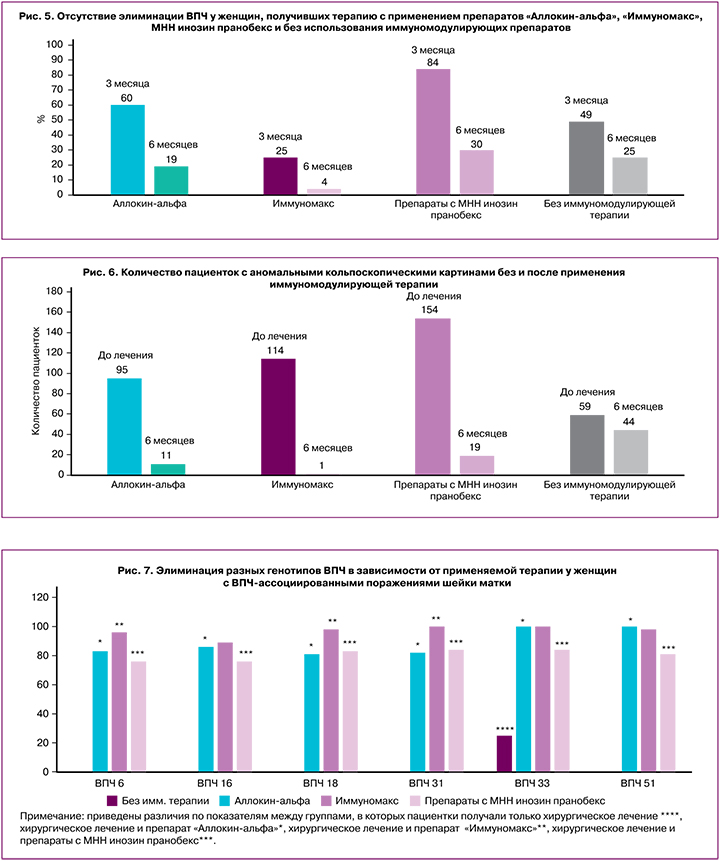
Элиминация ВПЧ через 6 месяцев у пациенток, имеющих положительные результаты на наличие вируса, после применения иммуномодулирующих препаратов «Аллокин-альфа», «Иммуномакс», препаратов с МНН инозин пранобекс значимо отличалась от показателей женщин, получивших только хирургическое лечение. Максимальная эффективность по динамике элиминации ВПЧ зарегистрирована у пациенток, получивших терапию с применением препарата «Иммуномакс».
Среди пациенток с отсутствием элиминации ВПЧ через 6 месяцев после применения препарата «Аллокин-альфа» выявлена реинфекция новым типом ВПЧ (4%), которого не было в момент начала исследования. После применения препарата «Иммуномакс» реинфекция новым типом ВПЧ, которого не было в момент начала исследования, отмечена только у 1% женщин, а после применения препаратов с МНН инозин пранобекс – у 4%.
Кольпоскопическая оценка шейки матки в зависимости от применяемой иммуномодулирующей терапии
Кольпоскопическая оценка шейки матки у женщин, включенных в регистр, проводилась до начала лечения и через 6 месяцев после его окончания. Нормализацией кольпоскопической картины считалась ситуация, когда до начала лечения кольпоскопия была аномальной, а через 6 месяцев после лечения – соответствующей норме. Количество пациенток с нормализацией картины при использовании иммуномодулирующих препаратов представлено на рисунке 6.
Нормализация кольпоскопической картины зарегистрирована во всех группах, где лечение пациенток включало применение иммуномодулирующих препаратов. Проанализирован исход комплексной терапии с применением иммуномодулирующих препаратов при моноинфекции (1 тип ВПЧ) и полиинфекции (2 и более типов ВПЧ). Выявлено, что элиминация ВПЧ была выше у пациенток с единственным типом по сравнению с имеющими 2 и более типов ВПЧ. Частота элиминации ВПЧ 16, 33, 51 была сопоставимой при применении препаратов «Иммуномакс» и «Аллокин-альфа».
Частота элиминации ВПЧ 6, 18 и 31 была максимально высокой у женщин, получавших препараты «Иммуномакс», «Аллокин-альфа», достоверно ниже – у получавших препараты с МНН инозин пранобекс. Сравнение частоты элиминации разных генотипов ВПЧ в зависимости от методов терапии (монотерапия с использованием хирургических методов или комплексная терапия с использованием иммуномодулирующих препаратов) представлено на рисунке 7.
По мере прогрессирования интраэпителиальных неоплазий повышается вероятность перехода ВПЧ-инфекции в интегративную фазу, поэтому отдельно была проанализирована частота элиминации ВПЧ в зависимости от применяемой терапии у пациенток с подтвержденной цервикальной интраэпителиальной неоплазией (CIN) (таблица).
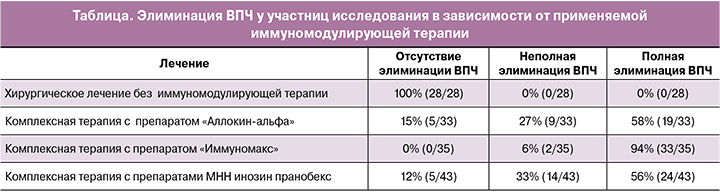
Обсуждение
Результаты исследования показали обоснованность использования иммуномодулирующей терапии при лечении ВПЧ-ассоциированных поражений шейки матки. Данные, полученные в результате открытого, многоцентрового, рандомизированного исследования, включены в электронный регистр. Анализ полученных результатов выявил распространенность коинфицирования женщин с ВПЧ-ассоциированными поражениями шейки матки несколькими типами ВПЧ: единственный тип ВПЧ – 54%, 2 типа ВПЧ – 45%, более 2 типов ВПЧ – 11%, что подтверждается результатами ранее проведенных эпидемиологических исследований [24, 25].
CIN ассоциировалась с 6, 11, 16, 18, 31, 33, 45 типами ВПЧ, а при инфицировании двумя и более типами ВПЧ встречались как ВПЧ 6, 16, 18, 33, 35, 45, 51, 56 типов, так и генотипов 16, 18, 33, 6, что подтверждает следующие результаты: инфицирование ВПЧ как высокого, так и низкого канцерогенного риска способно привести к развитию цервикальной дисплазии легкой степени (L-SIL или CIN I) [26–30].
Анализ данных регистра математически подтверждает эффективность применения комплексной терапии для элиминации ВПЧ в клинической практике: иммуномодулирующая терапия способствует элиминации ВПЧ, снижению частоты аномальных кольпоскопических картин, перспективна в канцеропревенции ВПЧ-ассоциированных заболеваний.
Учет эффективности проводимых диагностических и лечебных мероприятий с помощью созданного регистра позволит использовать возможности персонифицированных подходов к лечению ВПЧ-ассоциированных заболеваний шейки матки.
Ранее представленные данные о том, что иммунотерапия предраковых кожных образований снизила на 75% риск развития плоскоклеточной карциномы [21, 31], служат обоснованием для включения патологических изменений шейки матки в перечень терапевтических мишеней для иммуномодулирующей терапии. Проведенный авторами исследования анализ показал, что элиминация ВПЧ и нормализация кольпоскопической картины у пациенток статистически значимо связаны с применением комплексной терапии, а в ее отсутствие носят случайный характер; уровень эффективного воздействия препарата «Иммуномакс» на элиминацию ВПЧ и нормализацию кольпоскопических картин статистически значимо выше, чем препарата «Аллокин альфа» и препаратов с МНН инозин пранобекс.
Заключение
Комплексный подход к терапии ВПЧ-ассоциированных заболеваний шейки матки с использованием после эксцизионного иссечения патологически измененной ткани иммуномодулирующей терапии позволяет добиться лучших клинических и эпидемиологических результатов. В качестве перспективы расширения наблюдательных программ в сфере лечения ВПЧ-ассоциированных заболеваний шейки матки предлагается включить в Регистр больше центров, с охватом большинства городов России.



