Состояние репродуктивной функции после ЭМА вызывает множество споров среди ученых, занимающихся данной проблемой [1–5]. Особая актуальность данной проблемы обусловлена все более частым выявлением миомы матки среди пациенток раннего репродуктивного возраста, при этом у многих пациенток миома матки не позволяет реализовать репродуктивную функцию, являясь причиной первичного бесплодия [6–11].
N. Stringer и соавт. указывают на необходимость осторожного применения ЭМА среди пациенток детородного возраста в связи с риском развития преждевременной менопаузы [12, 13]. I. Diaz-Plaza и соавт., наоборот, считают, что риск развития данного осложнения наиболее высок в группе женщин старше 45 лет [14]. В некоторых исследованиях описывается ишемическое поражение яичников в результате эмболизации яичниковой артерии [5, 15]. Принимая во внимание данное осложнение, Hascalic и соавт. рекомендуют воздержаться от ЭМА с целью лечения миомы матки женщинам, планирующим беременность [16]. Однако другие исследования на эту тему показали, что детальное изучение коллатерального анастомозирования до операции позволит избежать подобных ошибок и добиться стойкого положительного эффекта практически в 100% случаев. Имеются сообщения о воз- никновении различных внутриматочных осложнений после проведения ЭМА, которые в дальнейшем могут препятствовать наступлению беременности либо при- водить к невынашиванию [17–19]. Некоторые исследования сообщают о патологии плаценты и гипотрофии плода у беременных после ЭМА [20, 21]. По другим данным, нет существенных различий между физиологически протекающей беременностью и беременностью после ЭМА [22, 23].
Таким образом, описанные в литературе данные о беременности и родах после ЭМА весьма противоречивы, представлены в виде отдельных сообщений о факте беременности и родов и не раскрывают особенностей периода гестации. На кафедре акушерства и гинекологии лечебного факультета № 2 ЭМА, в том числе и с целью лечения миомы матки, применяется с 2003 г., и в настоящий момент мы располагаем опытом проведения более 1500 технически успешных ЭМА. Имея десятилетний опыт применения данного вмешательства, а также достаточное количество успешных беременностей и родов после ЭМА, мы сочли необходимым и актуальным провести данное исследование, целью которого стало изучение особенностей течения беременности и родов у данной категории пациенток.
Материали методы исследования
В рамках исследования нами был проведен клинико-лабораторный анализ течения беременности, родов и послеродового периода у 161 пациентки. Были обследованы 59 беременных, которым в качестве лечения миомы матки до беременности была выполнена ЭМА (I основная группа), 67 беременных с миомой матки, обнаруженной до беременности, у которых с целью лечения миомы матки применялась медикаментозная терапия или лечение миомы не проводилось вовсе (II группа сравнения) и 35 беременных без миомы матки с физиологическим течением беременности и родов (III группа контроля).
Средние размеры ведущего (единственного) миоматозного узла составили: в I группе – 59,6±1,2 см³, во II группе – 56,2±1,5 см³.
Всем пациенткам проводили клиническое обследование, которое включало в себя тщательный сбор анамнеза, с выяснением всех перенесенных заболеваний и оперативных вмешательств, объективный осмотр; специальное акушерское обследование, включающее в себя различные методы; клинико-лабораторное обследование в полном объеме согласно стандартам оказания медицинской помощи с привлечением всех смежных специалистов по показаниям. Все полученные данные проанализированы с использованием персонального компьютера Intel(R)Core™ DuoCPU c пакетом прикладных программ для статистической обработки Microsoft Excel версия ХР, раздел
«Анализ данных», подразделение «Описательная статистика». Статистическая обработка полученных данных проводилась с расчетом следующих параметров: среднее арифметическое (М), ошибка среднего (m), стандартное квадратичное отклонение. Для проверки статистических гипотез были использованы следующие методы: t-критерий Стьюдента (парный и непарный) для оценки количественных данных, непараметрические критерии — χ2 (%2) и критерий Вилкоксона–Манна– Уитни для оценки качественных признаков. Для всех тестов и критериев величин критического уровня значимости принималась равной 0,05, то есть различия признавались статистически значи- мыми при р<0,05.
Результаты исследования и обсуждение
Прерывание беременности по различным причинам произошло у 4 (6,8%) пациенток I группы, у 12 (17,9%) беременных в группе с миомой матки без ЭМА и у 3 (8,6%) пациенток группы контроля. Необходимо отметить, что количество самопроизвольно прервавшихся беременностей в группе с миомой матки без ЭМА было достоверно больше по сравнению с основной (миома+ЭМА) и контрольной группами. При анализе осложнений первого триместра гестации выявлены следующие особенности. Угроза самопроизвольного прерывания беременности в сроке до 13 недель была установлена в 18,2% наблюдений в I группе (миома + ЭМА) и 16,6% наблюдений в III группе, что достоверно отличается от показателей в группе сравнения (38,2%). При этом необходимо отметить, что госпитализация и проведение стационарного лечения в группе сравнения (миома без ЭМА) потребовались у 85,7% (18) пациенток среди всех выявленных беременных с угрозой прерывания беременности (n = 21). Эти данные достоверно отличались от показателей в основной группе и группе контроля. Мы считаем, что снижение частоты угрозы прерывания беременности у пациенток после ЭМА по сравнению с пациентками с миомой матки без ЭМА связано с выключением патологического русла миомы из кровотока, а также с отсутствием ряда гормональных нарушений, которые провоцирует растущая миома матки во время беременности (ЭМА прекращает рост миомы матки). Основные данные по частоте осложнений беременности представлены в табл. 1.
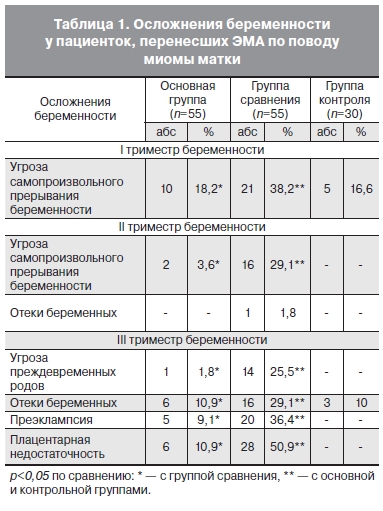
Аномальное расположение плаценты до 13 нед беременности было выявлено среди 5,5% пациенток основной группы (миома+ЭМА) и ни у одной пациентки группы контроля, что достоверно отличалось от показателей в группе сравнения (29,1%). Различия между основной группой и группой контроля были недостоверны. По другим осложнениям первого триместра беременности статистически значимых различий между пациентками всех трех групп не было.
Угроза самопроизвольного прерывания беременности во втором триместре диагностирована у 3,6% пациенток основной группы (миома+ЭМА), что достоверно не отличалось от группы контроля. В группе сравнения (миома без ЭМА) данное осложнение беременности диагностировано в 29,1% случаев. Различия между группой сравнения и основной и контрольной группами носили достоверный характер.
Во втором триместре аномалии расположения плаценты не выявлено ни у одной пациентки основной и контрольных групп, в отличие от группы сравнения: среди пациенток с миомой матки без ЭМА данная патология сохранялась у 12 (21,8%) беременных.
Нарушение питания миоматозного узла до 22 недель беременности не отмечалось ни у одной пациентки I группы (миома+ЭМА), в отличие от пациенток II группы: данное осложнение диагностировано у 4 (7,3%) пациенток. У беременных группы сравнения с нарушением питания миоматозного узла изначальный размер ведущего миоматозного узла превышал 5 см в диаметре и во втором триместре отмечался рост миомы. В основной группе значительный рост миоматозного узла (на 10% и более) диагностирован только у 1 (1,8%) беременной, что достоверно отличалось от группы сравнения: наиболее выраженный рост узлов был установлен среди 9 (16,4%) пациенток II группы. Согласно данным литературы, при беременности происходит увеличение содержания эпидермального фактора роста в миометрии и, соответственно, в миома- тозных узлах, обладающих обширной сосудистой сетью и усиленным кровоснабжением [9, 24]. Также происходят изменения в рецепторном аппа- рате миометрия, характеризующиеся увеличением числа рецепторов к прогестерону и эстрадиолу [24]. Совокупность перечисленных факторов может приводить к выраженному росту миоматозных узлов во время беременности и сопровождаться большим количеством осложнений. Применения ЭМА в качестве метода лечения миомы матки позволило избежать развития данных осложнений, связанных с ростом миомы, в основной группе.
В III триместре угроза преждевременных родов в основной группе (миома + ЭМА) была установлена в 1,8% наблюдений, что достоверно отличалось от группы сравнения (25,5%) и не отличалось от группы контроля (0%). В основной группе лечение всех пациенток было проведено амбулаторно. Стационарное лечение в связи с угрозой преждевременных родов потребовалось среди 57,1% беременных группы сравнения (миома без ЭМА). В контрольной группе угрозы преждевременных родов выявлено не было.
Отеки беременных среди пациенток, перенесших ЭМА, встречались достоверно реже по сравнению с пациентками с миомой матки без ЭМА (табл. 1). При этом у 4 (7,3%) беременных из группы сравнения потребовалось проведение стационарного лечения. Все остальные пациентки получали лечение амбулаторно. Как и отеки беременных, частота преэклампсии в I группе (миома+ЭМА) была достоверно ниже по сравнению с II группой (миома без ЭМА) и статистически не отличалась от группы контроля. Таким образом, согласно нашим данным, частота преэклампсии среди пациенток, перенесших ЭМА, не отличается от частоты преэклампсии при физиологической беременности. Перенесенная ЭМА не оказывает патологического влияния на формирование сосудов плаценты и не увеличивает риск развития преэклампсии. Более того, так как основным эффектом ЭМА является блокада патологической сосудистой сети миомы матки, что приводит к некрозу и перерождению миомы, ЭМА позволяет снизить риск развития преэклампсии у пациенток с миомой матки.
Показатели частоты формирования плацентарной недостаточности (ПН) в I (10,9%) и III (0%) группах были достоверно ниже по сравнению с показателями во II группе (50,9%). Также обращало на себя внимание раннее развитие (до 30 нед беременности) ПН среди пациенток с миомой матки без ЭМА. При этом тяжелое течение ПН, плохо поддающееся медикаментозной коррекции, также чаще встречалось во II группе. Однако, в отличие от общего числа пациенток с ПН, разница была статистически не достоверна. Нарушение питания миоматозного узла в III триместре не диагностировано ни у одной пациентки основной группы (миома+ЭМА), в отличие от пациенток группы сравнения (миома без ЭМА), где данное осложнение было обнаружено у 5,5% пациенток.
Таким образом, течение беременности в группе пациенток после ЭМА не имело статистически значимых различий с течением беременности у пациенток без миомы матки. Осложнения беременности достоверно чаще возникали в группе сравнения среди пациенток с миомой матки, которым ЭМА не проводилась. В целом, течение беременности в основной группе можно характе- ризовать как физиологическое, сравнимое с популяционными данными и показателями группы контроля.
Своевременные роды произошли у 53 (96,4%) пациенток I группы (миома+ЭМА), у 47 (85,5%)пациенток II группы (миома без ЭМА) и у 30 (100%) пациенток III группы. На рис. 1 представлена общая частота осложнений родов (несвоевременное излитие околоплодных вод, первичная слабость родовой деятельности, вторичная слабость родовой деятельности, внутриутробная гипоксия плода, дискоординация родовой деятельности, патология прикрепления плаценты) во всех трех группах по периодам.
Рисунок 1. Общая частота осложнений у пациенток трех групп.
Как видно из рис. 1, общая частота осложнений в течение 1-го и 3-го периодов родов была досто- верно ниже в I (миома+ЭМА) и III группах по сравнению со II группой. При этом статистически значимых различий в течение родов у рожениц после ЭМА и у рожениц контрольной группы без миомы матки не наблюдалось.
Путем операции кесарева сечения были родоразрешены 10 (18,2%) пациенток основной группы, 21 (38,2%) пациентка группы сравнения и 5 (16,7%) контрольной группы. Плановое кесарево сечение было выполнено у 8 (14,5%) пациенток I группы, у 9 (16,4%) пациенток II группы и у 4 (13,3%) пациенток III группы; экстренное – у 2 (3,6%) пациенток основной группы (миома+ЭМА) и 1 (3,3%) пациентки группы контроля, что достоверно ниже показателей группы сравнения (миома без ЭМА) – 12 (21,8%) пациенток.
Основными показаниями к оперативному родоразрешению в основной группе стали: сопутствующая экстрагенитальная патология (3,6%), отягощенный акушерско-гинекологический анамнез у первородящей старше 30 лет (3,6%), сумма относительных акушерских показаний (5,4%). Лишь у 1 (1,8%) пациентки основной группы показанием для родоразрешения путем операции кесарева сечения явился миоматозный узел больших размеров, препятствующий рождению плода. В группе сравнения основными показаниями для кесарева сечения были: рубец на матке после операции кесарева сечения в сочетании с другой акушерской патологией (3,6%), тазовое предлежание плода в сочетании с крупными размерами плода или другой акушерской патологией (5,4%), отягощенный акушерско- гинекологический анамнез у первородящей старше 30 лет (3,6%), декомпенсация ПН (5,4%), отсутствие эффекта от родовозбуждения/стимуляции (5,4%).
При анализе структуры кесарева сечения среди всех трех групп пациенток было выявлено, что перенесенная ЭМА у пациенток основной группы ни в одном случае не стала показанием для абдоминального родоразрешения. Частота проведения кесарева сечения как в плановом, так и в экстренном порядке не отличалась от таковой в группе пациенток без миомы матки и совпадала с общепопуляционными показателями, что, по- видимому, еще раз доказывает, что беременность и роды у пациенток после ЭМА по поводу миомы матки протекают физиологически.
Особый интерес представляет собой анализ состояния новорожденных у данной категории пациенток. Состояние новорожденных при рождении оценивали по шкале Апгар (рис. 2).
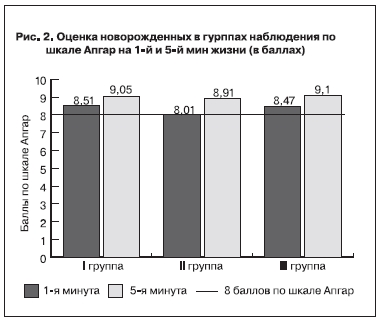
При анализе перинатальных исходов мы обратили внимание на достоверные различия в массе доношенных новорожденных I группы (миома+ЭМА) по сравнению со II (миома без ЭМА) и III группами. Средняя масса новорожденных представлена в табл. 2.
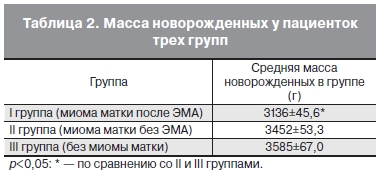
У 47 (85,45%) пациенток основной группы вес новорожденного не превышал 3500 г, при этом у 27 (49,1%) пациенток вес новорожденных не превышал 3000 г. Несмотря на это, необходимо отметить, что ни в одном случае срочных родов (53 (96,4%) из 55) не была диагностирована гипотрофия плода, подавляющее большинство новорожденных основной группы имело оценку по шкале Апгар 8 баллов и выше. Масса тела новорожденных не оказала влияния на течение раннего неонатального периода и дальнейшее развитие детей.
Изучение морфологической структуры последов не выявило признаков ПН. Таким образом, снижение массы тела новорожденных группы пациенток после ЭМА не является патологическим.
Заключение
В результате проведенного исследования мы пришли к выводу, чтоЭМА не оказывает отрицательного влияния на течение беременности и родов. Частота осложнений во время беременности, родов и послеродового периода у пациенток, перенесших ЭМА по поводу миомы матки, достоверно не отличается от таковой у пациенток без миомы матки. ЭМА не является противопоказанием к беременности и родам, а также не является поводом к прерыванию беременности. Таким образом, применение ЭМА для лечения миомы матки у пациенток репродуктивного возраста, планирующих беременность, представляет собой высокоэффективную альтернативу хирургическим и медикаментозным методам лечения.



