В настоящее время в мире отмечается неуклонный рост распространенности воспалительных заболеваний нижнего отдела гениталий, которые являются одной из основных причин обращения женщин на амбулаторно-поликлинический прием. Исследования последних лет демонстрируют увеличение частоты инфекционных поражений органов репродуктивной системы, в особенности обусловленных грибковой инфекцией. Вульвовагинальный кандидоз (ВВК) – инфекционное поражение слизистой оболочки вульвы и влагалища, вызываемое дрожжеподобными грибами рода Candida, которое составляет 30–40% в структуре инфекционной патологии нижнего отдела полового тракта. По различным оценкам исследователей, развитие ВВК вследствие грибковой инфекции является второй по распространенности причиной локальной воспалительной реакции влагалища, шейки матки и вульвы после бактериального вагиноза [1–3]. При этом ВВК является наиболее распространенной кандидозной инфекцией, которая, по общим оценкам, поражает примерно 75% всех женщин хотя бы раз в жизни, у 50% наблюдается повторное возникновение, у 5–10% пациенток развивается рецидивирующий ВВК (4 эпизода в год и более) [4–6]. Так, согласно приблизительным оценкам существующих мировых данных, на сегодняшний день наблюдается около 140 млн случаев рецидивирующего ВВК в год. Заболевание наиболее характерно для женщин репродуктивного возраста [7].
Грибы рода Candida относятся к условно-патогенной микрофлоре, выявляемой как в окружающей среде, так и на поверхности кожных покровов и слизистых оболочках здорового человека (полость рта, кишечник, влагалище). Необходимо отметить, что ВВК не относится к инфекциям, передаваемым половым путем (ИППП). Вместе с тем, не исключена возможность возникновения кандидозного баланопостита у мужчин – половых партнеров женщин с ВВК. Candida spp. свойственен тропизм к тканям, богатым гликогеном, в частности к слизистой влагалища. При снижении защитных сил организма возможно повышение адгезивных свойств грибов с прикреплением их к клеткам эпителия влагалища, колонизацией слизистой оболочки и развитием воспалительной реакции.
В норме во влагалище поддерживается баланс между численностью различных видов микроорганизмов. Ключевую роль в этом играют факторы местного иммунитета и лактобациллы, продуцирующие молочную кислоту, тем самым обеспечивая низкий уровень рН и предотвращение чрезмерного роста патогенов [8, 9]. Основным возбудителем ВВК является вид Candida albicans, выделяемый в 80–90% случаев заболевания. В настоящее время наблюдается увеличение распространенности штаммов Candida non-albicans, к которым относят C. glabrata (7–16% случаев), C. tropicalis, C. krusei, C. parapsilosis. Также часто встречается бессимптомное течение ВВК [10].
Случаи ВВК подразделяются на осложненные и неосложненные. Неосложненный ВВК представляет собой спорадические эпизоды инфекций легкой степени тяжести, вызванные C. albicans. К осложненному течению ВВК относят инфекции, вызванные другими видами Candida или связанные с сопутствующими заболеваниями, например, сахарным диабетом, а также развитие ВВК во время беременности и тяжелое течение ВВК [11].
Для лечения ВВК применяется широкий спектр противогрибковых препаратов (антимикотиков). В основе их классификации чаще всего лежит механизм действия. Выделяют три мишени воздействия антимикотиков на грибы рода Candida spp. – клеточная стенка, клеточная мембрана и ядро. Следует отметить, что 5-фторцитозин ингибирует синтез нуклеиновых кислот в ядре клетки. Полиены (амфотерицин В и нистатин) связываются с эргостеролом, тогда как азолы (флуконазол, миконазол, кетоконазол и др.) ингибируют биосинтез эргостерола, вследствие чего нарушается целостность клеточной мембраны.
Лечение неосложненного ВВК требует кратковременного местного применения противогрибковых препаратов. Альтернативой является однократное применение пероральных препаратов, причем оба варианта имеют сопоставимо высокую эффективность, которая достигает 90% [12].
Одними из наиболее распространенных являются препараты группы азолов, к которым в том числе относится фентиконазол, действующее вещество препарата «Ломексин» 600 мг, капсулы вагинальные. Фентиконазол – это синтетическое производное имидазола с широким спектром противогрибкового (в отношении грибов рода Candida spp., Trichophyton spp.) и противомикробного действия, в том числе в отношении штаммов Staphylococcus aureus, Streptococcus spp., Trichomonas vaginalis, Gardnerella vaginalis [13]. Фунгицидный механизм действия фентиконазола обусловлен взаимодействием с цитохром Р-450-зависимой системой ланостерола, что вызывает аккумуляцию 14-α-метилстеролов и блокирование синтеза эргостерола, обеспечивающего стабильность фосфолипидов клеточной стенки Candida, следовательно, приводит к ее разрушению. Также фунгитоксичность фентиконазола связана с нарушением мембранной проницаемости и блокадой цитохром-оксидазной активности ферментов клеточной мембраны Candida в результате потери энергетического потенциала.
В отличие от других азольных соединений фентиконазол обладает специфическим ингибирующим действием на синтез аспарагиновой протеазы C. albicans, которая обеспечивает адгезию грибов к клеткам эпителия. Эффективность фентиконазола в лечении ВВК сопоставима с другими местными препаратами, также он применяется для лечения смешанных инфекций в нижних отделах половых путей [14, 15].
Цель исследования: оценить эффективность, переносимость и безопасность применения препарата «Ломексин» 600 мг, капсулы вагинальные, у пациенток с неосложненным ВВК.
Материалы и методы
Дизайн исследования: открытое проспективное наблюдательное многоцентровое исследование. Клиническая часть исследования проводилась в период с октября 2021 г. по сентябрь 2022 г. В исследовании приняли участие 125 женщин в возрасте от 19 до 45 лет (средний возраст составил 31±6,5 года). Все пациентки подписали и датировали форму информированного согласия на участие в исследовании.
В исследование были включены пациентки с клиническим диагнозом неосложненного ВВК, подтвержденным клинико-лабораторными методами обследования, индексом массы тела от 18,5 до 30 кг/м2, которые принимали препарат «Ломексин» 600 мг, капсулы вагинальные («Рекордати», Италия) и соблюдали контрацепцию по условиям протокола исследования.
Протокол предусматривал 4 визита: Скрининг (включение в исследование, день -5–0), Визит 1 (начало терапии, день 1), Визит 2 (день 14±2), Визит 3 (месяц 3±5 дней).
На Скрининге, Визите 2 и Визите 3 проводились гинекологическое обследование и микроскопия отделяемого из влагалища. На каждом визите врачом оценивались объективные (эритема, отек, выделения), а пациентками – субъективные (выделения, зуд, жжение, боль) признаки ВВК. Каждый признак оценивался по шкале от 0 до 3, где «0» – отсутствие, «1» – незначительно выражен, «2» – умеренно выражен, «3» – значительно выражен.
Для изучения состава микрофлоры на наличие возбудителей грибковых инфекций использовался метод полимеразной цепной реакции (ПЦР) в реальном времени (тест-система «МикозоСкрин», ООО «ДНК-Технология», Россия). Набор реагентов предназначен для выявления и типирования возбудителей грибковых инфекций родов Candida, Malassezia, Saccharomyces и Debaryomyces: Meyerozyma guilliermondii (C. guilliermondii), Candida albicans, Pichia kudriavzevii (C. krusei), Saccharomyces cerevisiae, Candida auris, Candida tropicalis, Clavispora lusitaniae (C. lusitaniae), Debaryomyces hansenii (C. famata), Candida dubliniensis, Candida glabrata, Candida parapsilosis, Malassezia spp., Kluyveromyces marxianus (C. kefyr), Malassezia furfur. Для выделения ДНК использовали комплект реагентов «ДНК-сорб-АМ» (ООО «НекстБио», Москва, Россия), для постановки реакции использовали детектирующие амплификаторы «DT-96» и «DTprime» (ООО «НПО ДНК-Технология», Россия).
Для оценки локальной воспалительной реакции использовали метод экспрессионного профилирования с помощью комплекта реагентов «ИммуноКвантэкс C/V» (ООО «НПО ДНК-Технология», Москва, Россия), позволяющий сравнить транскрипционный профиль эпителиальных клеток влагалища пациентки с транскрипционным профилем, характерным для локального воспаления. Для оценки транскрипционных профилей использован метод определения соотношения уровней экспрессии генов (IL1b, IL10, IL18, TNFa, TLR4, GATA3, CD68, В2М), позволяющий не осуществлять нормировку на референсные гены, что существенно упрощает исследование. Мерой сходства исследуемого профиля с профилем при воспалительной реакции является индекс воспаления (ИВ). По величине ИВ возможно судить о наличии или отсутствии воспалительной реакции: <50% (низкий) – воспаление отсутствует, 50–60% (промежуточный) – не может быть исключено, >60% (высокий) – выявлено воспаление. Выделение мРНК осуществляли набором «Проба-МЧ-НК-200S».
Кроме того, на Визите 2 пациенткам предлагалось оценить общую переносимость препарата в соответствии с 5-балльной шкалой, где «1» – очень плохая (выраженный дискомфорт, неспособность выполнять никакую работу, значительное снижение повседневной активности), «2» – плохая (постоянный дискомфорт после применения препарата, значительное снижение повседневной активности), «3» – средняя (дискомфорт после применения препарата сохраняется продолжительное время, снижение повседневной активности), «4» – хорошая (незначительный и быстропроходящий дискомфорт после применения препарата, который не влияет на повседневную активность), «5» – очень хорошая (отсутствие любых изменений или чувства дискомфорта).
Все пациентки однократно интравагинально применяли капсулу препарата «Ломексин». Пациентки, у которых наблюдалось улучшение субъективных симптомов, не принимали вторую капсулу препарата, что не противоречило дизайну исследования. На Визите 1 всем пациенткам был выдан Дневник приема препарата, в котором они фиксировали дату применения первой и, при необходимости, второй капсулы препарата «Ломексин», а также выраженность субъективных симптомов заболевания.
Оценку переносимости и безопасности терапии проводили на основании анализа нежелательных реакций, развившихся на фоне применения препарата «Ломексин» 600 мг, капсулы вагинальные, путем оценки жалоб, клинически значимых изменений состояния лабораторных показателей, а также данных гинекологического обследования.
Статистический анализ
Статистическую обработку данных проводили с помощью программы Jamovi версии 2.3.18. Для оценки распределения данных использовался критерий Шапиро–Уилка. Для сравнения данных, соответствующих нормальному распределению, использовался парный t-критерий Стьюдента. Для сравнения данных, не соответствующих нормальному распределению, использовался T-критерий Вилкоксона или критерий Фридмана для повторных измерений. Для оценки различий в частоте наступления событий для повторных измерений использовался критерий МакНемара. Различия считались статистически значимыми при уровне p<0,05.
Для данных, не соответствующих нормальному распределению, в качестве меры центральной тенденции использовали медиану (Ме), а для характеристики рассеяния – межквартильный интервал (Q25%–Q75%).
Результаты
В исследование были включены 125 женщин, которым были проведены Скрининг (день -5–0), Визит 1 (день 1), Визит 2 (день 14±2) и Визит 3 (месяц 3±5 дней). Из 125 женщин 121 пациентка полностью прошли все Визиты и процедуры исследования согласно протоколу и были включены в популяцию для анализа эффективности и безопасности препарата. 4 пациентки завершили исследование досрочно, по причинам, не связанным с эффективностью и переносимостью лечения.
У всех 125 пациенток на Скрининге был подтвержден диагноз неосложненного ВВК как по клиническим, так и по лабораторным признакам. По результатам микроскопического исследования отделяемого из влагалища на Скрининге у всех пациенток были обнаружены дрожжевые клетки (в том числе почкующиеся) или фрагменты псевдомицелия. На фоне снижения или отсутствия лактобацилл в микрофлоре определялись грамположительные кокки, а также повышенное число лейкоцитов (более 20 в поле зрения светового микроскопа, ×1000), что свидетельствует о наличии воспаления. После применения препарата «Ломексин» на Визите 2 и Визите 3 у большинства пациенток не было обнаружено дрожжевых клеток или бактерий, наблюдалось снижение количества лейкоцитов во влагалищном отделяемом.
Согласно данным исследования влагалищного отделяемого методом «МикозоСкрин» на Скрининге у 121/125 (96,8%) пациентки было выявлено наличие возбудителей рода Candida. Такие дрожжеподобные грибы, как Debaryomyces hansenii (C. famata), были обнаружены одновременно с другими кандидами у 2 женщин. Другие грибы, такие как Malassezia furfur, выявлены у 15 пациенток, а Saccharomyces cerevisiae не были обнаружены ни у одной пациентки. Как видно из данных, приведенных в таблице 1, через 14 дней после интравагинального применения препарата «Ломексин» у 117/125 (93,6%) женщин дрожжеподобные грибы рода Саndida не выявлялись, через 3 месяца после применения препарата – у 113/121 (93,4%) женщин не были обнаружены дрожжеподобные грибы.
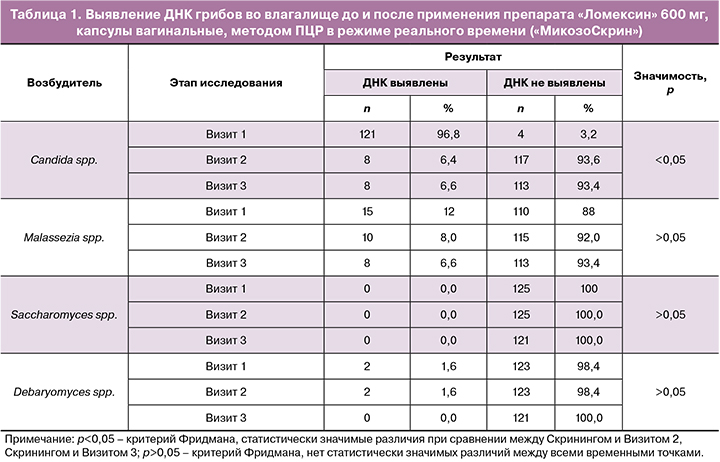
При оценке симптомов ВВК по субъективным признакам на Скрининге 124/125 (99,2%) пациентки отметили наличие выделений, 119/125 (95,2%) – зуд в области вульвы, 100/125 (80%) – жжение, 74/125 (59,2%) – боль различной степени выраженности. Через 14 дней после интравагинального применения препарата «Ломексин» 600 мг (1 или 2 капсулы) только 4/125 (3,2%) пациентки отмечали наличие выделений, 3/125 (2,4%) пациентки – зуд (табл. 2). Ни одна из пациенток не отметила наличия жжения или боли. Были выявлены статистически значимые различия по всем субъективным признакам ВВК между Скринингом и Визитом 2.
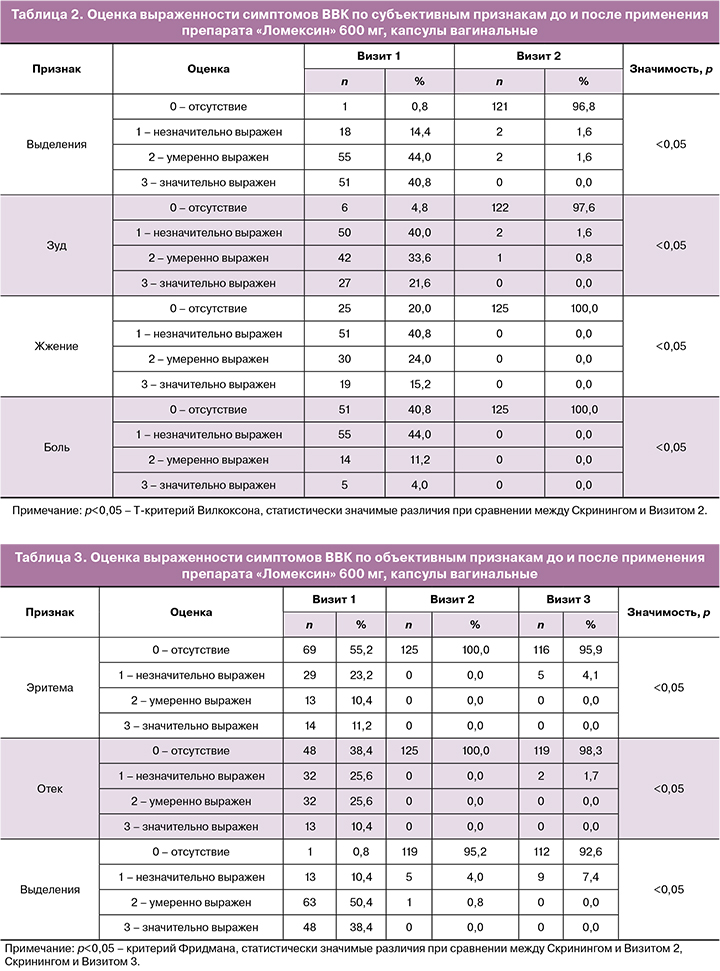
При оценке симптомов ВВК по объективным признакам на Скрининге у 56/125 (44,8%) пациенток была отмечена эритема стенок влагалища, у 77/125 (61,6%) – отек, у 124/125 (99,2%) – наличие выделений различной степени выраженности. На Визите 2 только у 6/125 (4,8%) пациенток отмечалось наличие выделений различной степени выраженности, при этом ни у одной из пациенток не отмечалось эритемы и/или отека (табл. 3). Через 3 месяца после применения препарата на Визите 3 незначительная выраженность эритемы отмечалась у 5/125 (4%) пациенток, отека – у 2/125 (1,6%), выделений – у 9/125 (7,2%). Были выявлены статистически значимые различия по всем объективным признакам ВВК между Скринингом и Визитом 2, между Скринингом и Визитом 3.
У 123/125 (98,4%) пациенток на Скрининге было выявлено наличие локальной воспалительной реакции эпителия влагалища – ИВ составил 99,1 (96,8–100,0)%. У 2 пациенток профиль экспрессии генов иммунного ответа не соответствовал локальному воспалению (ИВ 4,3 и 1,4%). Примечательно, что обе пациентки отмечали субъективно только наличие зуда и выделений. При осмотре у обеих женщин наблюдали только незначительные выделения.
Одну капсулу препарата «Ломексин» применили 32/125 (25,6%) пациентки, 2 капсулы – 93/125 (74,4%).
В ходе оценки безопасности и переносимости препарата только у 2/125 (1,60%) пациенток были выявлены нежелательные реакции: чувство жжения в вульвовагинальной области на 2-й день после применения второй капсулы препарата. Выявленные нежелательные реакции имели легкую степень выраженности, не требовали назначения сопутствующей терапии, медицинского вмешательства, отмены, изменения дозы и режима применения препарата.
В течение исследования по данным гинекологического осмотра не было выявлено клинически значимых отклонений от нормы, кроме тех, которые были связаны с основным заболеванием. По данным оценки общей переносимости препарата по 5-балльной шкале, 119/125 (95,2%) пациенток отметили очень хорошую переносимость препарата, 6/125 (4,8%) пациенток – хорошую переносимость.
Через 14 дней после применения Ломексина ИВ составил 31,8 (28,3–34,8)%. Таким образом, наблюдалось статистически значимое снижение уровня воспаления в процессе лечения (p=2,6×10-21). Из 123 пациенток с провоспалительным профилем экспрессии у 109/123 (88,6%) наблюдалась нормализация профиля экспрессии. Обе пациентки, отмечавшие нежелательные явления в процессе лечения, имели невоспалительный профиль экспрессии генов иммунного ответа после окончания терапии.
Для обеих пациенток с исходно невоспалительным профилем экспрессии ИВ оставался низким. При этом обе отмечали улучшение самочувствия и исчезновение симптомов, отмечавшихся на первом визите.
Обсуждение
Результаты проведенного исследования показали высокую эффективность препарата «Ломексин» по всем исследуемым параметрам через 14 дней и через 3 месяца после применения как одной, так и двух капсул.
Полученные нами результаты согласуются с литературными данными. Так, в нескольких слепых рандомизированных исследованиях было показано, что однократное интравагинальное применение капсул фентиконазола в дозе 600 мг приводило к эрадикации патогенов Candida albicans и снижению выраженности симптомов вагинального кандидоза (эритема, зуд, отек, наличие выделений) у 70 и 90% пациенток [16, 17]. В данных исследованиях не сообщалось о нежелательных местных или системных реакциях во время терапии препаратом.
В похожем открытом рандомизированном исследовании было показано, что через 7 дней после однократного интравагинального применения фентиконазола в дозе 600 мг у 92% пациенток отмечалось значительное снижение интенсивности или исчезновение симптомов ВВК. Через 30 дней после применения препарата у 83,6% пациенток не отмечалось каких-либо признаков заболевания или рецидивов. Кроме того, препарат хорошо переносился пациентками – было зафиксировано всего 5 (6,67%) случаев местных кратковременных нежелательных реакций (чувство жжения, болезненность в области влагалища) [18].
Согласно результатам другого открытого исследования, через 7 дней после однократного применения препарата наблюдалось статистически значимое уменьшение выраженности симптомов заболевания, при этом у 92,3% пациенток был выявлен отрицательный результат исследования на наличие патогенов в микрофлоре влагалища. Тем не менее в течение первых 7 дней терапии 20,1% пациенток применяли препарат повторно в связи с сохранением симптомов или положительным результатом исследования методом «МикозоСкрин». Через 28 дней после первого применения фентиконазола было отмечено полное выздоровление у 94% пациенток. Нежелательные явления во время терапии препаратом возникали очень редко и в основном проявлялись в виде легкого покраснения и зуда в области влагалища в течение первых дней терапии [19].
Заключение
В данном исследовании были продемонстрированы высокая эффективность, хорошая переносимость и безопасность препарата «Ломексин» 600 мг, капсулы вагинальные, в терапии неосложненного ВВК.



