Гормональные контрацептивы за 60 лет своего существования стали не только одним из самых надежных методов предохранения от нежелательной беременности, но и важным компонентом успешной терапии многих гинекологических заболеваний. Однако, с момента выхода на рынок первых комбинированных оральных контрацептивов (КОК) в 60-х годах ХХ в. вплоть до настоящего момента, тромботические осложнения продолжают оставаться на первом месте в списке побочных эффектов данной группы препаратов. За все эти годы было проведено множество исследований, направленных на изучение влияния КОК на систему гемостаза и их роль в патогенезе осложнений, связанных с нарушением свертываемости крови [1, 2]. Благодаря этим исследованиям, с момента появления первых контрацептивов до настоящего времени, препараты прошли большой эволюционный путь, в результате которого не только многократно уменьшилась доза эстрогенов, но и улучшилось качество гестагенов в составе КОК. Таким образом, число случаев тромботических осложнений на фоне приема КОК значительно уменьшилось, но до сих пор является проблемой номер один в современной медицинской практике [3, 4].
В настоящее время установлено, что важнейшей причиной тромботических осложнений являются исходные, порой скрытые, нарушения системы гемостаза, предрасполагающие к повышенному свертыванию крови и тромбозам. КОК даже с низким содержанием эстрогенного компонента могут представлять опасность в условиях генетической или приобретенной тромбофилии, циркуляции антифосфолипидных антител, гипергомоцистеинемии [4, 5]. К сожалению, до сих пор эти важнейшие факторы риска не всегда учитываются при назначении этого метода контрацепции.
Данные, полученные за последнее время о наследственных и приобретенных формах тромбофилии, позволили переосмыслить причины и патогенетические механизмы тромботических осложнений, в том числе в процессе приема КОК. Тромбофилии есть ни что иное, как наследственные или приобретенные дефекты системы гемостаза, предрасполагающие к повышенному тромбообразованию. Согласно данным литературы, каждая мутация или полиморфизм генов различаются по распространенности в популяции, а также механизмам и степени влияния на систему свертывания крови [6—9].
Цель исследования — обоснование необходимости исследования системы гемостаза у женщин, принимающих КОК с целью профилактики венозной тромбоэмболии (ВТЭ).
Материалы и методы
 В работе представлены результаты комплексного клинико-лабораторного обследования 56 пациенток репродуктивного возраста от 18 до 40 лет с тромбозами на фоне приема КОК. На первом этапе клинического обследования особое внимание было уделено изучению анамнеза пациенток, наличию отягощенного семейного тромботического анамнеза. Были собраны подробные сведения о приеме КОК: с какого возраста, с какой целью был назначен препарат, какой конкретно препарат был назначен, длительность приема препарата, при которой произошел тромбоз.
В работе представлены результаты комплексного клинико-лабораторного обследования 56 пациенток репродуктивного возраста от 18 до 40 лет с тромбозами на фоне приема КОК. На первом этапе клинического обследования особое внимание было уделено изучению анамнеза пациенток, наличию отягощенного семейного тромботического анамнеза. Были собраны подробные сведения о приеме КОК: с какого возраста, с какой целью был назначен препарат, какой конкретно препарат был назначен, длительность приема препарата, при которой произошел тромбоз.
На базе кафедры акушерства и гинекологии Первого МГМУ им. И.М. Сеченова «Сеченовский Университет» проводилось подробное изучение системы гемостаза обследуемых пациенток. В первую очередь, проводились исследования на наличие генетических и приобретенных форм тромбофилии, а также на наличие полиморфизмов генов тромбофилической направленности. Исследование системы гемостаза включало: определение генетических форм тромбофилии методом полимеразной цепной реакции (полиморфизмы генов системы фибринолиза: ингибитор активатора плазминогена 1 (PAI-1) 675 4G/5G, фибриногена -455G/A, фактора XIII 163G/T; генетически обусловленные дефекты коагуляционного звена гемостаза: мутации F V Leiden, протромбина G20210A, протромбина Thr165Met, F VII А353G; полиморфизмы генов тромбоцитарных рецепторов: GpIa 807C/T, GpIIIa 1565T/C; мутации генов фолатного цикла: MTHFR C677T, MTHFR 1298 А/С (MTAC), MTRR, MTR; дефекты антикоагулянтного звена гемостаза: наследственный дефицит протеина C, протеина S, антитромбина III); полиморфизмы генов провоспалительных цитокинов: интерлейкин (IL)-6 174 G/C, IL-1β 31 T/C), определение уровня гомоцистеина (иммуноферментный метод с использованием реактивов Axis фирмы Axis-Shield AS, Норвегия на приборе ANТОS 2020), определение активированного частичного тромбопластинового времени, тромбинового времени, уровня фибриногена, тромбоэластографию (Hellige, Германия), определение агрегации тромбоцитов (Рауtоn, США), количества тромбоцитов, уровней D-димера (латекс-тест Dimertest, Agen, Австралия), комплексов тромбин-антитромбин, определение глобальной функции протеина С («Парус»-тест, прибор «START 4», Stago, Франция). Диагностика антифосфолипидного синдрома (АФС) включала: антифосфолипидные антитела (АФА) (иммуноферментный метод, Stago, Asserachrom APA), волчаночный антикоагулянт, кофакторы антифосфолипидных антител (антитела к бета-2 гликопротеину I, антитела к протромбину, антитела к аннексину V, антитела к кардиолипинам.
 Результаты
Результаты
В первую очередь, был проведен анализ препаратов гормональной контрацепции среди пациенток с ВТЭ. Большинство обследованных женщин принимали препараты, которые содержат дроспиренон в качестве гестагена и отличаются между собой дозой эстрогена и схемой приема препарата.
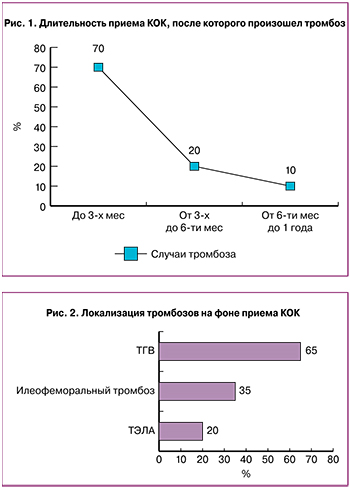
Анализ полученных данных показал, что у большинства пациенток (70%) случаи ВТЭ на фоне приема КОК были зарегистрированы в первые 3 месяца приема препарата, у 20% пациенток эпизод ВТЭ случился в период от 3-х мес до полугода приема КОК, у 10% пациенток — от полугода до года приема КОК (рис. 1).
Анализ локализации тромбозов у обследуемых пациенток показал, что на фоне приема КОК поражение сосудов, в основном, было локализовано в глубоких венах нижних конечностей — 65%, илеофеморальный тромбоз был диагностирован у 35% пациенток, тромбоэмболия легочной артерии (ТЭЛА) — у 20% (рис. 2).
 По данным анализа генетических и приобретенных форм тромбофилии у пациенток с ВТЭ на фоне приема КОК, было выявлено, что у 75% присутствовали те или иные формы тромбофилии. Из них у 32% пациенток была обнаружена генетическая тромбофилия, у 20% — мультигенная форма тромбофилии, у 15% — АФС. Комбинированные формы тромбофилии, включающие в себя сочетание приобретенной (АФС) и генетической/мультигенной форм, были обнаружены у 8% пациенток (рис. 3). У остальных 25% пациенток были обнаружены полиморфизмы генов системы гемостаза низкого тромботического риска. Интерес представляет тот факт, что у 80,5% из всех пациенток с генетической тромбофилией имел место отягощенный семейный тромботический анамнез, что свидетельствует о значимости подробного сбора семейного тромботического анамнеза перед назначением препаратов гормональных контрацептивов.
По данным анализа генетических и приобретенных форм тромбофилии у пациенток с ВТЭ на фоне приема КОК, было выявлено, что у 75% присутствовали те или иные формы тромбофилии. Из них у 32% пациенток была обнаружена генетическая тромбофилия, у 20% — мультигенная форма тромбофилии, у 15% — АФС. Комбинированные формы тромбофилии, включающие в себя сочетание приобретенной (АФС) и генетической/мультигенной форм, были обнаружены у 8% пациенток (рис. 3). У остальных 25% пациенток были обнаружены полиморфизмы генов системы гемостаза низкого тромботического риска. Интерес представляет тот факт, что у 80,5% из всех пациенток с генетической тромбофилией имел место отягощенный семейный тромботический анамнез, что свидетельствует о значимости подробного сбора семейного тромботического анамнеза перед назначением препаратов гормональных контрацептивов.
Анализ частоты встречаемости тех или иных мутаций и тромбофилических полиморфизмов в группе женщин с ВТЭ на фоне приема КОК выявил, что у 20% пациенток диагностирована мутация фактора V Leiden, мутация фактора II протромбина Thr165Met — у 5 %, АФС —у 15%. Почти у каждой второй женщины с полиморфизмами генов фолатного цикла, особенно при наличии сочетания этих полиморфизмов, был диагностирован повышенный уровень гомоцистеина в крови в той или иной степени (рис. 4)
Примечательным является еще и тот факт, что у женщин, у которых ВТЭ развились в течение первых месяцев приема КОК, значительно чаще выявляются наследственные нарушения системы гемостаза, чем у женщин с тромботическими осложнениями при более длительном приеме гормональных контрацептивов. При этом суммарная доза гормонов, которые получает женщина за этот период, составляет 1440 мкг этинилэстрадиола и 216 мг дроспиренона. У пациенток с развитием ВТЭ от 6 мес до 1 года были выявлены, преимущественно, полиморфизмы гемостаза низкой тромбофилической направленности и суммарная доза гормонов за полгода составила 2880 мкг этинилэстрадиола и 432 мг дроспиренона, за год — 5760 мкг этинилэстрадиола и 864 мг дроспиренона (таблица).

Обсуждение
Согласно уже известным данным о влиянии КОК на систему гемостаза, важно понимать действие этих препаратов на отдельные звенья системы гемостаза. Так, у женщин, принимающих КОК, наблюдается снижение чувствительности к активированному протеину С. Степень приобретенной резистентности к активированному протеину С схожа с таковой при наличии гетерозиготной формы мутации FV Leiden. Но, в отличие от генетически обусловленной резистентности, приобретенная резистентность к активированному протеину С не выявляется после отмены данной категории препаратов. Считается, что степень резистентности к активированному протеину С у женщин с гетерозиготной формой мутации FV Leiden, принимающих КОК, сходна с таковой при гомозиготной мутации FV Leiden. При наличии мутации FV Leiden, распространенность которой в популяции от 2 до 7%, риск ВТЭ у гетерозигот увеличен в 5—10 раз, у гомозигот – в 70—80 раз. При приеме КОК у женщин с гомозиготной формой мутации FV Leiden риск тромбозов увеличивается в 80—100 раз [3,10—12].
При приеме КОК также наблюдается повышение активности большинства прокоагулянтов крови, включая фибриноген, витамин-К зависимые факторы свертывания — протромбин, VII, IX, X, XII факторы. Степень увеличения содержания этих факторов напрямую зависит от дозы эстрогенов в препарате, а их изолированное увеличение свидетельствует о наличии гиперкоагуляции в отсутствии признаков активации внутрисосудистого свертывания крови и тромбоза. Тем не менее, судить о степени повышения уровня прокоагулянтов в крови можно только в соотношении с активностью противосвертывающих механизмов системы гемостаза [13, 14].
Кроме того, прием КОК влияет на функцию тромбоцитов, приводя к их гиперактивности, степень которой зависит от длительности приема препарата. В плазме крови повышаются маркеры тромбоцитарных реакций: β-тромбоглобулин, 4-антигепариновый фактор тромбоцитов, фактор 3 тромбоцитов и тромбоксан А2. В процессе приема КОК наблюдается умеренная активация тромбоцитов, не требующая дополнительной терапии, но увеличение срока приема данных препаратов более 9 мес приводит к прогрессированию агрегации тромбоцитов за счет инициации свертывания крови через тромбоцитарное звено. Как известно, тромбоцитарные реакции являются первым признаком активации системы гемостаза, а при наличии генетической или приобретенной форм тромбофилии у пациентки может исходно наблюдаться гиперагрегация тромбоцитов еще до начала приема КОК [3, 15, 16]. Так, например, по данным исследований, проведенных на кафедре акушерства и гинекологии медико-профилактического факультета Первого МГМУ им. И.М. Сеченова, было установлено, что при циркуляции АФА наблюдается стойкая гиперагрегация тромбоцитов. При наличии мутации генов тромбоцитарного звена системы гемостаза агрегация тромбоцитов также может быть изначально повышена; соответственно, бесконтрольное назначение КОК может привести к развитию тромботических осложнений. При назначении КОК следует исходно проверять агрегационную и функциональную активность тромбоцитов, а также в динамике при приеме препаратов с интервалами 2—3 мес. Если до начала приема КОК параметры агрегатограммы соответствуют нормативным значениям, то противопоказаний для назначения КОК со стороны тромбоцитарного звена системы свертывания крови нет. При развитии гиперагрегации тромбоцитов на фоне приема КОК показано назначение антиагрегантов на весь период контрацепции с обязательным динамическим наблюдением параметров агрегатограммы [13, 17].
О влиянии КОК на процесс фибринолиза свидетельствует стойкое повышение уровня PAI-1 и, соответственно, снижение концентрации тканевого активатора плазминогена и плазминогена. При исходно нормальной концентрации PAI-1 в крови, уже к 3-му месяцу приема КОК наблюдается увеличение его уровня в 2—3 раза, а к 9-му месяцу приема препарата регистрируются максимальные значения PAI-1. На изменения в системе фибринолиза на фоне приема КОК также указывают увеличение концентрации продуктов деградации фибрина — Д-димера и комплексов плазмин-антиплазмин. Таким образом, при наличии генетического дефекта системы фибринолиза (наличие полиморфизма PAI-1), когда имеет место изначальное увеличение уровня PAI-1 в крови до 25%, прием КОК значительно увеличивает риск развития тромботических осложнений [3, 14].
При длительном приеме КОК наблюдается снижение концентрации естественных антикоагулянтов крови: протеина С, протеина S, антитромбина III). Было установлено, что к 3-му месяцу приема КОК их уровень существенно не меняется, но уже к 9-му наблюдается значительное снижение антикоагулянтных компонентов системы гемостаза [10, 13].
Таким образом, можно сделать вывод о том, что в случае приема КОК и наличия врожденных дефектов системы гемостаза, а особенно, при наличии комбинированных форм тромбофилии, происходит однонаправленное влияние на систему гемостаза. Именно поэтому КОК во многих ситуациях являются триггерным фактором развития тромботических осложнений при уже существующих нарушениях баланса про- и антикоагулянтных механизмов.
Тем не менее, выраженность изменений в системе гемостаза, вызванных КОК, напрямую зависит от концентрации эстрогенного и гестагенного компонента в препарате. Корреляция риска тромботических осложнений с концентрацией этинилэстрадиола в препарате была обнаружена сразу после выхода на рынок первых высокодозированных КОК. Впоследствии, в результате снижения дозы эстрогенов в 5 раз, риск тромбообразования уменьшился в 4 раза [18]. Далее, в течение многих лет по результатам многочисленных исследований, ученые спорили о влиянии различных гестагенных компонентов в составе КОК на систему гемостаза. Так, в нескольких крупных исследованиях была проведена оценка рисков тромбообразования на фоне приема КОК в зависимости от типа прогестагена [19—21].
С учетом данных литературы, мы провели сравнительную характеристику КОК с целью выявления наиболее опасных комбинаций по риску развития тромботических осложнений. В настоящее время представлено множество препаратов, различных по комбинациям дозы эстрогена, типа гестагена, а также схемы приема. Еще одну категорию составляют трехфазные препараты, которые были созданы для имитации секреции эстрогенов и гестагенов в нормальном менструальном цикле. Если у монофазных препаратов уровень гормонов в таблетках остается неизменным в течение одного цикла, то трехфазные препараты содержат три комбинации гормонов, которые меняются в течение менструального цикла. Поэтому при сравнении препаратов мы учитывали не только дозы гормонов, содержащихся в одной таблетке, но также схему приема каждого конкретного препарата и суммарную дозу гормонов, которую получает женщина в течение одного цикла приема.
По нашим данным, наибольшая концентрация эстрогенов поступает в организм женщины при приеме препаратов, содержащих ципротерон ацетат 2 мг/этинилэстрадиол 35 мкг и норгестимат/этинилэстрадиол 35 мкг, а также трехфазных препаратов с левоноргестрелом /этинилэстрадиолом в различных комбинациях. Что касается дозы гестагенного компонента, наиболее высокие суммарные дозы имеют препараты, содержащие дроспиренон/этинилэстрадиол 30 мкг (этинилэстрадиол — 630 мкг, дроспиренон — 63 мг), дроспиренон/этинилэстрадиол 20 мкг (этинилэстрадиол — 480 мкг, дроспиренон — 72 мг), номегэстрола ацетат/ этинилэстрадиол 15 мкг и норгестимат/ этинилэстрадиол 35 мкг.
Заключение
Не вызывает сомнений высокое значение гормональной контрацепции, как метода планирования семьи, так и метода терапии многих гинекологический заболеваний. Но при наличии генетической или приобретенной форм тромбофилии, не выявленной заранее, прием гормональных контрацептивов может повлечь за собой серьезные осложнения. В нашем исследовании в 2/3 случаев при приеме КОК ретроспективно была выявлена скрытая тромбофилия, в 80 % из этих случаев был обнаружен отягощенный семейный тромботический анамнез. Поэтому исследование системы гемостаза перед назначением КОК позволяет своевременно идентифицировать женщин группы высокого риска тромботических осложнений и предотвратить их появление; также исследование системы гемостаза является абсолютно необходимым при наличии отягощенного семейного тромботического анамнеза.
Также, можно сделать вывод о том, что большинство генетических мутаций и полиморфизмов генов системы гемостаза могут не проявлять себя самостоятельно в течение всей жизни. Зачастую, именно сочетание нескольких видов мутаций или дополнительные факторы риска тромботических осложнений (прием КОК, беременность, оперативные вмешательства, травма, длительная иммобилизация, курение, инфекционные и онкологические заболевания и т.д.) могут спровоцировать манифестацию того или иного дефекта гена свертывающей системы крови. Поэтому при назначении КОК пациентка должна быть проинформирована о побочных эффектах и рисках, связанных с приемом данных препаратов. Также следует отдать предпочтение препаратам, оказывающим наименьшее влияние на систему гемостаза и проводить постоянный контроль параметров системы гемостаза, как перед назначением КОК, так и в процессе их приема.



