Эндометриоз определяется наличием эктопической ткани, подобной эндометрию, вне полости матки [1]. Клиническая картина эндометриоза гетерогенна и в ряде случаев зависит от фенотипа болезни (поверхностный эндометриоз, глубокий инфильтративный эндометриоз (ГИЭ) и эндометриоидные кисты (ЭК) яичников) [2]. Типичные клинические проявления болезни – это боль и бесплодие. Заболевание поражает 1 из 10 женщин репродуктивного возраста; однако истинная распространенность не известна, так как примерно в 25–50% случаев эндометриоз протекает бессимптомно [3]. Лапароскопия с гистологическим подтверждением наличия эктопической ткани эндометрия является «золотым стандартом» диагностики эндометриоза. К первой линии диагностики заболевания относят ультразвуковое исследование (УЗИ), в связи с его доступностью, высокой чувствительностью и специфичностью при ЭК яичников [4, 5]. Однако имеется ряд ограничений, которые коррелируют с опытом специалиста визуальной диагностики, качеством получаемых изображений на аппарате и локализацией процесса. Более точным методом визуализации при начальных и/или глубоких формах эндометриоза является магнитно-резонансная томография (МРТ) [6].
Гипотезы происхождения эндометриоза основаны на различных генетических, эпигенетических, гормональных, иммунологических, воспалительных, ангиогенных и лимфогенных изменениях, участвующих в патогенезе, но ни одна теория в отдельности не может объяснить этиологию болезни [7–9]. Фокус исследований последних лет направлен на изменение профиля кишечной микробиоты при эндометриозе и влияние продуктов микробного метаболизма на прогрессирование заболевания [10, 11]. Предполагается также вовлеченность других инфекционных агентов – вирусов, поскольку некоторые из них выявляются в нижних отделах репродуктивного тракта, например, вирус папилломы человека (ВПЧ), который может передаваться, в том числе, и половым путем [12]. В нескольких исследованиях была показана корреляция между наличием в организме ВПЧ высокого канцерогенного риска с различными фенотипами эндометриоза [13–15].
В настоящее время научное общество сконцентрировано на поиске неинвазивных маркеров (биохимических, фенотипических, анамнестических и инструментальных), которые могли бы сократить время постановки диагноза; ведь по различным данным оно может достигать 10 лет. Все больший интерес вызывают коморбидные состояния, которые предполагается рассматривать, как факторы риска наличия эндометриоза. В литературе наиболее часто упоминаемыми коморбидными заболеваниями являются мигрень и синдром раздраженного кишечника (СРК) [16]. Представлены также немногочисленные данные о проявлениях клинической гиперандрогении, а именно акне, у пациенток с эндометриозом. Так, в крупном проспективном исследовании Xie J. et al. (2014) было показано, что у женщин с подростковыми акне в анамнезе риск развития эндометриоза повышался на 20% (отношение рисков 1,20, 95% доверительный интервал 1,08–1,32) [17]. Попытки объяснения данной взаимосвязи были проведены также в работе Zhang M. et al., где описаны молекулярно-генетические и иммунологические теории ассоциаций [18]. Кроме того, экспосом (в том числе характер питания) может влиять на прогрессирование заболевания.
Как известно, эндометриоз является эстрогензависимым заболеванием. Широко обсуждается связь диеты с возникновением эстрогензависимых заболеваний, например рака эндометрия и рака молочной железы. Фактическое питание и генетически детерминированная особенность метаболизма питательных веществ могут играть роль в этиологии данных заболеваний [19]. В работе Huang M. et al. (2018) показано, что нутритивный статус может оказывать воздействие на активность и уровень половых гормонов [20]. Кроме того, некоторые нутриенты, а именно полиненасыщенные жирные кислоты (ПНЖК), обладают противовоспалительным действием [21–23]. Интересные исследования были проведены на мышах с индуцированным эндометриозом, где обнаружено, что метаболиты, полученные из ПНЖК, а именно эйкозапентаеновой кислоты (ЭПК), ингибируют рост эндометриоидных очагов [24].
Задержка в постановке диагноза может приводить к прогрессированию заболевания и повышает вероятность оперативного вмешательства, что влечет за собой интраоперационные риски, которые коррелируют со степенью распространенности эндометриоза. В литературе практически не описана динамика роста эндометриоидных очагов, так как «путь» пациента от появления первичных симптомов до постановки диагноза и подбора терапии достаточно сложный и долгий. Мы представляем клиническое наблюдение прогрессирования ретроцервикального (РЦ) эндометриоза в сочетании с ЭК яичников у пациентки 26 лет.
Клиническое наблюдение
Пациентка А., 24 года, впервые обратилась в отделение гинекологической эндокринологии в 2020 г. с жалобами на обильные и болезненные менструации с менархе (по визуальной аналоговой шкале (ВАШ) – 4 балла); задержки менструаций до 60 дней с менархе; боли в области прямой кишки, вздутие живота и периодические боли в животе; акне на коже лица с подросткового возраста.
Из анамнеза: акне вульгарные, СРК. В связи с акне и олигоменореей пациентка длительное время принимала различные виды комбинированных оральных контрацептивов. Со слов пациентки, причина олигоменореи не была установлена, однако предварительно был выставлен диагноз «синдром поликистозных яичников» (учитывая олигоменорею и клиническую гиперандрогению), было назначено дообследование. В связи с дисменореей назначались нестероидные противовоспалительные препараты с положительным эффектом. Боли в области прямой кишки начались с 2018 г. (с 22 лет), а периодические боли в животе беспокоили в течение последнего года, в связи с чем наблюдалась у гастроэнтеролога с предварительным диагнозом СРК, проводилась симптоматическая терапия. На момент первичного обращения вопрос реализации репродуктивной функции не стоял. Наследственность не отягощена, аллергии нет. Индекс массы тела – 18 кг/м2.
При гинекологическом осмотре: в зеркалах патологические образования не выявлены; при бимануальном исследовании отмечалась болезненность при тракции за шейку матки. По данным онкоцитологии шейки матки определено плоскоклеточное интраэпителиальное поражение низкой степени LSIL (low-grade squamous intraepithelial lesion). Выявлен ВПЧ 53 типа. Пациентке было выполнено кольпоскопическое исследование и обнаружены слабовыраженные изменения – тонкий ацетобелый эпителий, йод-негативная зона на 12 ч условного циферблата.
По данным УЗИ органов малого таза от 09.2020 г.: М-Эхо – 0,8 см, в средней трети полости матки, по переднему листку полиповидное образование размерами 0,7×0,4 см. В левом яичнике (V=9 см3) две ЭК размерами 16 мм и 10 мм.
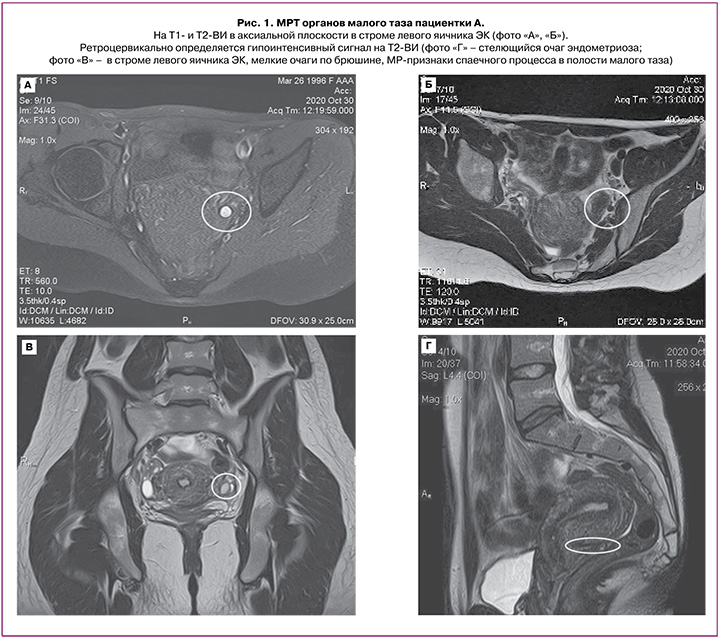
МРТ органов малого таза было выполнено в октябре 2020 г. специалистом экспертного уровня; был определен РЦ-очаг (1,7×0,8×0,6 см) эндометриоза (рис. 1Г) с преимущественным распространением в левые отделы, фиксацией левого яичника, ЭК левого яичника (1,2×0,5×0,9 см) (рис. 1А, В), МР-признаки эндометриоидных гетеротопий по брюшине таза, крестцово-маточных связок (КМС) на фоне спаечного процесса. МР-картина начальных признаков аденомиоза.
Пациентка на повторный прием не явилась, рекомендации по дообследованию не прошла. В течение 2 лет не наблюдалась, медикаментозное и хирургическое лечение не получала. Обратилась через 2 года в августе 2022 г. с жалобами на обильные и болезненные менструации (по ВАШ 7 баллов), резкие боли в области прямой кишки, усиливающиеся в сидячем положении, боли при половом контакте. Консультирована проктологом: патология со стороны прямой кишки и ануса исключена. Пациентка планирует реализовать свою репродуктивную функцию.
Был проведен гинекологический осмотр: при бимануальном осмотре обращает внимание выраженная болезненность при тракции за шейку матки. Тело матки нормальных размеров, неподвижно, безболезненно, плотное. Своды влагалища при пальпации резко болезненны, укорочены. В области левых придатков пальпируется округлое образование размерами 3,0×4,0 см тугоэластичной консистенции, чувствительное при пальпации.
Были взяты контрольные мазки, по результатам: LSIL, ВПЧ 51 и 53 типов. Выполнена кольпоскопия, по результатам: слабовыраженные изменения, тонкий ацетобелый эпителий, нежная пунктация, нежная мозаика на 12 ч условного циферблата. Была проведена прицельная биопсия шейки матки. По результатам гистологического исследования: Койлоцитоз. LSIL. Были даны рекомендации по дальнейшему скринингу, а также было рекомендовано дообследование для подбора терапии эндометриоза.
Пациентка обратилась с результатами исследований лишь в октябре 2022 г. По данным УЗИ выявлен рост ЭК яичников и РЦ очага.
При МРТ органов малого таза с контрастированием (02.09.2022 г.) отмечается массивный РЦ очаг (2,8×1,2×3,1 см) (рис. 2) эндометриоза с преимущественным распространением в левые отделы, вовлечением левого яичника и стенки прямой кишки, без признаков глубокого прорастания, ЭК левого яичника (4,1×3,9×3,4 см; 2,3×1,0×1,4 см; 0,8×0,5 см), МР-признаки эндометриоидных гетеротопий по брюшине таза и КМС на фоне спаечного процесса. МР-признаки аденомиоза.
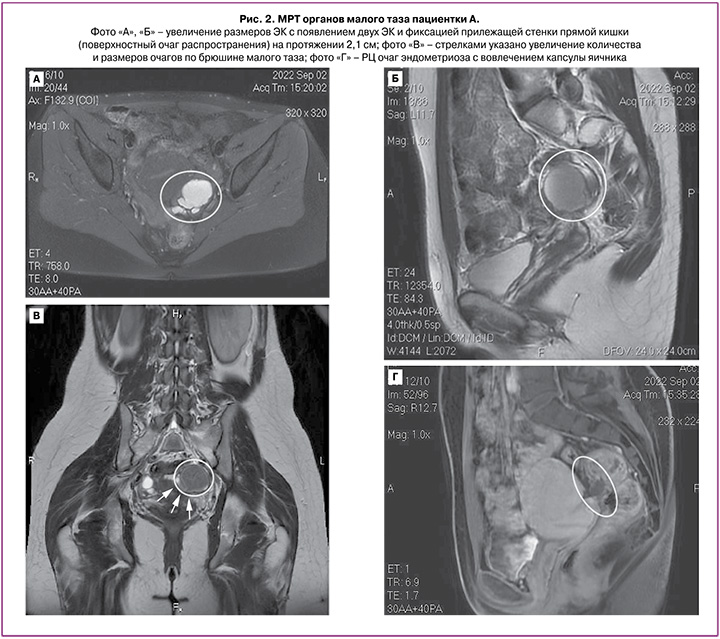
Таким образом, РЦ очаг эндометриоза почти за 2 года увеличился более чем на 90% от исходного значения (исходно – 1,7×0,8×0,6 см; через 2 года – 2,8×1,2×3,1 см). Увеличились размеры ЭК левого яичника до 4,1×3,9×3,4 см (ранее – 1,2×0,5×0,9 см) с появлением двух ЭК (размерами 2,3×1,0×1,4 см; 0,8×0,5 см), с фиксацией прилежащей стенки прямой кишки (поверхностный очаг распространения) на протяжении 2,1 см; также увеличились количество и размеры очагов по брюшине малого таза.
Пациентке была проведена колоноскопия и обнаружены единичные дивертикулы сигмовидной кишки. Данных за врастание и новообразование не было.
Онкомаркеры: СА 19-9 – 80 ЕД/мл, СА-125 – 60 ЕД/мл, НЕ-4 – 35,7 пмоль/л, индекс RОМА1 – 3,79%.
Пациентке также была проведена оценка пищевого статуса путем частотного анализа при помощи компьютерной программы, зарегистрированной ГУ «НИИ питания» РАМН, 2003–2006, версия 1.2.4.
Рост – 180 см, вес – 73 кг, индекс массы тела – 21 кг/м2 (соответствует нормальным показателям массы тела), объем талии – 73 см, объем бедер – 106 см.
При анализе питания выявлены следующие особенности. Калорийность рациона соответствовала возрасту и физическим нагрузкам пациентки и составила 2300 ккал, содержание основных компонентов в суточном рационе: белки – 47 г (норма – 60–90 г), жиры – 87 г (норма – 57–100 г), углеводы – 181 г (норма – 238–435 г). Выявлено нарушение оптимального соотношения основных пищевых составляющих (1:1:4). Снижение доли углеводов связано с низким потреблением овощей и фруктов, что привело к выраженному дефициту пищевых волокон – 9,9 г в рационе (норма – 20–25 г/сут); также выявлено недостаточное поступление витаминов С, В1, В2, ниацина и магния. Отмечается дефицит ПНЖК класса омега-3 у пациентки – 1,85 г/сут, что составляет 0,7% от общей калорийности (норма – 1–2%) и объясняется полным отсутствием рыбы в меню.
Принимая во внимание стремительный рост ЭК, РЦ очага, выраженный болевой синдром, а также заинтересованность пациентки в реализации репродуктивной функции, было рекомендовано оперативное лечение. Однако в связи с низкой комплаентностью пациентки лишь в апреле 2023 г. она обратилась для хирургического лечения. Ей было проведено оперативное вмешательство в объеме: гистероскопия, лапароскопия, хромогидротубация, коагуляция и иссечение очагов эндометриоза, шейвинг ректосигмоидного отдела толстой кишки, резекция левого яичника. По результатам лапароскопии и гистологического заключения подтвержден наружный генитальный эндометриоз, ЭК левого яичника.
После проведенной операции, учитывая заинтересованность в беременности, оценив статус фертильности (маточные трубы проходимы, антимюллеров гормон – 2,1 нг/мл и фертильная спермограмма партнера), данной пациентке была рекомендована противорецидивная терапия агонистами гонадотропин-рилизинг-гормона (аГнРГ) в течение 3 месяцев до планирования беременности, однако дан ограниченный период времени на планирование.
Обсуждение
Данный клинический пример иллюстрирует динамику роста очагов эндометриоза в течение 2 лет. Благодаря своевременной комплексной и детальной диагностике на момент первичного обращения, принимая во внимание размеры эндометриоидных образований, отсутствие вовлечения смежных органов и нормальный уровень онкомаркеров, была возможность ограничиться консервативными методами лечения. Однако крайне низкая приверженность пациентки и отсутствие своевременно начатой терапии привели к скорому прогрессированию заболевания. При положительном эффекте супрессивной терапии, в том числе относительно купирования болевого синдрома, она могла стать долгосрочной перспективой до планирования беременности. Однако спустя два года мы наблюдаем прогрессирование эндометриоза до размеров, при которых уже возможности гормональной терапии ограничены, и по результатам обследования пациентка направлена на оперативное лечение. При отсутствии репродуктивных планов после операции обсуждались бы варианты длительного противорецидивного лечения в сочетании с модификацией диеты. Арсенал препаратов включает аГнРГ, комбинированные гормональные контрацептивы, прогестагены. Диагностические и терапевтические подходы должны быть адаптированы индивидуально к каждой пациентке, ее симптомам и репродуктивным планам.
Симптомы эндометриоза неспецифичны, а результаты методов визуализации во многом зависят от опыта специалиста. Задержка в постановке диагноза, прогрессирование болезни и нередко возникающая хроническая тазовая боль вследствие развития центральной сенситизации требуют более сложной дифференциальной диагностики и междисциплинарного подхода [16, 25]. Это может приводить к различным физическим, а также психологическим и социальным негативным последствиям для пациентов. Поэтому крайне важно своевременно реагировать на «ранние признаки» заболевания, включая коморбидные заболевания; а для этого необходимо детально изучать жалобы и историю заболевания пациента, факторы риска, соматический и наследственный анамнез.
Факторы риска эндометриоза известны: раннее менархе, менструальный цикл менее 28 дней, отягощенный семейный анамнез по эндометриозу, низкий паритет, бесплодие, европеоидная раса, ежедневное употребление большого количества алкоголя, чрезмерное потребление красного мяса и курение [26, 27]. Широко обсуждается коморбидность или полиморбидность эндометриоза не только с мигренью и СРК, но и с аутоиммунными заболеваниями, акне, синдромом болезненного мочевого пузыря [28–30]. Инфекции также могут влиять опосредованно, за счет нарушения модуляции иммунных реакций и усиления воспалительной активности из-за изменения микробиоты кишечника и ее метаболитов. При инфекционном процессе усиливается окислительный стресс, который является одним из эпигенетических факторов возникновения и прогрессирования эндометриоза [30, 31]. Учитывая данные литературы о возможной взаимосвязи акне у подростков и риска эндометриоза, а также сочетания с различными сопутствующими заболеваниями, в дальнейшие исследования должна быть включена оценка факторов риска, коморбидных заболеваний, анамнеза пациента для расширения потенциала ранней диагностики.
Известно, что эктопическая ткань связана с гиперпродукцией простагландинов (ПГ), провоспалительных и противовоспалительных цитокинов, хемокинов, факторов роста и ангиогенеза, а определенные пищевые жирные кислоты оказывают влияние на уровни маркеров воспаления, например, интерлейкин-6, который обнаруживается в более высоких концентрациях у женщин с эндометриозом [32]. Применение диеты с высоким содержанием антиоксидантов снижает окислительный стресс и прогрессирование эндометриоза [33]. Считается, что определенные медиаторы воспаления, такие как лейкотриен (ЛТ) В4 и ПГ Е2, связаны с тазовой болью при эндометриозе [34]. Арахидоновая кислота является наиболее важным компонентом омега-6 ПНЖК, которая играет роль субстрата в производстве ЛТ В4 и ПГ Е2. И наоборот, ЭПК, важный компонент омега-3 ПНЖК, играет значимую роль в биосинтезе ЛТ В5 и ПГ E3, которые оказывают противовоспалительное действие, по сравнению с ПГ Е2 и ЛТ В4 [35]. Анализ взаимосвязи питания и дисменореи показал, что увеличение потребления рыбьего жира, содержащего большое количество омега-3 ПНЖК, приводит к снижению интенсивности болей [36]. В крупном проспективном исследовании с участием более 70 000 женщин было показано, что повышенное потребление омега-3 ПНЖК может снижать риски развития эндометриоза [37]. Интересные данные о роли питательных веществ и антиоксидантов при эндометриозе были описаны в обзоре 2023 г., где авторы пришли к выводу, что диетические факторы могут влиять на патофизиологические механизмы эндометриоза, в том числе и на воспаление [38].
В описанном случае у пациентки обнаружены нарушения в нутритивном статусе, которые были выявлены при оценке питания, а также имели место акне с менархе и СРК, по поводу которого она длительное время наблюдалась у гастроэнтеролога, ВПЧ высокого онкогенного типа. Все перечисленные факторы, по немногочисленным данным литературы, можно использовать как потенциальные критерии для отбора пациентов повышенной группы риска по развитию заболевания для дальнейшего обследования и наблюдения. Достижения в области визуальной диагностики, в частности МРТ, позволяют более точно оценить локализацию очагов эндометриоза и степень инвазии в прилегающие органы (наиболее часто кишечник, мочевой пузырь и мочеточники) для последующего выбора оптимальной тактики введения пациенток, в частности возможности проведения консервативной терапии. Примерно у 20% женщин развивается фенотип ГИЭ или ЭК яичников [39]. При наличии эндометриом яичников ГИЭ выявляется в 45% случаев; в литературе имеются данные, когда ЭК яичников могут быть предикторами наличия глубоких форм эндометриоза [40–42].
Заключение
Отбор пациенток для долговременной консервативной терапии в настоящее время является одной из основных задач в ведении пациенток с эндометриозом, принимая во внимание хроническое течение заболевания. Возможность диагностики и терапии на ранних стадиях эндометриоза способствовала бы более высокому качеству жизни пациенток и контролю прогрессирования заболевания. С одной стороны, необходима гистологическая верификация эндометриоза, с другой, – всегда необходимо учитывать интраоперационные риски и риски ятрогенной преждевременной недостаточности яичников, особенно при повторных оперативных вмешательствах. Возможности МРТ в диагностике эндометриоза позволяют своевременно определить пациенток в группу консервативного ведения. Все это указывает на необходимость в совершенствовании подходов к ранней диагностике заболевания и, соответственно, своевременному старту терапии, что, возможно, в будущем позволит избежать многократных вмешательств по поводу эндометриоза и всех негативных последствий эндометриоза, которые мы наблюдаем в настоящее время.



