Вслед за респираторными инфекциями инфекции мочевых путей (ИМП) являются наиболее частыми бактериальными инфекциями, и около 20–30% женщин с ИМП имеют рецидивы инфекции. Рецидивирующая ИМП определяется как по крайней мере 3 эпизода ИМП в течение года или 2 обострения за 6 месяцев [1].
Как правило, острый неосложненный бактериальный цистит поддается антибактериальной терапии в амбулаторных условиях [2, 3]. Индивидуальный риск заражения зависит от различных факторов, включая возраст, сексуальную активность, семейный анамнез, сопутствующие заболевания и индивидуальный анамнез инфекций нижних мочевых путей (ИНМП).
Рецидивирующие ИНМП в значительной степени влияют на частоту и заболеваемость мочевой инфекцией, поскольку более 30% женщин страдают от последующей инфекции в течение 12 месяцев после исчезновения начальных симптомов, несмотря на соответствующую антибактериальную терапию. Антибиотики эффективны в низкодозовой антимикробной профилактике рецидивов [4], но ведут к увеличению антимикробной резистентности [5].
ИМП становится все труднее лечить из-за быстрого распространения антибактериальной устойчивости среди грамотрицательных организмов [6]. Рекомендации по эмпирическому лечению основываются на результатах региональных исследований возбудителей неосложненных ИМП и определения уровня их устойчивости к антимикробным препаратам.
Предпочтение в терапии ИМП отдается антимикробным препаратам, которые сочетают низкий уровень устойчивости к преобладающему возбудителю острого неосложненного цистита – уропатогенной кишечной палочке (UPEC) и низкий уровень нежелательных побочных действий препарата. Согласно последним международным и российским рекомендациям, фосфомицина трометамол и нитрофураны являются препаратами первого выбора при лечении острого неосложненного цистита [7].
При ИНМП у женщин необходимо учитывать состояние влагалищного биоценоза и микрофлоры кишечника. Известно, что в 60% случаев рецидивы бактериального цистита вызываются тем же уропатогеном, что и первый эпизод ИНМП [8, 9].
Этот феномен можно объяснить формированием внутриклеточных бактериальных сообществ внутри клеток поверхностного слоя слизистой оболочки мочевого пузыря, однако нельзя исключить и формирование очагов персистирующей инфекции внутри слизистой оболочки влагалища и/или кишечника, которые способны привести к ратифицированию мочевых путей у женщин.
С этой точки зрения большой интерес вызывает антимикробный препарат нифурател, имеющий многолетний опыт применения в урологии и гинекологии.
Нифурател является одним из производных 5-нитрофурана, которые, как известно, ингибируют различные грамположительные и грамотрицательные микроорганизмы. Спектр действия нифуратела включает основных возбудителей острых урогенитальных инфекций: штаммы UPEC, Enterococci, Staphylococci. Нифурател также обладает активностью против Candida и Trichomonas vaginalis и отдельных вагинальных инфекций [10–16]. Механизм антибактериального действия предполагает подавление ферментативных процессов, необходимых для роста бактерий. Бактерии развивают лишь ограниченную резистентность, и перекрестной устойчивости между нифурателом и сульфониламидами или другими антибиотиками не возникает [15]. Особенностью нифуратела является создание высокой концентрации активного метаболита в моче, которая, в отличие от нитрофурантоина, не зависит от pH мочи. Максимальная концентрация в моче составляет 30–50 мг/л, в сыворотке крови – 1,0–2,5 мг/л, в эпителии мочевыводящих путей – 0,8–3,6 мг/л [15].
Целью данного обзора является изучение клинико-бактериологической эффективности нифуратела при терапии ИМП.
Материалы и методы
Данный систематический обзор включает опубликованные исследования за период 1969–2020 гг., которые оценивали эффективность применения нифуратела при ИНМП у женщин, включая беременных. Наш систематический обзор был проведен согласно чек-листу PRISMA [17]. PRISMA – это основанный на фактах минимальный набор элементов отчетности для написания систематических обзоров и метаанализов (рис. 1). PRISMA фокусируется на составлении отчетов об обзорах, оценивающих рандомизированные исследования, но также может использоваться в качестве основы для составления отчетов о систематических обзорах других типов исследований, в частности, оценок вмешательств.

В анализ были включены рандомизированные и нерандомизированные оригинальные клинические исследования (проспективные контролируемые, проспективные когортные, ретроспективные исследования и т.д.) и исследования «серия случаев», которые включали минимум 10 пациентов. Рассматривались публикации только на английском и русском языках.
Для электронного поиска использовались следующие базы данных: PubMed, MEDLINE, Cochrane Library, а также КиберЛенинка и Google Академия. Ключевые слова: (nifuratel) AND (urinary tract infection), MeSH – медицинские предметные рубрики: ("Nifuratel"[Mesh]) AND "Urinary Tract Infections"[Mesh] и «нифурател», «инфекции мочевыводящих путей».
Два исследователя независимо друг от друга провели электронный поиск публикаций. Далее подходящие исследования по названию и абстракту были оценены по полному тексту публикации. Списки литературы исследований, которые подошли для скрининга полного текста, были просмотрены для поиска дополнительной литературы. Скрининг полнотекстовых публикаций был проведен независимо двумя исследователями для включения публикаций в качественный анализ (систематический обзор). После полноценного скрининга авторами были исключены дубликаты. Любые разногласия по включению или исключению предварительно отобранных исследований для качественного синтеза или любые другие разногласия в процессе обзора были устранены путем консенсуса после совместного обсуждения. Данные из включенных исследований были независимо собраны двумя авторами с помощью стандартной процедуры извлечения данных (авторы, год публикации, дизайн исследования, характеристики пациентов, вмешательство и исходы). Основной анализ данного систематического обзора оценивал эффективность применения нифуратела как действующего вещества для антибиотикотерапии у пациентов с ИМП.
Критериями включения для данного систематического обзора были: 1) подтвержденный диагноз – инфекция мочевыводящих путей, 2) возраст старше 18 лет. Статьи, включающие пациентов без симптомов ИНМП, а также статьи, в которых наблюдалась статистически значимая разница между средним возрастом пациентов в исследуемых группах, были исключены.
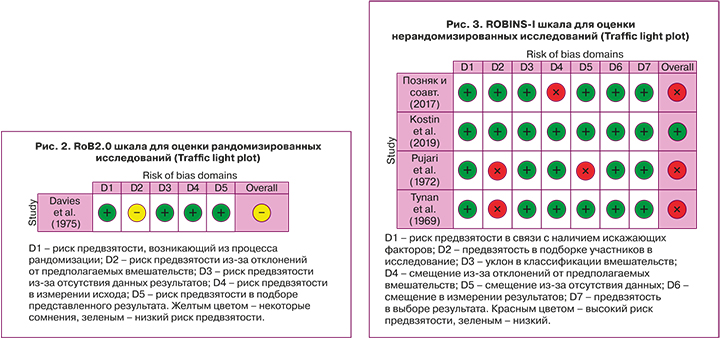
Оценка предвзятости включенных исследований проводилась при помощи The Cochrane Handbook for Systematic Reviews of Interventions [18]. Два исследователя проводили оценку предвзятости независимо друг от друга согласно шкалам, рекомендованным обществом Cochrane. Разногласия в процессе оценки предвзятости были устранены путем консенсуса или с привлечением третьего автора. Согласно справочнику Cochrane для написания систематических обзоров, шкала RoB2 [19] использовалась для оценки риска систематической ошибки в рандомизированных контролируемых исследованиях и ROBINS-I [20] – в нерандомизированных исследованиях (проспективных контролируемых, проспективных когортных или ретроспективных исследованиях и др.). Также исследования дизайна «серия случаев» были оценены по шкале для оценки риска предвзятости исследований «серия случаев» согласно NIH (National heart, lung and blood institute) [21].
Результаты
После электронного поиска в базах данных было найдено 106 исследований, которые были подвергнуты независимому скринингу по названиям и абстрактам. Также 95 исследований были найдены в списках литературы приемлемых по названию и абстракту исследований. После полноценного поиска и исключения дубликатов 192 публикации вошли в скрининг, из которых 169 были исключены по названию и абстракту. 23 исследования были оценены в полнотекстовом формате для систематического обзора (рис. 1). После прочтения полнотекстовых статей 14 из них были исключены: 6 – обзор литературы, 2 – рассматривались пациенты до 18 лет, 2 – серия клинических случаев, 4 – не рассматривались ИМП. 9 исследований были использованы для качественного анализа: 1 рандомизированное исследование [22], 4 когортных нерандомизированных исследования [10–13], 2 исследования «серия случаев» [3, 14] и 2 исследования, которые рассматривали эффективность нифуратела in vitro [15, 16].
В 7 клинических исследованиях оценивалась эффективность приема нифуратела у 442 пациентов (табл. 1).
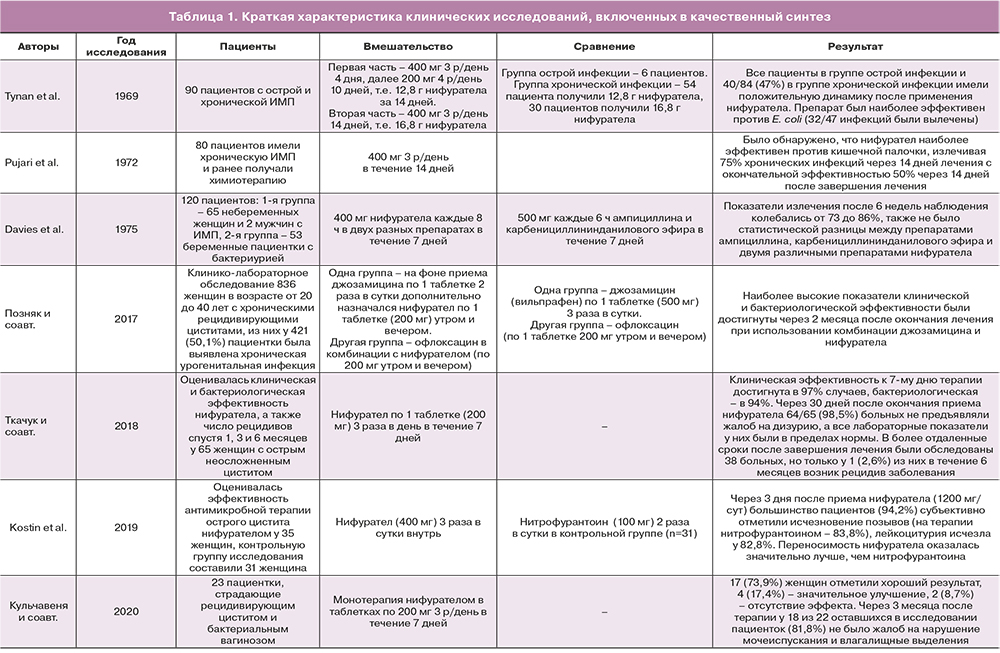
В исследовании Tynan et al. (1969) [11] образцы мочи исследовали как до, так и в конце 14-дневного курса лечения и через 14 дней после его завершения. 57 пациентам давали ударную дозу 400 мг (2 таблетки) 3 раза в день в течение 4 дней, далее дозу уменьшали до 200 мг (1 таблетка) 4 раза в день в течение 10 дней, всего 12,8 г нифуратела. Во 2-й группе 33 пациентам была назначена ударная доза 400 мг трижды в день в течение 14 дней, то есть всего 16,8 г нифуратела. В исследовании приняли участие 90 пациентов. У 6 была острая ИМП, а у 84 инфекция носила хронический характер. У всех пациентов с острой инфекцией и у 40/84 (47%) с хронической инфекцией лечение нифурателом было эффективным. Наиболее эффективен препарат против кишечной палочки (вылечено 32 из 47 случаев инфекции). Побочные эффекты были минимальными.
В работе Pujari et al. (1972) [13] исследовали среднюю порцию мочи, за исключением случаев, когда образец был взят из постоянного катетера или во время цистоскопии. Анализы мочи забирали до, на 14-й день лечения и через 14 дней после завершения курса. 80 пациентов получали 400 мг 3 раза в день в течение 14 дней, таким образом, общая доза составляет 16,8 г нифуратела. Все пациенты имели хроническую ИМП с какой-либо основной причиной и ранее получали химиотерапию. Отсутствие бактериурии на 14-й день после окончания 14-дневного курса лечения считали за излечение. После 14 дней лечения у 60/80 (75%) пациентов моча была стерильной, но у 25 возник рецидив через 14 дней, так что через 28 дней только 35 пациентов (44%) были вылечены. Сделан вывод о том, что нифурател подавляет грамотрицательные и грамположительные микроорганизмы и обладает хорошим терапевтическим действием против Candida spp. и Trichomonas vag. Было обнаружено, что нифурател наиболее эффективен против кишечной палочки (75%) через 14 дней лечения с окончательной эффективностью 50%. Он также эффективен против клебсиелл и фекального энтерококка и в меньшей степени – против протейной инфекции. Побочные эффекты при этом минимальны.
Davies et al. [22] провели рандомизированное исследование в 1975 г.: 120 пациентов были разделены на 2 отдельные группы, первая из которых состояла из 65 небеременных женщин и 2 мужчин с ИМП, вторую группу составили 53 пациента, направленных из дородового скрининга с бактериурией при беременности. Пациентам назначали 7-дневный курс терапии: по 500 мг каждые 6 ч для ампициллина и карбенициллина и 400 мг каждые 8 ч для двух препаратов нифуратела. 4 проведенных схемы лечения были распределены в соответствии со списком случайных чисел лицом, не имевшим отношения к исследованию, и тем пациентам, которые не прошли лечение, давали 1 из 3 оставшихся соединений. Таким образом, 67 небеременных пациенток получили 91 курс лечения, а 53 женщины с бактериурией во время беременности прошли 72 курса лечения. Единственным критерием излечения было устранение исходного возбудителя инфекции из мочи через 2 и 6 недель после начала лечения. Критерием включения в исследование служили 2 последовательных образца мочи, содержащих более 10 на 1 мл одних и тех же бактерий при чистом росте, использовали антисыворотки для определения серотипа каждого изолята Escherichia coli. Результаты как основного, так и полного курса лечения не показали статистически значимых различий между 4 лекарственными препаратами, хотя нифурател оказался незначительно лучше. Таким образом, в общей сложности 120 пациентов, включая 53 беременных со значительной бактериурией, прошли 163 семидневных курса пероральных антимикробных препаратов, распределенных рандомизированным образом. Показатели излечения после 6 недель наблюдения колебались от 73 до 86%, также не было статистической разницы между препаратами ампициллина, карбенициллина и двумя различными препаратами нифуратела. Побочные эффекты наблюдались в 30–40% случаев при использовании пенициллиновых препаратов, но менее чем в 15% при назначении нифуратела. Сделан вывод, что нифурател является высокоактивным нетоксичным лекарством, эффективным при лечении ИМП.
Следующее большое исследование [12] 836 пациенток было проведено в период с 2000 по 2017 гг.; возраст женщин от 20 до 40 лет, с рецидивирующим циститом. Перед началом терапии осуществляли забор материала из влагалища, цервикального канала, уретры и анализы мочи. Наиболее значимыми были микст-хламидийные ассоциации: Ch. trachomatis, B. fragilis и E. coli (29,5%). С целью разработки наиболее эффективных схем эмпирического лечения больных с хроническими циститами микст-хламидийной этиологии были сформированы четыре однородные по возрасту группы пациенток. В 1-ю (n=12) и 2-ю (n=16) группы включили женщин одного возраста (34,4±3,9 года), имеющих одинаковую этиологию заболевания (Ch. trachomatis+B. fragilis). Эмпирическую этиотропную терапию (без учета чувствительности выявленных возбудителей к этиотропным препаратам) проводили непрерывно в течение 18 суток. Пациентки 1-й группы получали вильпрафен по 1 таблетке (500 мг) 3 раза в сутки, а больным 2-й группы на фоне приема джозамицина по 1 таблетке 2 раза в сутки дополнительно назначался нифурател по 1 таблетке (200 мг) утром и вечером. Группы 3-я (n=15) и 4-я (n=13) были сформированы по аналогичному признаку, однако у них диагностировалась другая этиология заболевания (Ch. trachomatis+B. fragilis+Gardnerella). Эмпирическая терапия больных 3-й группы проводилась офлоксацином (по 1 таблетке 200 мг утром и вечером), а пациенток 4-й группы – офлоксацином в комбинации с нифурателом (по 200 мг утром и вечером) в течение аналогичного срока (18 суток). В результате обнаружена значительная эффективность нифуратела в комплексном лечении женщин с хроническим рецидивирующим циститом, наибольшая результативность была определена через 2 месяца после завершения терапии при назначении джозамицина и нифуратела в комбинации.
В 2018 г. было проведено еще одно исследование [3], где 65 пациенткам с острым неосложненным циститом назначили семидневную терапию нифурателом по 200 мг 3 раза в день. Возраст больных составил от 20 до 43 лет. Динамическое обследование проводили до терапии, через 7 и 30 дней после ее окончания и через полгода после завершения терапии у 38 больных. К 7-му дню терапии была достигнута клиническая эффективность в 97% случаев, бактериологическая – в 94%. Трем больным с неэффективностью терапии продолжили лечение еще на 7 дней. У 64 пациентов после 30 дней окончания терапии нифурателом жалоб не было, их лабораторные данные соответствовали норме. Только у 1/38 (2,6%) больной через 6 месяцев после окончания терапии был обнаружен рецидив. Побочных действий препарат не оказал. В заключении сделан вывод о том, что нифурател быстро подавляет симптомы острого неосложненного цистита у женщин и эффективен против возбудителя болезни, предотвращает возможность рецидива.
В следующей статье [10] оценивается эффективность антимикробной терапии острого цистита нифурателом (400 мг 3 раза в сутки внутрь) у 35 женщин. Критериями включения в исследование являлись: боль при мочеиспускании, частое мочеиспускание, позывы к мочеиспусканию, лейкоцитурия, возраст от 18 лет. Критериями исключения являлись: отсутствие эпизода острого цистита в предыдущие 3 месяца, отсутствие эпизода острого пиелонефрита в предыдущем месяце, частые рецидивы цистита, отсутствие болей в поясничной области, неосложненный гинекологический анамнез, отсутствие заболеваний, передаваемых половым путем. Контрольную группу составили женщины (n=31), получавшие нитрофурантоин (100 мг 2 раза в сутки) для лечения острого неосложненного цистита. Женщин обследовали на 3-й и 7-й день приема. Через 3 дня после приема нифуратела (1200 мг/сут) большинство пациентов (94,2%) субъективно отметили исчезновение позывов, лейкоцитурия исчезла у 82,8%. Но при этом 22,8% женщин по-прежнему испытывали дискомфорт при мочеиспускании, после чего было решено продлить курс антимикробной терапии нифурателом до 7 дней. Через 3 дня после приема нитрофурантоина (200 мг/сут) 83,8% женщин субъективно отметили исчезновение позывов, лейкоцитурия купирована у 77,4%. Так, в 12 (38,7%) наблюдениях было принято решение о продлении курса антимикробной терапии нитрофурантоином до 7 дней. В 1-й группе пациентов побочные реакции возникли только в 3 (8,5%) наблюдениях, во 2-й – в 13 (41,9%). В заключении сделан вывод, что противомикробная активность нифуратела достаточно высока при лечении острого неосложненного цистита. Из-за высокой чувствительности кишечной палочки нифурател эффективен как при трехдневной терапии острого цистита, так и при более длительном применении. Эффективность, благоприятный профиль безопасности и отсутствие аллергических реакций делают нифурател надежным средством лечения острого неосложненного цистита.

В проспективном исследовании [14], проведенном в 2020 г., участвовали 23 женщины с бактериальным вагинозом и рецидивирующим циститом. Они получали нифурател по 200 мг 3 раза в день. Контрольные наблюдения проводили через 7, 90, 180 дней. Критериями включения являлись: возраст от 18 до 45 лет, рецидивирующий цистит в стадии обострения, бактериальный вагиноз. Критериями исключения являлись: инфекции, передаваемые половым путем, ВИЧ, беременность и лактация, альтернативные инфекционно-воспалительные заболевания в стадии обострения; интеркуррентные соматические заболевания в стадии декомпенсации. У всех участниц исследования был диагностирован бактериальный вагиноз, а у 19 (82,6%) пациенток также выявлен кандидоз влагалища. У 17 (73,9%) женщин отметили хороший результат, у 4 (17,4%) – значительное улучшение, у 2 (8,7%) – отсутствие эффекта. Через 3 месяца после терапии у 18 из 22 оставшихся в исследовании пациенток (81,8%) не было жалоб на нарушение мочеиспускания и влагалищные выделения. В течение 6 месяцев после окончания терапии никто из участниц исследования не предъявлял жалоб. В заключении сделан вывод, что терапия нифурателом у женщин с бактериальным вагинозом и рецидивирующим циститом достаточно эффективна при обоих заболеваниях.
Два исследования, которые оценивали эффективность in vitro, были опубликованы в 1972 и 1978 гг. Hamilton-Miller et al. [16] оценивали 5 препаратов нитрофуранов (нитрофурантоин, нифурател, нитрофуразон, фуразолидон и SQ 18,506) на 201 штамме микроорганизмов. Полученные данные свидетельствуют о явном превосходстве нифуратела над нитрофурантоином по активности in vitro в отношении уропатогенов. Также результаты показывают, что нифурател является единственным доступным нитрофураном, который ингибирует C. albicans, также имея эффективность против Trichomonas vaginalis in vitro.
Одно исследование было оценено по шкале RoB2 (рис. 2), 4 исследования по шкале ROBINS-I (рис. 3) и 2 исследования – по шкале для оценки качества исследований «серия случаев» согласно NIH (табл. 2).
Обсуждение
Современные рекомендации по лечению больных с ИМП предлагают препараты 5-нитрофурана как один из наиболее оптимальных вариантов, подходящих для эффективной терапии. Однако в достаточно разнообразном ряде препаратов этой группы выделяется нифурател. Спектр действия нифуратела включает главных возбудителей острых урогенитальных инфекций: штаммы кишечной палочки, энтерококки, стрептококки и стафилококки. Для вагинальных инфекций большое значение имеет чувствительность к препарату факультативно анаэробных штаммов Gardnerella vaginalis, анаэробных бактерий Bacteroides spp. и Fusobacterium spp., Chlamydia trachomatis и Mycoplasma spp., Trichomonas vaginalis и отчасти Candida spp. [11].
Систематический обзор показывает, что эффективность нифуратела в качестве препарата терапии ИМП сопоставима и иногда превосходит эффективность других антимикробных препаратов.
Однако, учитывая большой временной промежуток между первыми исследованиями в 1960-х гг. и последними, более современными, нужно сказать, что присутствует значительная неоднородность между исследованиями, которая не предоставила возможности составить метаанализ в данном систематическом обзоре. Тем не менее стоит отметить, что даже с учетом этих недостатков представленные работы дают результаты, подтверждающие эффективность нифуратела в качестве препарата для терапии ИМП. Кроме того, наш систематический поиск литературы не дал какой-либо надежной информации об эффективности и токсичности нифуратела для особых групп населения, таких как пожилые люди и люди с почечной недостаточностью. Учитывая увеличивающееся использование нифуратела, терапия и профилактика данным препаратом в этих группах населения потребуют дальнейшего изучения.
Заключение
В настоящее время, с учетом клинического опыта и научно-практических данных, формируется точное понимание, что нельзя изолированно рассматривать ИНМП у женщин и не учитывать состояние влагалищного биоценоза и флоры кишечника. Помимо растущей резистентности кишечной палочки, есть еще ряд факторов, которые способны привести к реинфицированию у женщин.
При использовании нифуратела в качестве препарата для терапии ИМП его клиническая эффективность эквивалентна показателям других антибиотиков, а в некоторых аспектах превосходит их. Так, к примеру, препарат оказывает более выраженный терапевтический эффект в сравнении с нитрофурантоином и демонстрирует лучшую переносимость. Для нифуратела характерна высокая активность в эрадикации уропатогенов с низкой вероятностью возникновения резистентности к действующему веществу при курсовом приеме. Низкий процент рецидивов заболеваний мочевыводящих путей и отсутствие значительных побочных эффектов позволяют сформулировать вывод о достаточной эффективности нифуратела для использования в клинической практике. Кроме того, нифурател интересен тем, что активен не только в отношении уропатогенов, но и возбудителей отдельных вагинальных инфекций.
Наш систематический обзор помог суммировать клинические исследования, опубликованные на английском и русском языках в связи с выбранной методологией систематического обзора, и это позволило дать более доказательный ответ на вопрос об эффективности нифуратела, включая беременных. Однако не исключено наличие большего количества исследований за рамками данной методологии отбора. Также требуется больше рандомизированных контролируемых исследований для клинико-микробиологической оценки этого препарата.



