Основные положения
Железодефицитная анемия у женщин репродуктивного возраста: масштабы проблемы, последствия для женщины, плода и ребенка
Анемия продолжает оставаться одним из наиболее распространенных заболеваний у женщин репродуктивного возраста, внося значительный вклад в ухудшение качества жизни и увеличение показателя DALY (disability-adjusted life year − годы жизни, скорректированные по нетрудоспособности) [1].
Железодефицитная анемия (ЖДА) является наиболее распространенным патогенетическим вариантом анемии, особенно в период беременности. Дефицит железа (латентный или манифестный) имеют до 40% женщин фертильного возраста [2, 3, 4], что определяет важное значение профилактических, диагностических и лечебных мероприятий для снижения глобальных негативных последствий, в том числе в период беременности [5]. Анемия является одним из наиболее частых патологических состояний, сопровождающих течение беременности и послеродового периода [6, 7, 8]. ЖДА во время беременности может оказывать негативное влияние как на течение беременности и ее исходы, так и на развитие ребенка.
Истощение запасов железа в материнском организме – одна из причин ЖДА у детей в возрасте до 1 года. Железо участвует в обеспечении функционирования нейронов. При дефиците этого микроэлемента нарушаются активность нейромедиаторов и энергетический обмен в мозге, ухудшается миелинизация, что способствует расстройству когнитивных и адаптационных функций [9, 10].
В случае наступления беременности на фоне скрытого дефицита железа, вероятность развития ЖДА у женщины и далее у новорожденного крайне высока [11]. Наиболее частыми негативными эффектами ЖДА у матери на плод являются гипотрофия, гипоксия плода, задержка внутриутробного развития, морфофункциональная незрелость, повышение риска внутриутробного инфицирования. У новорожденных нередко развиваются асфиксия различной степени тяжести, анемия [12].
Выявлена связь между материнским статусом железа в I триместре беременности и массой тела ребенка. Концентрация гемоглобина (Hb) у беременной женщины менее 110 г/л связана с 3-кратным повышением риска рождения ребенка с низкой массой тела. На каждые 10 г/л увеличения Hb у матери в первой половине беременности на ⅓ снижается риск рождения ребенка с низкой массой тела [13]. У матерей с анемией в III триместре выше вероятность преждевременных родов и рождения детей с низкой массой тела [14], а также повышается риск перинатальной и неонатальной смертности [15].
Изучено влияние анемии матери на развитие нервной системы плода. Объем гиппокампа и продукция нейротрофического фактора головного мозга (brain-derived neurotrophic factor − BDNF) значительно снижаются и коррелируют с тяжестью анемии у матери [16]. Отмечено негативное влияние анемии беременных на раннюю адаптацию новорожденных детей. Показатели моторного развития детей 1-го года жизни, родившихся у матерей с анемией, свидетельствовали об отставании в среднем на 1,5 месяца от возрастной нормы. У детей 1-го года жизни чаще регистрируются анемия, а также болезни верхних дыхательных путей, аллергический дерматит, заболевания желудочно-кишечного тракта [17].
Несмотря на многосторонность и длительность изучения вопросов дифференциальной диагностики, эффективности различных подходов при анемиях, отсутствуют единые алгоритмы, позволяющие унифицировать профилактические, диагностические и терапевтические мероприятия при дефиците железа, в том числе в период беременности. Отсутствуют единые подходы к рациональной фармакотерапии анемического синдрома, недостаточно понимание необходимости коррекции анемии не только для устранения симптомов заболевания, но и для профилактики осложнений беременности, родов, послеродового периода, а также профилактики ЖДА у новорожденного.
Вопросы диагностики и лечения ЖДА во время беременности и в послеродовом периоде относятся к компетенции врача акушера-гинеколога при консультации с врачом-терапевтом (врачом-гематологом) согласно Приказу Минздрава России N 572н «Об утверждении Порядка оказания медицинской помощи по профилю “акушерство и гинекология”» от 01.11.2012 [18].
Вопросы диагностики железодефицитной анемии во время беременности, после родов и в период грудного вскармливания
Для оценки наличия нарушений обмена железа необходимо при первом обследовании выполнить общий анализ крови и определить концентрацию сывороточного ферритина (СФ).
По данным ВОЗ, анемия во время беременности определяется по концентрации Hb менее 110 г/л. Центр по контролю и профилактике заболеваний США (Centers for Disease Control and Prevention – CDC) указывает на особенность диагностики анемии во II триместре: с 13-й по 28-ю неделю беременности анемией считается снижение концентрации Hb менее 105 г/л.
Анемия в послеродовом периоде диагностируется при концентрации Hb менее 100 г/л [7, 19], в период грудного вскармливания − снижении концентрации Hb менее 120 г/л.
СФ является наиболее специфичным показателем для оценки дефицита железа в организме [20]. Концентрация СФ менее 30 мкг/л свидетельствует о дефиците железа [20–22], поэтому видится целесообразным включение скрининга на СФ в первый пренатальный визит и далее не реже 1 раза в триместр. Скрининг на СФ на этапе прегравидарной подготовки – оптимальный вариант профилактики ЖДА беременных.
На основании показателя среднего объема эритроцитов (mean corpuscular volume − MCV) в общем анализе крови можно выделить 3 группы анемий (табл. 1).
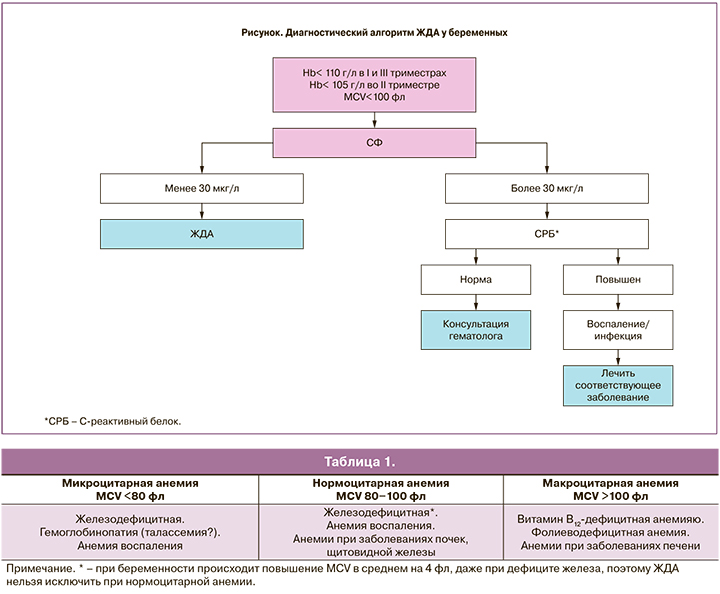
В компетенции акушера-гинеколога – первичная оценка всех микроцитарных и нормоцитарных анемий, оценка показателей обмена железа, назначение терапии пероральными препаратами железа при выявленном дефиците железа.
Макроцитарные анемии, анемии, резистентные к проводимой терапии пероральными препаратами железа, сочетание анемии со снижением количества лейкоцитов и/или тромбоцитов требуют консультации гематолога и/или терапевта (рисунок).
Вопросы лечения железодефицитной анемии
Назначение препаратов железа − основа терапии ЖДА, но уточнение и устранение причин, приведших к развитию анемии, являются непременными условиями для достижения эффекта.
Первой линией терапии ЖДА являются пероральные препараты железа.
Для лечения ЖДА доступны солевые препараты железа, которые могут быть как двухвалентными (сульфат, глюконат, фумарат), так и трехвалентными (протеинсукцинилат), а также железа (III) гидроксид полимальтозат. Солевые препараты железа и железа (III) гидроксид полимальтозат сопоставимы по эффективности, но препараты железа (III) гидроксида полимальтозата отличаются более высоким профилем безопасности и лучшей переносимостью. Хорошая переносимость и отсутствие нежелательных явлений препарата особенно важны во время беременности, так как тошнота, запоры, вздутие живота могут ухудшать состояние беременных значительно более выраженно, чем дефицит железа, и привести к прекращению приема препаратов железа. Приверженность беременных пациенток лечению ЖДА остается недостаточной [23]. Одна из основных причин этого – нежелательные явления при применении препаратов железа [24]. Поэтому для повышения приверженности лечению целесообразно исходный выбор останавливать на препарате с наилучшей переносимостью. Таковым зарекомендовал себя железа (III) гидроксид полимальтозат в сравнении с солями железа (сульфат, фумарат, глюконат) [25−28].
Адекватная суточная доза железа для лечения ЖДА составляет 160−200 мг при использовании солевых препаратов двухвалентного железа и 200−300 мг при применении железа (III) гидроксид полимальтозата.
Через 1 месяц от начала ферротерапии следует оценить эффективность проводимого лечения. Критерием эффективности терапии является повышение концентрации Hb на 10 г/л через 1 месяц терапии. Более раннее определение прироста Hb видится нецелесообразным.
Терапия ЖДА предполагает длительное применение препаратов железа для перорального приема: после нормализации концентрации Hb необходимо продолжить терапию с целью восполнения запасов железа. Обычно длительность курса лечения пероральными препаратами железа составляет от 3 месяцев при легкой анемии до 6 месяцев при тяжелой анемии. У беременных с ЖДА прием препаратов железа в профилактической дозе необходимо продлевать до конца беременности и в период лактации. Перед прекращением ферротерапии необходимо удостовериться в нормализации результатов общего анализа крови и концентрации СФ [4, 20, 21, 22, 29].
В подавляющем большинстве случаев отсутствие ожидаемого эффекта лечения требует не смены одного препарата железа на другой, а поиска причин неэффективности терапии (неадекватность дозы препарата железа, низкая приверженность терапии и др.).
Назначение парентеральных препаратов железа разрешено со II триместра беременности при лабораторно доказанном дефиците железа. Основными показаниями для назначения парентеральных препаратов железа являются [4, 7, 19, 20]:
- ЖДА с Нb менее 80 г/л (при необходимости более быстрого достижения эффекта);
- ЖДА после 34 недель беременности (при выраженном анемическом синдроме или концентрации Hb менее 80 г/л рекомендовано добавление к парентеральным препаратам железа препаратов рекомбинантного человеческого эритропоэтина − рчЭПО);
- неэффективность лечения пероральными препаратами железа;
- непереносимость пероральных препаратов железа (тошнота, рвота, запоры, поносы);
- установленный диагноз патологии желудочно-кишечного тракта (ЖКТ) с нарушением всасывания железа (синдром мальабсорбции, энтериты, воспалительные заболевания кишечника, инфекция H. pylori, целиакия);
- отказ от приема пероральных препаратов железа.
Анализ имеющихся данных литературы [4, 20, 21, 22] позволил составить алгоритм ведения пациенток с ЖДА на этапе планирования беременности, во время беременности, в послеродовом периоде и далее до окончания грудного вскармливания (табл. 2).

Таким образом:
- соблюдение объема и сроков обследования женщин репродуктивного возраста позволяет своевременно выявлять не только ЖДА, но даже начальные стадии дефицита железа;
- ранняя диагностика способствует своевременному назначению терапии и не позволяет развиться осложнениям как у матери, так и у плода;
- при необходимости терапии должен избираться максимально физиологичный подход до полного восстановления показателей обмена железа.
Совет Экспертов проходил при поддержке компании ЗАО «Сандоз».



