Проблемой является запоздалая диагностика заболевания. От момента появления первых жалоб до окончательной диагностики заболевания даже в развитых странах происходит в среднем 6,8 года. Ведущие исследователи и хирурги придерживаются тактики органосохраняющих реконструктивно-пластических операций у пациенток репродуктивного возраста при распространенных формах инфильтративного эндометриоза с минимальным воздействием на очаги эндометриоза смежных органов. Неудовлетворительные результаты проводимого лечения при тяжелых формах инфильтративного эндометриоза, наличие резидуального эндометриоза, а также отсутствие статистически убедительных данных о значительном улучшении репродуктивной функции женщин после перенесенных «паллиативных» операций привели к расширению показаний для более радикальных операций на органах малого таза при этой форме заболевания.
Однако количество и характер осложнений, возникающих у пациенток с распространенными формами инфильтративного эндометриоза, прямо пропорциональны объему выполняемой операции. Так, по данным литературы, частота осложнений после лапароскопических операций при инфильтративном эндометриозе составляет 3,4%, увеличиваясь до 10–22% при колоректальной резекции. Кишечные и мочевые свищи являются наиболее тяжелыми осложнениями хирургического лечения инфильтративного эндометриоза, резко ухудшающими качество жизни женщин. В связи с этим такой «агрессивный» метод хирургического лечения инфильтративных форм эндометриоза требует изучения в плане как восстановления репродуктивной функции у молодых женщин, так и уменьшения числа осложнений во время и после операции.
Нами были обследованы и прооперированы 86 пациенток с инфильтративными формами генитального и экстрагенитального эндометриоза в возрасте от 21 до 45 лет, средний возраст составил 30,4±0,4 года. Гинекологическое обследование при квалифицированном исполнении обеспечивает ценную диагностическую информацию. Осмотр больных с подозрением на глубокий инфильтративный эндометриоз мы проводили до и во время менструации, что позволило во всех случаях определить наличие болезненных бугристых инфильтратов позади и кпереди от шейки матки, в досягаемых областях клетчаточных пространств таза. Деформация и инфильтрация тканей кпереди от шейки матки, боль во время исследования, позывы к мочеиспусканию наводили на мысль о вовлечении в патологический процесс стенки мочевого пузыря. Дополняя исследование ректальным осмотром, особенно у пациенток с характерными симптомами нарушения эвакуаторной функции прямой кишки и наличия патологического отделяемого, выявляли наличие плотного болезненного инфильтрата, чаще в передней стенке верхнеампулярного отдела прямой кишки и ректосигмоидного отдела толстой кишки. При этом важно учитывать такие критерии, как размеры инфильтрата, подвижность слизистой оболочки кишки над ним, наличие ее втяжений в ткань инфильтрата, наличие деформации и сужения просвета кишки, распространение патологического процесса на параректальную клетчатку и клетчатку боковых стенок таза, наличие крови в просвете кишки. Надо отметить, что полученные данные позволяли только предположить наличие колоректального эндометриоза, но никак не оценить степень его инвазии.
Обладающее высокой чувствительностью и удобством скринингового метода УЗИ при эндометриозе органов малого таза было выполнено всем больным. Исследование проводилось на аппаратуре фирмы «Аloka-636» и «Аloka SSD-650». Последовательно выполняли сканирование брюшной полости, забрюшинного пространства, органов малого таза через переднюю брюшную стенку, трансвагинально и трансректально датчиками с частотой 3,5 и 7,5 МГц.
При этом выявляли не только более простые для диагностики формы эндометриоза − эндометриоидные кисты и аденомиоз, но и инфильтративные формы генитального и экстрагенитального эндометриоза − ретроцервикальной и ректовагинальной локализации, эндометриоз стенки верхнеампулярного отдела прямой кишки и ректосигмоидного отдела толстой кишки, мочевого пузыря, передней брюшной стенки.
У всех пациенток оценивали состояние органов мочевыделительной системы − наличие и степень расширения проксимальных отделов мочеточников, изменение чашечно-лоханочного сегмента. Однако нередко сопутствующий эндометриозу спаечный процесс малого таза затруднял визуализацию вследствие наложения на исследуемую область петель кишки или большого сальника, что снижало чувствительность метода для тонкой топической диагностики поражения. Кроме того, результаты ультразвуковой диагностики при определенных условиях не лишены субъективизма.
 Всем больным была выполнена МРТ малого таза и забрюшинного пространства. Возможность значительной детализации патологического процесса и выявления нарушений анатомии органов малого таза на фоне распространенного инфильтративного эндометриоза, получаемая при МРТ, позволила выставить правильный диагноз. Исследования проведены на МР-томографе Magnetom Hamone фирмы Siemens (Германия). Критериями оценки распространения заболевания были: локализация, размеры, структура патологического очага, глубина инвазии вовлеченного в патологический процесс органа, прорастание эндометриоидной ткани в просвет влагалища, степень распространения в ректовагинальном пространстве, глубина инвазии в стенку толстой кишки с наличием или отсутствием поражения слизистой оболочки, наличие участков синхронного поражения толстой кишки, вовлечение в процесс стенки мочевого пузыря, поражение тазовой клетчатки, наличие уродинамически значимой стриктуры мочеточников, расширение чашечно-лоханочного сегмента почек до формирования гидронефроза. Выполнение МРТ с введением лазикса отражало полную картину состояния мочевыводящей системы (рис. 1).
Всем больным была выполнена МРТ малого таза и забрюшинного пространства. Возможность значительной детализации патологического процесса и выявления нарушений анатомии органов малого таза на фоне распространенного инфильтративного эндометриоза, получаемая при МРТ, позволила выставить правильный диагноз. Исследования проведены на МР-томографе Magnetom Hamone фирмы Siemens (Германия). Критериями оценки распространения заболевания были: локализация, размеры, структура патологического очага, глубина инвазии вовлеченного в патологический процесс органа, прорастание эндометриоидной ткани в просвет влагалища, степень распространения в ректовагинальном пространстве, глубина инвазии в стенку толстой кишки с наличием или отсутствием поражения слизистой оболочки, наличие участков синхронного поражения толстой кишки, вовлечение в процесс стенки мочевого пузыря, поражение тазовой клетчатки, наличие уродинамически значимой стриктуры мочеточников, расширение чашечно-лоханочного сегмента почек до формирования гидронефроза. Выполнение МРТ с введением лазикса отражало полную картину состояния мочевыводящей системы (рис. 1).
При подозрении на поражение мочевого пузыря, мочеточников, толстой кишки в комплекс диагностических мероприятий в обязательном порядке включали эндоскопические методы исследования − цистоскопию и колоноскопию, выполненные 18 (20,9%) и 67 (77,9%) больным соответственно. Несмотря на инвазивный характер исследований, во всех случаях была получена ценная информация о степени инвазии эндометриоза, повлиявшая на выбор адекватного объема планируемого оперативного вмешательства. При этом при получении дополнительной информации о расположении эндометриоидного инфильтрата относительно устьев мочеточников и вовлечении их в патологический процесс менялась тактика предоперационной подготовки.
Длительность заболевания варьировала в пределах от 2 до 12 лет, в среднем составила 6,7±0,5 года. При этом 62 (72%) женщины были заинтересованы в сохранении и реализации репродуктивной функции. У 69 (80,2%) пациенток преобладали жалобы на стойкий болевой синдром, обильные менструации наблюдались у 69 (80,2%) пациенток, анте-постпонирующие сукровичные скудные выделения − у 51 (59,3%) больной, диспареуния − у 31 (36%) женщины, 58 (67,5%) пациенток страдали бесплодием.
При акцентированном сборе анамнеза были выявлены симптомы поражения смежных органов. Так, у 21 (24,4%) женщины в период менструации возникала задержка стула и нарушение отхождения газов, сопровождающееся выраженным болевым синдромом и вздутием живота, у 12 (13,9%) пациенток отмечалось выделение слизи и крови из прямой кишки, тенезмы наблюдались у 7 (8,1%) больных. В 24 (33,3%) наблюдениях отмечено учащенное и болезненное мочеиспускание, у 6 (6,9%) женщин – выделение мочи, окрашенной кровью, у 4 (4,6%) – почечные колики.
Подавляющее большинство (67–77,9%) женщин ранее уже подвергались оперативному лечению. Среди них 12 (17,9%) пациенток перенесли 2 оперативных вмешательства, 7 (10,4%) – 3 операции, 3 (4,4%) пациентки – 5 операций по поводу эндометриоза. Анализ ранее проведенных оперативных вмешательств показал, что у 34 (50,7%) больных была выполнена энуклеация эндометриоидных кист яичников, у 17 (25,3%) женщин проводилась коагуляция очагов эндометриоза тазовой брюшины, крестцово-маточных связок и ретроцервикального эндометриоза. Частичное иссечение очага ретроцервикального эндометриоза было выполнено в 7 (10,5%) наблюдениях, адгезиолизис в малом тазу был проведен у всех пациенток. При локализации очага эндометриоза на стенке толстой кишки объем операции у 2 (2,9%) больных сводился к частичному иссечению эндометриоза (биопсии) стенки патологического очага, у 4 (6,5%) больных была выполнена его коагуляция. Коагуляция очага инфильтративного эндометриоза, локализованного на стенке мочевого пузыря, проведена у 3 (4,4%) пациенток. Объем операции ограничился диагностической лапароскопией и констатацией факта распространенного эндометриоза у 11 (16,4%) пациенток.
Согласно данным анамнеза, всем пациенткам в послеоперационном периоде проводилась терапия агонистами гонадотропин-рилизинг гормона курсами от 4 до 6 мес. Важно отметить, что у всех пациенток после отмены гормональной терапии в разные сроки симптомы заболевания возникали вновь. Так, у 38 (56,7%) больных жалобы, беспокоящие их до лечения, возникли через 2 месяца после отмены препарата, у 21 (31,3%) − через 6 месяцев, у 8 (11,9%) симптомы заболевания возникли уже в следующем цикле после прекращения консервативной терапии. Кроме того, в описываемой группе пациенток ни у одной из них не была реализована репродуктивная функция.
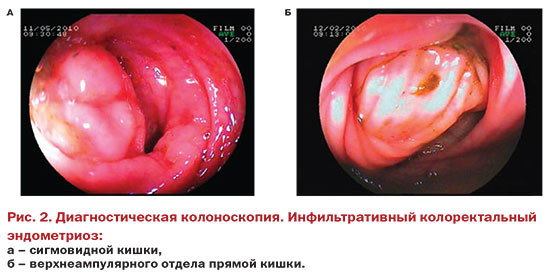
Наиболее частыми косвенными признаками колоректального эндометриоза были: наличие подслизистого образования в стенке кишки – 34 (39,5%), обеднение или отсутствие сосудистого рисунка слизистой оболочки – 27 (31,3%), наличие разницы окрашивания слизистой оболочки над образованием и вне его при проведении электронной хромоколоноскопии – 17(19,7%), боль при контакте с эндоскопом области инфильтрата – 32 (37,2%), изменение подвижности слизистой оболочки над образованием – 30 (34,8%) (рис. 2).
У 19 (22%) больных наблюдали повышенную контактную кровоточивость слизистой оболочки. Наличие эндометриоидных гетеротопий на слизистой оболочке кишки в проекции инфильтрата выявили только в 10 (11,6%) наблюдениях, полиповидные разрастания слизистой оболочки в области образования – в 9 (10,4%), деформацию просвета кишки – в 4 (16,2%), стеноз − в 7 (8,%) случаях.
Всем пациенткам во время колоноскопии была выполнена биопсия области инфильтрата. При этом морфологическое подтверждение диагноза колоректального эндометриоза, по данным щипцовой биопсии, было получено в 17 (25,3%) случаях. В 3 (4,4%) наблюдениях мы применили метод глубокой пункционной биопсии, позволяющий произвести забор ткани из эндометриоидного инфильтрата на глубине от 0,5 до 1,0 см. Во всех случаях диагноз был подтвержден.
Отмечены различные локализации инфильтративного генитального и экстрагенитального эндометриоза. Колоректальный эндометриоз был выявлен у 57 (66,2%) больных, при этом чаще всего процесс поражал ректосигмоидный отдел толстой кишки. У 33 (38,3%) больных наблюдали сочетание с ретроцервикальным эндометриозом, у 17 (19,7%) женщин процесс был локализован в передней стенке верхнеампулярного отдела прямой кишки в сочетании с эндометриозом ректовагинальной перегородки, сигмовидная кишка была вовлечена в процесс в 7 (8,1%) наблюдениях. У 12 (13,8%) больных диагностировано поражение стенки мочевого пузыря, у 6 (6,9%) пациенток – с прорастанием в слизистую оболочку. Распространение эндометриоза в клетчаточные пространства малого таза с вовлечением в процесс дистальных отделов мочеточников было выявлено у 7 (8,1%) пациенток; при этом у 5 (5,8%) больных эти изменения были уродинамически значимыми и привели к развитию гидронефроза, а в 3 (3,4%) случаях − к сморщиванию почки с полной потерей ее функции. Эндометриоз передней брюшной стенки, как правило, был локализован в области послеоперационных рубцов: после операций кесарева сечения – в 9 (10,4%) наблюдениях, у 1 (1,1%) женщины диагностирован эндометриоз промежности в рубце после эпизиотомии.
В наших наблюдениях были выявлены редкие локализации эндометриоидных гетеротопий, которые сочетались с ранее перечисленными локализациями основного очага заболевания. Эндометриоз червеобразного отростка диагностирован у 2 (2,2%) больных, эндометриоидное поражение терминальной петли подвздошной кишки − у 2 (2,2%) больных. У 1 (1,1%) больной эндометриоз был локализован в пресакральной клетчатке с компрессией нервных стволов сакрального сплетения с яркой клинической картиной неврологического характера.
Для купирования процесса обструктивного пиелонефрита в предоперационном периоде при наличии блока мочеточника и гидронефроза было выполнено стентирование мочеточников: одностороннее – в 5 (5,8%), двустороннее – в 2 (2,3%) наблюдениях.
Операции выполнялись в сроки от 8 месяцев до 3 лет после предыдущего оперативного лечения. При этом степень распространения процесса была значительной, и с учетом данных прежних протоколов УЗИ и МРТ практически не отличалась от операционной картины, что может свидетельствовать о неадекватном объеме ранее выполненных операций. Расчет на консервативную терапию, неэффективную при инфильтративных формах эндометриоза, оказался неоправданным, так как ни один медикаментозный препарат не устраняет морфологический субстрат эндометриоза, а оказывает только опосредованное влияние на его биологическую активность, на что указывают ряд признаков. Поэтому все случаи такого раннего рецидива заболевания следует расценивать как резидуальный, то есть неудаленный эндометриоз при первичных операциях.
Все оперативные вмешательства начинались с выполнения диагностической лапароскопии, ревизии органов малого таза и брюшной полости с использованием четырех троакаров, во время которой оценивалась возможность проведения операции лапароскопическим методом. В трети случаев (21–24,5%) было принято решение о переходе на лапаротомию. Показаниями к лапаротомии были невозможность выполнения планируемого объема операции и опасность ятрогении ввиду значительного распространения эндометриоидного инфильтрата на клетчаточные пространства пресакральной области, паравезикальной и парауретральной клетчатки, интимного плотного сращения эндометриоза с надкостницей костей таза.
У 42 (48,8%) пациенток эндометриоидный инфильтрат был иссечен в пределах здоровых тканей со стенки пораженного мочевого пузыря и толстой кишки. При этом в 27 (31,3%) случаях поражения смежных органов сочетались с ретроцервикальным эндометриозом, в 12 (13,9%) – с эндометриозом ректовагинального пространства. Инвазия эндометриоза в стенку кишки до мышечного слоя была выявлена у 26 (30,2%) пациенток, до подслизистого слоя – у 13 (15,1%), до слизистой оболочки мочевого пузыря – у 14 (16,2%) больных. Стенку кишки ушивали отдельными узловыми викриловыми швами (00). Дефект стенки мочевого пузыря ушивали двухрядным викриловым швом (00): первый ряд – ушивание мышечной оболочки (детрузора), второй ряд – перитонизация серозным покровом.
При прорастании эндометриоза в просвет кишки в зависимости от площади и размеров инфильтрата выполняли два варианта резекции. Клиновидная резекция в 2/4 или в 3/4 была выполнена в 9 (10,4%) случаях при размерах прорастания эндометриоидного инфильтрата слизистой оболочки от 0,5 до 2,5 см. Техника операции заключалась в том, что после иссечения основного объема эндометриоидного инфильтрата со стенки кишки на участок прорастания накладывали провизорный шов, с помощью которого резецируемый участок погружали в аппарат циркулярного шва диаметром 34 мм с формированием линии шва на передней полуокружности кишечной трубки. Линию скрепочных швов перитонизировали отдельными серо-серозными швами.
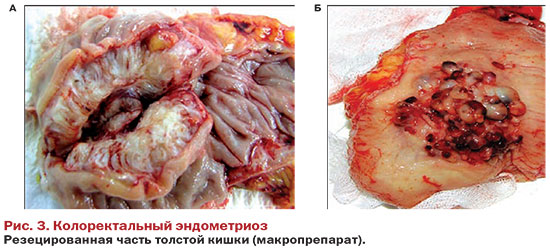
Передняя резекция была выполнена у 21 (24,4%) больной при распространенном поражении толстой кишки с формированием клинически значимого стеноза и заключалась в удалении части кишечной трубки с формированием компрессионного циркулярного толстокишечного анастомоза диаметром 33 мм. В отличие от операций, предпринимаемых по поводу рака толстой кишки, выделение пораженного участка кишечной трубки должно выполняться в непосредственной близости к кишечной стенке. Это объясняется отсутствием необходимости удаления региональных лимфатических узлов. Данная методика является профилактикой нарушения кровоснабжения и иннервации органов малого таза, что позволяет избежать развития парадоксальной ишурии, возникающей в связи с денервацией мочевого пузыря, особенно при низких резекциях прямой кишки (рис. 3).
Лапароскопическая резекция мочевого пузыря в связи с поражением всех слоев его стенки выполнена 5 (6,9%) больным. При этом размеры дефекта стенки мочевого пузыря после иссечения составляли от 1,5 до 4 см. Целостность стенки восстанавливали трехрядным викриловым швом с проведением контрольной интраоперационной цистоскопии.
При поражении эндометриозом червеобразного отростка у 9 (10,4%) больных выполнили аппендектомию по принятой в клинике методике.
Для обеспечения хорошей визуализации позадиматочного пространства при обширных эндометриоидных инфильтратах и спаечных конгломератах малого таза во всех случаях после разделения висцеро-висцеральных, висцеро-париетальных спаек выполняли транспозицию яичников узловыми швами к париетальной брюшине подвздошных областей. Мочеточники прослеживали под брюшиной, оценивали их взаимоотношение с границей эндометриоидного инфильтрата. При близком расположении их к инфильтрату рассекали париетальную брюшину в неизмененной зоне и выполняли диссекцию мочеточников до уровня маточных сосудов. При вовлечении дистальных отделов мочеточников в патологический процесс выполняли интраоперационную цистоскопию и стентирование мочеточника на стороне поражения. При прогнозируемой массивной кровопотере для снижения региональной перфузии осуществляли временную окклюзию внутренних подвздошных артерий. Диссекцию тканей всегда начинали на 0,5–1,0 см латеральнее очага инфильтративного эндометриоза в зоне неизмененной клетчатки таза.
Иссечение очагов эндометриоза проводили гармоническим скальпелем, а вблизи анатомических образований (мочеточников, магистральных сосудов, стенки кишки и т.д.) – ножницами. Для иссечения эндометриоза стенки толстой (прямой) кишки, мочевого пузыря нередко использовали гидропрепаровку, для чего в подслизистый слой вводили 5–10 мл 0,9% физиологического раствора. После иссечения очагов и достижения гемостаза выполняли перитонизацию узловыми викриловыми швами.
После резекции толстой кишки проводили декомпрессию ее просвета анальным зондом диаметром до 1,5 см, установленным проксимальнее линии анастомоза. Через сутки после операции проводили болюсное промывание просвета кишки растворами антисептиков. Удаляли зонд на 4–5-е сутки. Постоянная декомпрессия мочевого пузыря в течение 10 сут послеоперационного периода в случае его резекции сопровождалась ежедневным промыванием полости водным раствором фурациллина 1:5000.
В 7 (9,7%) случаях экстрагенитального эндометриоза передней брюшной стенки были иссечены очаги с пластикой дефекта по ненатяжной методике сетчатым трансплантатом по методу SUB LAY.
В послеоперационном периоде проводилась инфузионно-коррегирующая терапия, профилактика тромбоэмболических осложнений.
Число возникших осложнений после проведенных операций коррелирует с данными отечественных и зарубежных авторов. Мы наблюдали 7 (8,1%) случаев осложнений. Так, в 4 (4,6%) наблюдениях у пациенток сохранялась продолжительная, от 7 до 14 сут, лимфорея из клетчатки забрюшинного пространства объемом от 500 до 1000 мл, потребовавшая длительного дренирования Дугласова пространства. В 2 (2,3%) случаях в раннем послеоперационном периоде на 3-и сутки развилась острая спаечная послеоперационная непроходимость, что потребовало повторной операции для устранения причины непроходимости, назогастроинтестинальной интубации. Несостоятельность прямокишечно-сигмовидного анастомоза была выявлена у 1 (1,16%) больной. В этом случае повторная операция закончилась ушиванием участка несостоятельности анастомоза, широким дренированием параректального пространства и наложением разгрузочной трансверзостомы.
Клинический эффект лечения оценивали по следующим критериям качества жизни пациенток: субъективные ощущения (исчезновение или изменение характера болевого синдрома), социальная реабилитация, сексуальная жизнь, фертильность.
У 84 (97,6%) больных после операции был получен значимый клинический эффект, что было связано с устранением таких тяжелых симптомов заболевания, как ректальные кровотечения, нарушения эвакуаторной функции толстой кишки, стойкий болевой синдром, макрогематурия, рецидивирующая дизурия, почечные колики. Это позволило этим пациенткам восстановить социальную и ролевую функцию в семье и на работе. Из 31 (36%) больной, у которой наблюдалась диспареуния, лишь у одной после операции отмечалась менее интенсивная боль при половой жизни, что, по всей видимости, связано с наличием диффузно-узловой формы аденомиоза. У 4 (7%) пациенток в течение первого года после операции наступила беременность: у одной самостоятельно, у трех с использованием ЭКО.
Приведенные данные объективно показали важность акцентированного выявления симптомов поражения органов, не относящихся к системе репродукции. В сочетании с грамотно выполненным осмотром женщины этот начальный этап дает возможность планировать обследование и тактику хирургического лечения.
Современная инструментальная диагностика распространенных форм эндометриоза представляет собой систематизированный комплекс последовательно проводимых исследований. В случаях колоректального эндометриоза и эндометриоза мочевыделительной системы особую значимость приобретают МРТ и эндоскопические методы − колоноскопия и цистоскопия. Высокая чувствительность МРТ, возможность детализации степени инвазии эндометриоза в стенку кишки, диагностика нарушений эвакуаторной функции почек на фоне компрессии мочеточников эндометриоидным инфильтратом без применения контрастирующих веществ и отсутствие лучевой нагрузки делают этот метод ведущим в диагностике тяжелых форм заболевания.
В последнее время стала шире использоваться колоноскопия в диагностике колоректального эндометриоза, который в первую очередь следует дифференцировать с карциномой, неэпителиальными опухолями толстой кишки. В большинстве случаев эндоскопическая картина при инфильтративном эндометриозе представлена подслизистым образованием в стенке толстой кишки с отсутствием или незначительными проявлениями на слизистой оболочке в виде гиперемии, обеднения или отсутствия сосудистого рисунка. В редких случаях удается выявить очаги эндометриоза синюшного цвета размерами от 3 до 5 мм. Дифференциальная диагностика становится возможной при проведении щипцовой и пункционной биопсии, позволяющей установить верный диагноз.
Вопрос о том, может ли излишняя хирургическая агрессивность на органах нерепродуктивной системы повлиять на сохранность репродуктивной функции пациентки, остается открытым. Однако приводимые данные объективно доказывают, что чрезмерный «консерватизм» при выполнении операции приводит к большому количеству неудовлетворительных результатов лечения, прогрессированию заболевания, неутешительному прогнозу фертильного здоровья женщин. Качество лечения эндометриоза обусловлено и зависит прежде всего от своевременности и объема проведенного оперативного вмешательства.
В настоящее время принято считать, что «золотым стандартом» хирургического лечения «малых» форм эндометриоза является лапароскопия, тяжелых и сочетанных форм эндометриоза – лапаротомия. Мы считаем лапароскопический метод приоритетным в лечении инфильтративных форм эндометриоза при условии высокой профессиональной подготовки оперирующего хирурга. Даже в случаях повторных операций или планируемой резекции пораженного органа (толстой кишки, мочевого пузыря) использование лапароскопической техники при определенном навыке обеспечивает лучшую, чем при лапаротомии, степень детализации патологически измененных тканей, особенно в случаях мультифокального поражения и измененной анатомии органов малого таза. Необходимость расширения доступа должна быть продиктована объективными причинами в каждом конкретном случае. Стремление хирурга вопреки всему выполнить операцию лапароскопическим методом не должно быть определяющим.
Выводы
При обследовании пациенток с распространенными формами инфильтративного эндометриоза, особенно в группе ранее оперированных больных, необходимо учитывать возможность наличия экстрагенитального эндометриоза любой локализации. Нацеленность врача на поиск распространения патологического процесса за пределы органов репродуктивной системы является залогом достоверной диагностики заболевания.
Диагностика распространенных инфильтративных форм эндометриоза должна включать применение комплекса современных методов обследования: УЗИ, МРТ, колоноскопию, цистоскопию для уточнения распространенности процесса, биопсию патологических очагов с целью исключения злокачественного характера изменений. Успех хирургического лечения эндометриоза зависит от адекватности объема первичной операции, что особенно важно для пациенток молодого возраста. Лапароскопический доступ является предпочтительным при проведении оперативного лечения инфильтративного эндометриоза, включая выполнение операций на мочевом пузыре, мочеточниках, толстой кишке.



