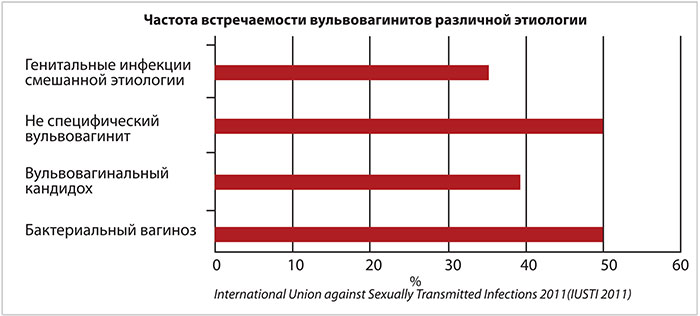
Воспалительные заболевания нижних отделов половых путей (вульвиты, вагиниты) являются одной из наиболее распространенных причин обращения к врачу акушеру-гинекологу [1]. Так, например, согласно данным Европейского международного союза по борьбе с инфекциями, передаваемыми половым путем (IUSTI – International Union against Sexually Transmitted Infections) 2011 года анализ зарубежных исследований, опубликованных в период между 1966 и 2003 гг., показал, что у женщин с симптомами вагинита наиболее часто диагностируется бактериальный вагиноз (БВ) – в 22–50%, вульвовагинальный кандидоз – (ВВК) в 17–39%, трихомониаз в – 4–35% случаев (см. рисунок) [2].
От неспецифического вагинита (НВ) страдает почти каждая пятая пациентка (19,2%) гинекологической практики, а среди пациенток с патологическими белями частота его выявления возрастает в 4 раза [3].
Вульвовагинит – воспаление слизистой оболочки влагалища и вульвы. В настоящее время среди инфекционных вагинитов выделяют специфические вагиниты, вызванные патогенами (Neisseria gonorrhoeae, Trichomonas vaginalis, Chlamydia trachomatis, Candida spp. и др.), и неспецифические, обусловленные условно-патогенными микроорганизмами (УПМ), такими как стрептококки, стафилококки, кишечная палочка и др.
Различают острую и хроническую форму течения заболевания. Острая форма заболевания отличается ярко выраженными жалобами, а хроническая форма обладает менее явными, слабо выраженными симптомами.
Бактериальный вагиноз
На сегодняшний день по структуре инфекций влагалища БВ занимает лидирующее положение. БВ – это полимикробный невоспалительный синдром, характеризующийся дисбиозом генитального тракта, развивающийся вследствие замещения нормальных Lactobacillus sp., вырабатывающих перекись водорода (<105 КОЕ/мл), большим количеством (106–108 КОЕ/мл) анаэробных бактерий (Prevotella sp., Mobiluncus sp., G.vaginalis, Ureaplasma, Micoplasma и др.) и многочисленными требовательными к условиям культивирования, а также некультивируемыми бактериями, включая представителей вида Atopobium и сопровождающийся увеличением pH [4]. БВ встречается в различных популяциях женщин от 16 до 65%, у 15–37% беременных женщин. Считается, что в современном мире каждая женщина имела БВ хотя бы один раз в жизни. Интересно, что БВ может возникать и исчезать спонтанно и не относится к ИППП, а также до настоящего времени БВ не вошел в МКБ 10-го пересмотра, по всей видимости, в связи с тем, что окончательно не установлена его роль и место в структуре инфекционных заболеваний нижнего отдела гениталий. Возможно, в МКБ 10-го пересмотра его можно отнести к шифру N89.5 «Бели не уточненные как инфекционные» или к шифру N 89.9 – «Другие не воспалительные болезни влагалища». Тем не менее, в настоящее время данной проблеме уделяется большое внимание в связи не только с широким распространением БВ, но и с возникновением тяжелой патологии женских половых органов и осложнений беременности и родов.

Основная роль в возникновении БВ отводится воздействию экзогенных и эндогенных триггерных факторов. К эндогенным триггерным факторам относятся: гормональные изменения, нарушение микробиоценоза желудочно-кишечного тракта, снижение количества Н2О2-продуцирующих лактобацилл и концентрации Н2О2 в содержимом влагалища, а также нарушение в системе местного иммунитета.
Кроме того, доказано, что лактобациллы могут поражаться специфическими вирусами, в результате чего они не могут колонизировать влагалище, что облегчает преимущественное размножение анаэробов.
К триггерным факторам экзогенного генеза относятся: длительная нерациональная терапия антибиотиками и другими лекарственными препаратами, частые и чрезмерные влагалищные души, спринцевания и др.
Большинство экспертов считают, что основным фактором риска БВ является сексуальная активность. БВ не развивается у женщин, которые не имели вагинальных контактов [5, 6]. У сексуально активных женщин дополнительными факторами риска развития БВ являются множество половых партнеров, частая их смена, спринцевание и курение [7, 8].
Клиническая картина и диагностика. Клиническая картина характеризуется наличием жидких выделений из половых путей сероватого цвета с неприятным запахом протухшей рыбы, иногда женщины предъявляют жалобы на зуд и жжение. «Золотым стандартом» диагностики БВ во всем мире служит метод Амселя, основанный на обнаружении 4 общеизвестных критериев:
- специфические бели (однородные, светловато-белые, жидкие с неприятным запахом);
- отмечается повышение рН>4,5 (используются индикаторные полоски со шкалой);
- положительный аминный тест (усиление запаха «гнилой рыбы» при смешивании вагинального отделяемого с 10% раствором гидроокиси калия);
- наличие в мазках по Граму «ключевых клеток», лейкоцитов <20 в поле зрения.
Среди молекулярно-биологических методов исследования ПЦР в реальном времени имеет большое диагностическое значение: уменьшение числа лактобактерий, большое количество Gardnerella vaginalis – 105–7 КОЕ/мл, Prevotella, Peptostreptococcus spp., Fusobacterium spp., Mobiluncus spp., Micoplasma hominis, Ureaplasma urealiticum и др., отсутствием патогенной флоры.
Лечение. Вопрос тактики лечения БВ предусматривает два этапа: элиминацию условно-патогенных микроорганизмов и анаэробов и восстановление микрофлоры влагалища. На первом этапе применяют препараты метронидазола и клиндамицина, на втором – длительное применение эубиотиков. К препаратам комплексного действия для влагалищного применения относят:
- метронидазол 750 мг + миконазола нитрата 200 мг + лидокаин 100 мг – вагинальные суппозитории № 7;
- миконазол 0,1 г + метронидазол 0,1 г – вагинальные таблетки № 7;
- нифурател 0,1 г + нистатин 200 МЕ – вагинальные суппозитории № 8–12;
- нистатин + неомицин + полимиксин В – вагинальные свечи № 6;
- тернидазол + неомицина сульфат + нистатин + преднизолон – вагинальные свечи № 6 и др.
Но лечение БВ зачастую осложнено наличием во влагалище биопленок – сообществ разных микроорганизмов, в составе которых патогены способны выжить в самых неблагоприятных условиях с одной стороны, с другой – биопленки сами по себе являются причиной рецидивов вагинальных инфекций. Не так давно было установлено, что в результате подкисления влагалищной среды бактериальные пленки теряют свою прочность. Кислая среда способствует разрушению бактериальных пленок, что помогает эффективно устранить симптомы БВ и снизить риск рецидивов. Поэтому при рецидивирующем течении БВ после завершения стандартной терапии рекомендуется назначение закисляющих агентов (витамин C, молочная кислота) в течение 6 дней после окончания менструации на протяжении 6 менструальных циклов.
Вульвовагинальный кандидоз
Среди вагинальных инфекций ВВК прочно занимает второе место после БВ. ВВК – инфекционное поражение слизистой оболочки вульвы и влагалища, вызываемое дрожжеподобными грибами рода Candida. Наиболее часто – Candida albicans (50–80%), второе место занимают Candida glabrata (5–10%), реже заболевание обусловлено Candida krusei, Candida pseudotropicalis, Candida tropicalis и другими видами гриба Candida [9]. Описаны также случаи вагинальной грибковой инфекции, обусловленные Saccharomyces cerevisiae [10]. В соответствии с МКБ 10-го пересмотра ВВК не относится к инфекциям, передаваемым половым путем (ИППП) и является самостоятельной нозологической единицей (код В 37.3). Ввиду высокой распространенности самолечения истинная частота ВВК в общей популяции неизвестна, но, по данным разных авторов, заболевание диагностируется у 30–40% женщин с жалобами на выделения из половых путей. Считается, что клинические симптомы ВВК возникают по меньшей мере 1 раз в жизни у 3 из 4 женщин, при этом у 20–30% здоровых женщин репродуктивного возраста в составе микробиоценоза влагалища обнаруживаются грибы рода Candida, но признаки воспаления и иммуносупрессии у них отсутствуют [11].

В клинической практике ВВК принято различать первичный эпизод ВВК и рецидивирующий ВВК (РВВК). По данным разных авторов у 5–20,7% женщин репродуктивного возраста с первичным эпизодом ВВК в последующем наблюдаются рецидивы заболевания, сопровождающиеся значительными психосексуальными нарушениями и снижением качества жизни. ВВК считается рецидивирующим при наличии 4 и более эпизодов обострения в течение года [12].
Микроорганизмы рода Candida входят в состав нормальной микрофлоры влагалища. Заболевание обусловлено не просто наличием грибов, а их размножением в большом количестве, образованием псевдогифов, что, по мнению многих исследователей, способствует инвазии микроорганизма в глубокие слои слизистой оболочки и образованию микробных биопленок. Чаще всего кандидоз возникает при снижении местного и общего иммунитета. Имеются также исследования, доказывающие, что Candida albicans является мощным аллергеном и предрасполагает к развитию локальной аллергической реакции [13, 14]. К другим факторам риска развития ВВК относят: некомпенсированный сахарный диабет, патологию щитовидной железы, прием антибиотиков, прием КОК, а также ношение тесной одежды и белья из синтетических материалов, применение гигиенических прокладок и др.
Клиническая картина и диагностика. Клинические проявления ВВК: зуд и густые творожистые или пастообразные не очень обильные выделения, без запаха, болезненность при прикосновении к стенкам влагалища, ощущение жжения в области наружных половых органов, болезненность при половом контакте, ограничение половой активности. На основании только жалоб поставить правильный диагноз невозможно – ни один из названных симптомов не является специфичным.
Методами диагностики являются: клинический метод (анамнестические, данные, оценка жалоб), нативный препарат, обнаружение при микроскопии дрожжеподобных грибов и псевдогифов в выделениях из влагалища, предварительно разведенных 10% раствором гидроокиси калия или солевым раствором и окрашенных по Граму, культуральный метод (посев выделений на специальные среды).
Лечение. Терапия ВВК направлена на элиминацию возбудителя, устранение факторов риска и лечение сопутствующих заболеваний, утяжеляющих течение ВВК. Основное место в фармакотерапии принадлежит противогрибковым препаратам, назначать которые необходимо с учетом выявленного вида Candida и данных о чувствительности к основным лекарственным препаратам. Препараты для местной терапии:
- полиены: нистатин, натамицин 0,1 г № 3–6;
- имидазолы (вагинальные свечи): клотримазол 0,1 г № 7, эконазол 0,15 г № 3–5, миконазол 0,1 г № 7, изоконазол 0,6 г № 7, сертаконазол 300 мг № 1;
- комбинированные препараты: нистатин + неомицин + полимиксин В, миконазол 0,1 г + метронидазол 0,1 г, тернидазол + неомицина сульфат + нистатин + преднизолон;
- системные антимикотики: триазолоны: флуконазол 150 мг per os или в/в.
При осложненном течении ВВК длительность терапии увеличивается, и предпочтение отдается противогрибковым препаратам для системного применения, с целью предотвращения рецидивов – терапия продолжается в течение 6 месяцев. Однако доказано, что широкое применение противогрибковых препаратов, а также рост Candida non-albicans, обусловленных кандидозом, в какой-то степени объясняют неэффективность стандартных схем лечения, несмотря на широкий арсенал имеющихся на сегодняшний день антимикотических средств. Есть мнение, что развитие кандидозных биопленок также способствует развитию лекарственной устойчивости и рецидивированию ВВК. Известно, что грибы рода Candida практически всегда присутствуют в составе бактериальных биопленок (смешанные биопленки) и играют особую роль в развитии пленочных инфекций вследствие структурных особенностей мицелия. Моновидовые (чистые) биопленки кандид образуются в условиях агрессивной антибактериальной терапии, при формировании смешанных биопленок микробы-участники ускоряют рост друг друга. При образовании биопленок инфекционный процесс обретает затяжное течение и склонность к рецидивированию, снижается эффективность традиционной антимикробной терапии. Из вышесказанного следует, что для лечения кандидозной инфекции целесообразно применение препаратов, активных не только по отношению инфекционного агента, но и биопленок. В результате исследований, посвященных антибиопленочной эффективности различных веществ, неожиданной находкой оказался фентиконазол, ингибирующий образование биопленок C. albicans и вызывающий дисперсию зрелых смешанных биопленок. Дополнительным преимуществом фентиконазола является снижение активности аспартат протеаз – основного фактора патогенности Candida.
Неспицифический бактериальный вагинит
В последнее время уделяется большое внимание изучению микробиоценоза при неспецифическом бактериальном вагините. При этой патологии происходит вытеснение одним условно-патогенным видом микроорганизмов других членов микробного сообщества и сопровождается выраженной местной лейкоцитарной реакцией и другими признаками воспаления (МКБ-10 В95–96). В качестве инфекционной причины неспецифического вульвовагинита чаще всего выступают представители энтеробактерий (кишечные палочки – МКБ-10 В96.2, клебсиела – МКБ-10 В96.1, протей МКБ-10 В96.4, бактероиды, стафилококки – МКБ-10 В95.6–8, стрептококки – МКБ-10 В95 1–4 и др).
Неспецифический вульвовагинит может быть связан с нарушением правил гигиены, травматизацией наружных половых органов и влагалища, аллергическими состояниями и другой хронической экстрагенитальной и гинекологической патологией.
Клиническая картина и диагностика.
Диагностика вульвовагинитов обычно не представляет трудностей. Наличие в анамнезе указаний на тяжелые общие заболевания, воспалительные процессы половых органов (аднекситы), нарушения функции яичников и другие патологические состояния, способствующие возникновению заболевания, значительно облегчает диагностику. Большое внимание следует уделять типичным жалобам на зуд в области наружных половых органов, появление патологических выделений из половых путей (бели) и пр. Предположение о возможности развития вульвовагинита подтверждается при осмотре наружных половых органов и исследовании влагалища с помощью зеркал. Постоянными признаками неспецифических вульвовагинитов являются гиперемия и отек наружных половых органов, бели (водянисто-желтые или серозно-гнойные). В большинстве случаев неспецифические вульвовагиниты протекают со скудной симптоматикой, не имеют специфических признаков, обостряются на фоне интеркуррентных заболеваний и переохлаждения.
В мазках по Граму обнаруживаются лейкоциты >20 в поле зрения, микрофлора в большом количестве (чаще смешанная), нет патогенных микроорганизмов и грибов. Для уточнения этиологии воспалительного процесса прибегают к бактериологическому исследованию выделений, полученных из влагалища. При высевании возбудителей неспецифической инфекции (стафилококки, стрептококки, протей, кишечная палочка и пр.) необходимо определить их чувствительность к антибиотикам [15].
Лечение. Лечение неспецифических вульвовагинитов проводится амбулаторно и является непростой задачей в связи с недостаточной эффективностью многих терапевтических методов и высоким процентом развития рецидивов. Препарат выбора при лечении трихомониаза является метронидазол (2 г per os однократно или 0,375 г х 3 раза в сутки № 7). Альтернативная схема: тинидазол или орнидазол 2 г per os № 1. Во время беременности во II триместре – метронидазол вагинальные свечи № 7, с III триместра беременности – метронидазол 2 г per os однократно.
Лечение хламидийной инфекции. Рекомендованные схемы:
- азитромицин 1 г внутрь однократно;
- доксициклин 0,1 г внутрь х 2 раза в сутки 7 дней.
Альтернативные схемы:
- эритромицин 0,5 г внутрь х 4 раза в сутки 7 дней;
- офлоксацин 0,2 г внутрь х 2 раза в сутки 7 дней;
- рокситромицин 0, 15 г внутрь х 2 раза в сутки 7 дней;
- кларитромицин 0,25 г внутрь х 2 раза в сутки 7 дней.
Европейские рекомендации по лечению хламидийной инфекции у беременных женщин 2001 г., рекомендованные схемы: эритромицин основание 500 мг х 4 раза в день – 7 дней, или амоксициллин 500 мг х 3 раза в день – 7 дней, или джозамицин 750 мг х 2 раза в день – 7 дней. Альтернативные схемы: эритромицин основание 250 мг х 4 раза в сутки 14 дней, или эритромицина этилсукцинат 800 мг х 4 раза в день – 7 дней, или эритромицина этилсукцинат 400 мг х 4 раза в день – 14 дней, или азитромицин 1 г, однократно.
Схема лечения гонококковой инфекции: цефтриаксон 250 мг в/м однократно или амоксициллина клавуланат 1,2 г в/в однократно.
Со II триместра: азитромицин 0,5 г 2 раза в сутки № 4 per os.
Эффективность проводимого лечения во многом определяется точным выявлением возбудителя, назначением этиотропной терапии и хорошей переносимостью препарата. Согласно требованиям Международного экспертного совета Национального центра по контролю и профилактике заболеваний (США) при выборе препарата для лечения рекомендовано учитывать необходимость воздействия препарата на микробные ассоциации и отдавать предпочтение тем, которые обеспечивают элиминацию широкого спектра возможных возбудителей и обладают одновременно трихомонацидным, бактериоцидным, противогрибковым, противовоспалительным, противоэксудативным и антиаллергическим действием. Кроме того, лекарственное средство должно обладать минимальным системным действием на организм, быть удобным в применении и не оказывать выраженного повреждающего воздействия на лактобациллярную флору.
Выводы
Таким образом, проблема инфекционных заболеваний влагалища приобрела в последние годы особую актуальность. Во всем мире возросло число инфекционных заболеваний женских половых органов, среди которых ведущее место принадлежит бактериальному вагинозу, вульвовагинальному кандидозу и неспецифическим вульвовагинитам. По мнению некоторых авторов, вульвовагиниты являются самыми распространенными вагинальными инфекциями у женщин репродуктивного возраста.



